Class 12 : Chemistry (Hindi) – Lesson 6.हैलोऐल्केन तथा हैलोऐरीन
पाठ का विश्लेषण एवं विवेचन

🟢 1. नामकरण तथा संरचना
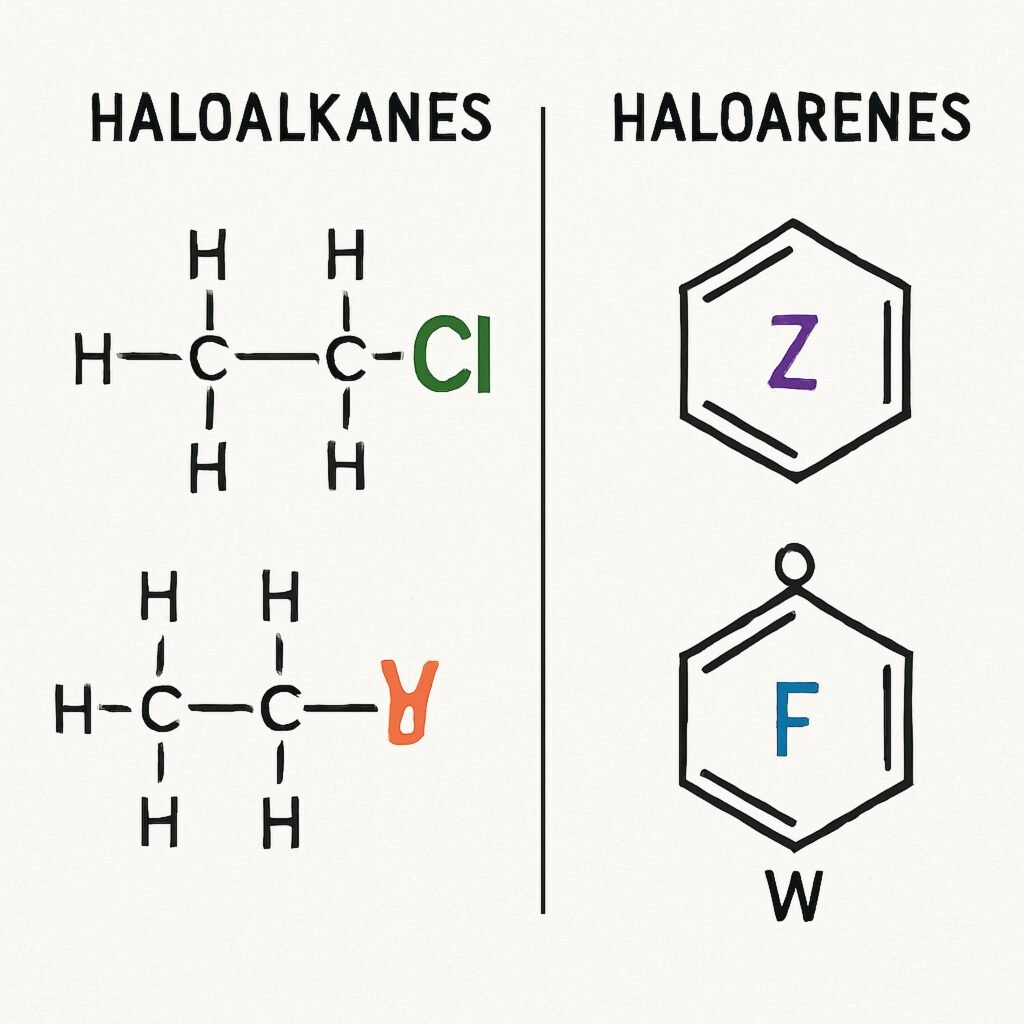
🌿 हैलोएल्केन – एलकिल समूह में हाइड्रोजन के स्थान पर हैलोजन परमाणु।
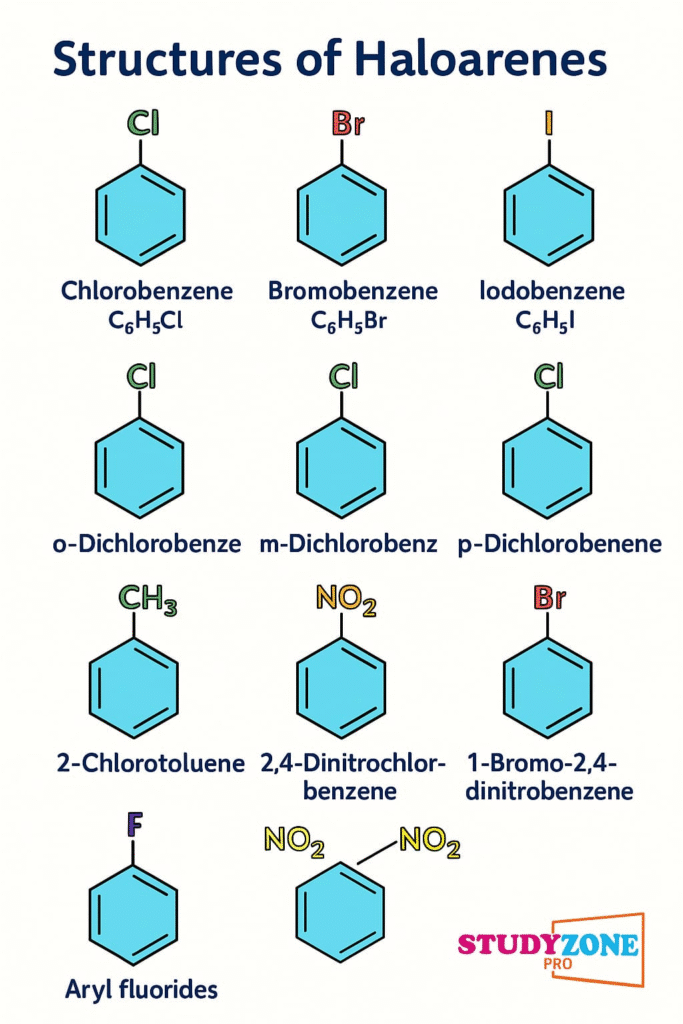
🌿 हैलोएरीन – एरीन (जैसे बेंजीन) में हाइड्रोजन के स्थान पर हैलोजन।
🧠 IUPAC नामकरण के मुख्य नियम:
✔️ सबसे लंबी श्रृंखला का चयन
✔️ हैलोजन को उपसर्ग के रूप में लिखना (जैसे – क्लोरो, ब्रोमो)
✔️ संख्या ऐसी चुनना जिससे हैलोजन को न्यूनतम स्थानांक मिले।
💡 उदाहरण:
CH₃–CHCl–CH₃ → 2-क्लोरोप्रोपेन
C₆H₅Cl → क्लोरोबेंजीन
🟡 2. वर्गीकरण
हैलोएल्केन को 3 भागों में वर्गीकृत किया जाता है:
1️⃣ प्राथमिक (1°): जिस कार्बन से हैलोजन जुड़ा है, वह केवल एक अन्य कार्बन से जुड़ा हो।
2️⃣ माध्यमिक (2°): वह कार्बन दो कार्बन से जुड़ा हो।
3️⃣ तृतीयक (3°): वह कार्बन तीन अन्य कार्बन से जुड़ा हो।
🧠 हैलोएरीन में हैलोजन सीधे एरीन वलय से जुड़ा होता है।
🔴 3. भौतिक गुण
⚡ अवस्था:
➡️ निम्नवर्गीय हैलोएल्केन गैसीय होते हैं।
➡️ मध्यमवर्गीय द्रव होते हैं और उच्चवर्गीय ठोस।
⚡ उबलनांक:
➡️ हैलोजन का भार बढ़ने पर उबलनांक भी बढ़ता है।
➡️ समवयवी यौगिकों में शाखाहीन यौगिकों का उबलनांक अधिक होता है।
⚡ घनत्व और घुलनशीलता:
➡️ जल में कम घुलनशील परन्तु कार्बनिक विलायकों में अधिक।
✏️ नोट: हैलोजन की उपस्थिति के कारण इन यौगिकों में ध्रुवता होती है।
🟢 4. कार्बनिक यौगिकों में हैलोजन का अभिग्रहण
प्रमुख अभिग्राही विधियाँ:
1️⃣ एल्केन से हैलोएल्केन: मुक्त कणीय अभिक्रिया द्वारा।
CH₄ + Cl₂ → CH₃Cl + HCl (उजाले में)
2️⃣ एल्कोहल से हैलोएल्केन:
ROH + HX → RX + H₂O
3️⃣ बेंजीन से हैलोएरीन:
C₆H₆ + Cl₂ → C₆H₅Cl + HCl (FeCl₃ उपस्थिति में)
💡 सुझाव: हैलोएरीन का निर्माण एलेक्ट्रोफिलिक प्रतिस्थापन द्वारा होता है।
🟡 5. रासायनिक अभिक्रियाएँ
(क) नाभिकीय प्रतिस्थापन अभिक्रियाएँ
➡️ हैलोएल्केन में हैलोजन बंध अपेक्षाकृत कमजोर होने के कारण प्रतिस्थापन संभव।
⚡ Sᴺ1 तंत्र: दो चरणों में होती है, माध्यमिक व तृतीयक हैलोएल्केन में प्रमुख।
⚡ Sᴺ2 तंत्र: एक चरणीय, प्राथमिक हैलोएल्केन में होती है।
(ख) विलोपन अभिक्रिया (Elimination):
➡️ जब क्षार की उपस्थिति में गर्म किया जाता है तो एलीन प्राप्त होता है।
CH₃CH₂Br + alc. KOH → CH₂=CH₂ + KBr + H₂O
🔴 6. हैलोएरीन की अभिक्रियाएँ
🧠 हैलोएरीन में C–X बंध आंशिक द्विबंध सरीखा होता है, इसलिए प्रतिस्थापन कठिन होता है।
✔️ प्रतिस्थापन अभिक्रिया: कठोर स्थितियों में संभव – NaOH के साथ गर्म करने पर।
✔️ धातु अभिक्रिया: Wurtz-Fittig अभिक्रिया – एरीन और एलकिल हैलाइड से हाइड्रोकार्बन।
🟢 7. प्रभाव – कार्बन–हैलोजन बंध की प्रकृति
⚡ C–X बंध ध्रुवीय होता है – C आंशिक धनावेश और X आंशिक ऋणावेश।
✔️ बंध की शक्ति (Bond Strength):
➡️ C–F > C–Cl > C–Br > C–I
✔️ बंध की लंबाई (Bond Length):
➡️ C–F < C–Cl < C–Br < C–I
✏️ नोट: C–F अत्यधिक मजबूत होता है इसलिए यह बंध रासायनिक अभिक्रिया हेतु अधिक प्रतिरोधक होता है।
🟡 8. पर्यावरणीय प्रभाव और विषाक्तता
🔴 कुछ हैलोयौगिक जैसे – DDT, BHC, क्लोरोफ्लोरोकार्बन (CFCs) पर्यावरण के लिए अत्यंत हानिकारक हैं।
🌿 CFCs ओज़ोन परत को क्षति पहुँचाते हैं।
🌿 DDT कीटनाशक होते हुए भी जीवों में वसा में एकत्रित होकर जैव-वृद्धि उत्पन्न करता है।
✏️ नोट: इनका प्रयोग संयमित और नियंत्रित ढंग से ही करना चाहिए।
🌟 यह अध्याय क्यों महत्वपूर्ण है? 🌟
(📦 Why This Lesson Matters Box)
➡️ औषधि, औद्योगिक विलायक, कीटनाशक और सिंथेटिक उत्पादों में हैलोयौगिकों का व्यापक उपयोग होता है।
➡️ यह अध्याय रासायनिक प्रतिक्रिया की बारीकियाँ और पर्यावरणीय चेतना, दोनों को जोड़ता है।
📝 Quick Recap: (स्मृति-पुनरावलोकन)
🔵 हैलोएल्केन = एल्केन + हैलोजन
🟢 हैलोएरीन = एरीन + हैलोजन
🟡 C–X बंध = ध्रुवीय, प्रतिक्रिया में सक्रिय
🔴 Sᴺ1 = दो चरण, Sᴺ2 = एक चरण
🟢 विलोपन से एलीन बनता है
🟡 DDT, CFC = पर्यावरण के लिए हानिकारक
🔴 उपयोग: औषधियाँ, विलायक, कीटनाशक
🟢 हैलोजन की उपस्थिति = अभिक्रियाशीलता में वृद्धि

🔻 सारांश
🔹 हैलोएल्केन और हैलोएरीन ऐसे यौगिक हैं जिनमें हाइड्रोजन की जगह हैलोजन परमाणु होता है। ये यौगिक रासायनिक प्रतिक्रिया में अत्यंत महत्वपूर्ण भूमिका निभाते हैं और जीवन के अनेक क्षेत्रों में इनका प्रयोग होता है।
🔸 नामकरण में IUPAC नियमों का पालन किया जाता है। हैलोएल्केन को प्राथमिक, माध्यमिक और तृतीयक वर्गों में विभाजित किया जाता है।
🔹 निर्माण विधियाँ जैसे – एल्केन या एल्कोहल से हैलोएल्केन, बेंजीन से हैलोएरीन, महत्वपूर्ण हैं। हैलोएरीन में एलेक्ट्रोफिलिक प्रतिस्थापन प्रमुख होता है।
🔸 रासायनिक अभिक्रियाएँ दो मुख्य प्रकार की होती हैं – नाभिकीय प्रतिस्थापन (Sᴺ1 और Sᴺ2) तथा विलोपन। हैलोएरीन अपेक्षाकृत कम प्रतिक्रियाशील होते हैं।
🔹 भौतिक गुण जैसे – उबलनांक, घुलनशीलता, घनत्व आदि हैलोजन की प्रकृति पर निर्भर करते हैं। बंध की शक्ति और लंबाई भी प्रतिक्रिया दर को प्रभावित करती है।
🔸 पर्यावरणीय प्रभाव भी इस अध्याय का महत्वपूर्ण भाग है। CFCs और DDT जैसे यौगिक पर्यावरण के लिए खतरनाक हैं।
यह अध्याय विद्यार्थी को हैलोयौगिकों की संरचना, प्रतिक्रिया, व्यवहार और उनके प्रभाव की व्यापक समझ प्रदान करता है। यह न केवल परीक्षा के दृष्टिकोण से, बल्कि व्यावहारिक जीवन और विज्ञान की दिशा में भी अत्यंत उपयोगी है।
————————————————————————————————————————————————————————————————————————————
पाठ्यपुस्तक के प्रश्न
प्रश्न 1. एल्कोहॉल को हेलोजन युक्त यौगिकों में बदलने के लिए प्रयुक्त प्रमुख विधियों का वर्णन कीजिए।
उत्तर:
एल्कोहॉल को हेलोजन युक्त यौगिकों (हैलोएल्केनों) में परिवर्तित करने के लिए निम्नलिखित प्रमुख विधियाँ प्रयुक्त होती हैं:
🔹 (1) हाइड्रोजन हेलाइड (HX) की सहायता से
R-OH + HX → R-X + H₂O
यह प्रतिक्रिया प्राथमिक, द्वितीयक तथा तृतीयक एल्कोहॉल पर निर्भर करती है।
➡️ उदाहरण:
CH₃CH₂OH + HBr → CH₃CH₂Br + H₂O
🔹 (2) फॉस्फोरस ट्राईहेलाइड (PX₃)
R-OH + PX₃ → R-X + H₃PO₃
➡️ उदाहरण:
3CH₃CH₂OH + PBr₃ → 3CH₃CH₂Br + H₃PO₃
🔹 (3) थियोनिल क्लोराइड (SOCl₂)
R-OH + SOCl₂ → R-Cl + SO₂ + HCl
यह विधि सर्वाधिक प्रभावी मानी जाती है क्योंकि उपोत्पाद गैसों के रूप में बाहर निकल जाते हैं।
प्रश्न 2. हेलोएल्केनों को ग्रिग्नार्ड अभिकारक द्वारा संश्लेषित करने की एक विधि को समझाइए।
उत्तर:
ग्रिग्नार्ड अभिकारक (RMgX) को सामान्यतः एल्काइल हेलाइड को मैग्नीशियम धातु की उपस्थिति में सूखे ईथर में प्रतिक्रिया कराकर तैयार किया जाता है:
🔹 R-X + Mg → RMgX (सूखे ईथर में)
➡️ उदाहरण:
CH₃Br + Mg → CH₃MgBr
यह अभिक्रिया नाभिकीय कार्बन और विद्युत ऋणात्मक हेलोजन के बीच के बंध को मैग्नीशियम द्वारा तोड़ने पर आधारित है, जिससे कार्बन आंशिक ऋणात्मक और मैग्नीशियम आंशिक धनात्मक होता है।
प्रश्न 3. प्राथमिक, द्वितीयक तथा तृतीयक हेलोएल्केनों की SN1 एवं SN2 अभिक्रियाशीलता की तुलना कीजिए।
उत्तर:
🔵 SN1 अभिक्रिया:
➡️ यह दो चरणों में होती है:
(i) कार्बोकैटायन का निर्माण
(ii) न्यूक्लियोफाइल का आक्रमण
➡️ यह अभिक्रिया तृतीयक > द्वितीयक > प्राथमिक के क्रम में होती है क्योंकि तृतीयक कार्बोकैटायन सबसे स्थिर होता है।
🔵 SN2 अभिक्रिया:
➡️ यह एक चरण में होती है; न्यूक्लियोफाइल द्वारा पीछे से आक्रमण
➡️ प्राथमिक > द्वितीयक > तृतीयक (क्योंकि तृतीयक में स्थानिक अवरोध बहुत होता है)
सारांश:
✔️ SN1 के लिए तृतीयक हेलोएल्केन सबसे उपयुक्त
✔️ SN2 के लिए प्राथमिक हेलोएल्केन सबसे उपयुक्त
प्रश्न 4. SN1 एवं SN2 अभिक्रियाओं की गति पर विलायक की प्रकृति का क्या प्रभाव पड़ता है?
उत्तर:
🔹 SN1 अभिक्रिया:
➡️ यह ध्रुवीय प्रोटिक विलायकों में तीव्र होती है क्योंकि वे कार्बोकैटायन को स्थिर करते हैं।
➡️ जैसे: जल, एथेनॉल आदि।
🔹 SN2 अभिक्रिया:
➡️ यह ध्रुवीय एप्रोटिक विलायकों में तीव्र होती है क्योंकि ये न्यूक्लियोफाइल को अवरोध नहीं करते।
➡️ जैसे: एसीटोन, DMSO, DMF आदि।
निष्कर्ष:
✔️ SN1 → ध्रुवीय प्रोटिक विलायक में तेज
✔️ SN2 → ध्रुवीय एप्रोटिक विलायक में तेज
प्रश्न 5. हेलोएल्केनों के अणु में कौन-से कारक उनके न्यूक्लियोफिलिक प्रतिस्थापन की गति को प्रभावित करते हैं?
उत्तर:
निम्न कारक न्यूक्लियोफिलिक प्रतिस्थापन की गति को प्रभावित करते हैं:
🔹 (1) उपवर्ती समूह का प्रकार – प्राथमिक, द्वितीयक, तृतीयक
🔹 (2) हेलोजन का प्रकार – I⁻ > Br⁻ > Cl⁻ > F⁻
🔹 (3) न्यूक्लियोफाइल की शक्ति – अधिक शक्तिशाली न्यूक्लियोफाइल अधिक गति
🔹 (4) विलायक का प्रकार – SN1 के लिए प्रोटिक, SN2 के लिए एप्रोटिक
🔹 (5) स्थानिक अवरोध – अधिक अवरोध से SN2 की गति कम
प्रश्न 6. C–X बंध की प्रकृति के आधार पर बताइए कि हेलोएल्केनों में कार्बन ऋणात्मक क्यों होता है?
उत्तर:
हेलोएल्केनों में C–X बंध ध्रुवीय होता है क्योंकि:
🔸 हेलोजन (X) की विद्युत ऋणात्मकता कार्बन से अधिक होती है।
🔸 परिणामस्वरूप, हेलोजन की ओर इलेक्ट्रॉनों का खिंचाव होता है।
🔸 इस कारण कार्बन पर आंशिक धनात्मक आवेश (δ⁺) और हेलोजन पर आंशिक ऋणात्मक आवेश (δ⁻) आ जाता है।
➡️ यही आंशिक धनात्मक आवेश न्यूक्लियोफाइल के आक्रमण को संभव बनाता है।
प्रश्न 7. कौन-से यौगिक न्यूक्लियोफिलिक प्रतिस्थापन अभिक्रिया नहीं दर्शाते? कारण सहित समझाइए।
उत्तर:
🔸 आरिल हैलोइड्स (जैसे: क्लोरोबेंज़ीन) न्यूक्लियोफिलिक प्रतिस्थापन नहीं दर्शाते क्योंकि:
(1) C–X बंध आंशिक द्वि-बंधीय स्वभाव रखता है – यह π-बन्धन के कारण होता है जो बेंजीन के p-कक्ष और हेलोजन के lone pair से होता है।
(2) कार्बोकैटायन अस्थिर होता है
(3) स्थानिक अवरोध – बेंजीन रिंग के कारण पीछे से न्यूक्लियोफाइल का आक्रमण संभव नहीं।
इसलिए, आरिल हैलोइड्स न्यूक्लियोफिलिक प्रतिस्थापन नहीं करते।
प्रश्न 8. न्यूक्लियोफिलिक प्रतिस्थापन अभिक्रिया में एल्कोहॉल का उपयोग नहीं किया जाता जबकि हेलोएल्केनों का किया जाता है। क्यों?
उत्तर:
🔹 एल्कोहॉल में –OH समूह एक खराब प्रस्थान समूह होता है क्योंकि यह स्वयं ही एक स्थिर आयन के रूप में नहीं निकल सकता।
🔹 जबकि हेलोएल्केनों में X⁻ (जैसे Cl⁻, Br⁻, I⁻) एक अच्छा प्रस्थान समूह होता है क्योंकि ये स्थिर आयन के रूप में आसानी से निकल जाते हैं।
🔸 इसलिए एल्कोहॉल न्यूक्लियोफिलिक प्रतिस्थापन नहीं करते जबकि हेलोएल्केन करते हैं।
प्रश्न 9. हेलोएल्केनों और हेलोएरीनों के भौतिक गुणों को सूचीबद्ध कीजिए।
उत्तर:
🔹 हेलोएल्केनों तथा हेलोएरीनों के प्रमुख भौतिक गुण:
(1) अवस्था: निम्नवर्तित सदस्य गैसें होती हैं; मध्यम सदस्य द्रव; भारी सदस्य ठोस।
(2) सांद्रता: जल में कम व कार्बनिक विलायकों में अधिक
(3) सांध्रता: अणु भार बढ़ने पर बढ़ती है
(4) उबलांक: अणु भार व इलेक्ट्रॉनों की संख्या पर निर्भर
(5) घनत्व: हाइड्रोजन की तुलना में अधिक
प्रश्न 10. SN1 तथा SN2 अभिक्रियाओं में प्रस्थान समूह का क्या महत्व है?
उत्तर:
🔹 SN1 और SN2 दोनों अभिक्रियाओं में प्रस्थान समूह (Leaving Group) का अच्छा होना आवश्यक होता है:
🔸 SN1 में:
➡️ पहला चरण – प्रस्थान समूह का स्वयं निकलना
➡️ अच्छा प्रस्थान समूह कार्बोकैटायन बनाने में सहायक होता है
🔸 SN2 में:
➡️ न्यूक्लियोफाइल के आक्रमण के साथ-साथ प्रस्थान समूह निकलता है
➡️ यदि प्रस्थान समूह अच्छा न हो तो अभिक्रिया की गति धीमी होती है
✔️ हेलोजन जैसे: Br⁻, I⁻, Cl⁻ अच्छे प्रस्थान समूह होते हैं
प्रश्न 11. क्लोरोबेंज़ीन में न्यूक्लियोफिलिक प्रतिस्थापन क्यों नहीं होता?
उत्तर:
🔹 क्लोरोबेंज़ीन में C–Cl बंध आंशिक द्विबंधीय स्वभाव रखता है
➡️ इसका कारण है: pπ–pπ संगमन जो Cl के lone pair और बेंजीन रिंग के p-कक्ष के बीच होता है
🔹 परिणामस्वरूप बंध मजबूत हो जाता है और टूटता नहीं
🔹 साथ ही, कार्बोकैटायन अस्थिर होता है व स्थानिक अवरोध भी अधिक होता है
✔️ इसीलिए क्लोरोबेंज़ीन न्यूक्लियोफिलिक प्रतिस्थापन नहीं करता
प्रश्न 12. SN1 अभिक्रिया की दो विशेषताएँ लिखिए।
उत्तर:
(1) दो चरणों में होती है:
(i) पहले चरण में प्रस्थान समूह निकलता है, कार्बोकैटायन बनता है
(ii) दूसरे चरण में न्यूक्लियोफाइल का आक्रमण होता है
(2) प्रतिक्रिया की गति केवल हेलोएल्केन की एकाग्रता पर निर्भर करती है, न्यूक्लियोफाइल पर नहीं।
Rate = k [RX]
प्रश्न 13. एक SN2 अभिक्रिया की दर को किन कारकों से नियंत्रित किया जा सकता है?
उत्तर:
SN2 अभिक्रिया की दर निम्नलिखित कारकों से नियंत्रित होती है:
🔸 (i) न्यूक्लियोफाइल की शक्ति: अधिक शक्तिशाली न्यूक्लियोफाइल → अधिक दर
🔸 (ii) सब्सट्रेट की प्रकृति: प्राथमिक > द्वितीयक > तृतीयक
🔸 (iii) स्थानिक अवरोध: अधिक अवरोध → कम दर
🔸 (iv) विलायक: एप्रोटिक विलायक → अधिक दर
🔸 (v) प्रस्थान समूह: बेहतर प्रस्थान समूह → अधिक दर
Rate = k [RX][Nu⁻]
प्रश्न 14. क्लोरोएरिन की रासायनिक संरचना क्या है?
उत्तर:
🔸 क्लोरोएरिन (2,4,6-Trichlorophenylmethyl chloride) एक कीटनाशक यौगिक है।
🔸 इसका रासायनिक नाम है: 1,1,1-Trichloro-2,2-bis(4-chlorophenyl)ethane (DDT)
🔸 इसमें बेंजीन रिंगों पर क्लोरीन और मिथाइल समूह उपस्थित होते हैं।
🔸 इसका सूत्र:
Cl-C₆H₄-CH(Cl)-C₆H₄-Cl
(यह संरचना DDT के समान होती है)
प्रश्न 15. SN1 और SN2 अभिक्रियाओं में अभिकारक की संरचना किस प्रकार प्रभावित करती है?
उत्तर:
🔸 SN1 अभिक्रिया में:
➡️ तृतीयक हेलोएल्केन → सर्वाधिक उपयुक्त क्योंकि कार्बोकैटायन अधिक स्थिर
➡️ प्राथमिक हेलोएल्केन → अनुपयुक्त
🔸 SN2 अभिक्रिया में:
➡️ प्राथमिक हेलोएल्केन → अधिक उपयुक्त
➡️ तृतीयक हेलोएल्केन → अनुपयुक्त, स्थानिक अवरोध के कारण
✔️ संरचना प्रतिक्रिया पथ तय करती है
प्रश्न 16. 1-ब्रॉमोप्रोपेन और 2-ब्रॉमोप्रोपेन के SN1 तथा SN2 अभिक्रियाशीलता की तुलना कीजिए।
उत्तर:
🔸 1-ब्रॉमोप्रोपेन (प्राथमिक हेलोएल्केन):
➡️ SN2 अभिक्रिया में अधिक सक्रिय
➡️ SN1 में कार्बोकैटायन अस्थिर, इसलिए कम सक्रिय
🔸 2-ब्रॉमोप्रोपेन (द्वितीयक हेलोएल्केन):
➡️ SN1 में मध्यम स्थायित्व का कार्बोकैटायन → SN1 संभव
➡️ SN2 में कुछ स्थानिक अवरोध होता है
✔️ निष्कर्ष:
1-ब्रॉमोप्रोपेन → SN2 उपयुक्त
2-ब्रॉमोप्रोपेन → SN1 तथा SN2 दोनों संभव, परंतु धीमी दर
प्रश्न 17. एल्कोहॉल से हेलोएल्केन बनाने की एक विधि दीजिए।
उत्तर:
🔹 एल्कोहॉल + PCl₅ → हेलोएल्केन + POCl₃ + HCl
उदाहरण:
CH₃CH₂OH + PCl₅ → CH₃CH₂Cl + POCl₃ + HCl
✔️ इस अभिक्रिया में PCl₅ एल्कोहॉल के –OH समूह को क्लोरीन से प्रतिस्थापित करता है।
अन्य अभिकर्मक: SOCl₂, PBr₃, HI + Red P
प्रश्न 18. SN1 तथा SN2 अभिक्रियाओं में अंतर्वर्ती अवस्थाओं का आरेख चित्रित कीजिए।
उत्तर:
🔹 SN1 अभिक्रिया में:
➡️ चरण 1: RX → R⁺ + X⁻ (कार्बोकैटायन बनता है)
➡️ चरण 2: R⁺ + Nu⁻ → R–Nu
🔹 SN2 अभिक्रिया में:
➡️ एक ही चरण: Nu⁻ + RX → [Transition State] → R–Nu + X⁻
✔️ Transition state में न्यूक्लियोफाइल तथा प्रस्थान समूह दोनों जुड़े होते हैं।
(आरेख आपको अभ्यास पुस्तिका या NCERT चित्रों में स्पष्ट रूप से मिल सकता है।)
प्रश्न 19. क्लोरोबेंज़ीन के न्यूक्लियोफिलिक प्रतिस्थापन में इलेक्ट्रॉन-प्रेरण प्रभाव तथा स्थानिक अवरोध की क्या भूमिका होती है?
उत्तर:
🔹 इलेक्ट्रॉन-प्रेरण प्रभाव:
➡️ –I प्रभाव के कारण Cl इलेक्ट्रॉन खींचता है
➡️ परंतु –M प्रभाव से lone pair रेज़ोनेंस में जाता है → C–Cl बंध द्विबंध स्वभाव प्राप्त करता है
➡️ बंध मजबूत हो जाता है → न्यूक्लियोफिलिक प्रतिस्थापन कठिन हो जाता है
🔹 स्थानिक अवरोध:
➡️ बेंजीन रिंग का समतल ढांचा तथा Cl की स्थिति न्यूक्लियोफाइल के आक्रमण में बाधा उत्पन्न करती है
✔️ इसलिए क्लोरोबेंज़ीन न्यूक्लियोफिलिक प्रतिस्थापन में निष्क्रिय होता है।
प्रश्न 20. SN1 अभिक्रिया में स्टीरियोकेमिस्ट्री कैसे प्रभावित होती है?
उत्तर:
🔸 SN1 अभिक्रिया में कार्बोकैटायन मध्यवर्ती बनता है जो समतल रचना वाला होता है।
🔹 न्यूक्लियोफाइल समतल के दोनों ओर से आक्रमण कर सकता है → परिणामस्वरूप racemization होती है
🔸 उदाहरण: ऑप्टिकली सक्रिय 2-ब्रॉमोब्यूटेन → racemic मिक्सचर बनाता है SN1 द्वारा
✔️ SN1 अभिक्रिया → ऑप्टिकल निष्क्रियता ला सकती है
प्रश्न 21. SN2 अभिक्रिया में उलटाव क्यों होता है?
उत्तर:
🔸 SN2 अभिक्रिया एक ही चरण में होती है जिसमें न्यूक्लियोफाइल पीछे से आक्रमण करता है
🔹 यह ‘back side attack’ कहलाता है
➡️ इसके कारण प्रतिक्रिया के दौरान कार्बन की संरचना पलट जाती है
🔸 इसे Walden inversion कहते हैं
✔️ SN2 अभिक्रिया → स्टीरियोकेमिकल उलटाव (Inversion of configuration) उत्पन्न करती है
प्रश्न 22. हेलोएल्केनों से एल्कोहॉल प्राप्त करने की विधि बताइए।
उत्तर:
🔹 हेलोएल्केन + NaOH (जलीय) → एल्कोहॉल + NaX
उदाहरण:
CH₃CH₂Cl + NaOH (aq) → CH₃CH₂OH + NaCl
✔️ यह SN2 अभिक्रिया होती है, विशेषतः प्राथमिक हेलोएल्केन के लिए उपयुक्त
प्रश्न 23. क्लोरोबेंज़ीन को बेंजीन सल्फोनिक अम्ल में परिवर्तित कीजिए।
उत्तर:
🔹 क्लोरोबेंज़ीन को NaOH के साथ उच्च ताप (300°C) और उच्च दाब में गरम किया जाता है:
C₆H₅Cl + NaOH → C₆H₅OH + NaCl
🔸 फिर फिनोल को Oleum के साथ क्रियाविंत कर:
C₆H₅OH + SO₃ → C₆H₄OH–SO₃H
✔️ इस प्रकार बेंजीन सल्फोनिक अम्ल प्राप्त होता है
प्रश्न 24. DDT क्या है? इसकी संरचना और प्रयोग बताइए।
उत्तर:
🔹 DDT का पूर्ण नाम है: डाईक्लोरोडाइफेनिलट्राईक्लोरोएथेन
🔸 संरचना:
Cl–C₆H₄–CH(Cl)–C₆H₄–Cl
➡️ इसमें दो बेंजीन रिंग और तीन क्लोरीन परमाणु होते हैं
🔹 उपयोग:
✔️ यह एक प्रभावशाली कीटनाशक (Insecticide) है
✔️ मलेरिया फैलाने वाले मच्छरों के विरुद्ध प्रयुक्त होता है
🔸 पर्यावरण में अधिक समय तक बना रहता है, जिससे जैव संचयन की समस्या होती है
प्रश्न 25. SN1 और SN2 अभिक्रियाओं में प्रमुख अंतर लिखिए।
उत्तर:
🔹 SN1 अभिक्रिया:
▪️ दो चरणों में होती है
▪️ मध्यवर्ती में कार्बोकैटायन बनता है
▪️ अभिक्रिया दर केवल सब्सट्रेट पर निर्भर (rate ∝ [RX])
▪️ माध्यम का ध्रुवीय होना आवश्यक
▪️ स्टीरियोकेमिकल रूप से racemization होती है
▪️ तृतीयक हैलोएल्केन उपयुक्त होते हैं
🔹 SN2 अभिक्रिया:
▪️ एक चरणीय अभिक्रिया
▪️ कोई मध्यवर्ती नहीं, संक्रमण अवस्था बनती है
▪️ दर न्यूक्लियोफाइल व सब्सट्रेट दोनों पर निर्भर (rate ∝ [RX][Nu⁻])
▪️ माध्यम इतना आवश्यक नहीं
▪️ स्टीरियोकेमिकल इनवर्ज़न होता है
▪️ प्राथमिक हैलोएल्केन उपयुक्त होते हैं
प्रश्न 26. एल्कोहॉल से हेलोएल्केन की तैयारी के लिए थायोनिल क्लोराइड का उपयोग क्यों वांछनीय है?
उत्तर:
🔹 थायोनिल क्लोराइड (SOCl₂) से एल्कोहॉल की अभिक्रिया में केवल गैसीय उत्पाद बनते हैं:
ROH + SOCl₂ → RCl + SO₂↑ + HCl↑
✔️ यह विधि उपयुक्त है क्योंकि
▪️ उत्पाद को शुद्ध करना आसान होता है
▪️ अभिक्रिया को नियंत्रित करना सरल होता है
▪️ उच्च उपज प्राप्त होती है
प्रश्न 27. SN1 अभिक्रिया की दर पर घुलनशीलता का क्या प्रभाव होता है?
उत्तर:
🔹 SN1 अभिक्रिया ध्रुवीय माध्यमों में अधिक तीव्रता से होती है
▪️ जैसे: जल, ऐल्कोहल
🔹 कारण: ये माध्यम कार्बोकैटायन के निर्माण को स्थायित्व प्रदान करते हैं
✔️ उच्च ध्रुवीयता वाला माध्यम → तेजी से आयनन → उच्च दर
प्रश्न 28. क्लोरोबेंज़ीन का न्यूक्लियोफिलिक प्रतिस्थापन क्यों कठिन है?
उत्तर:
🔹 क्लोरोबेंज़ीन में Cl का lone pair बेंजीन रिंग के साथ संक्रिया करता है → C–Cl बंध आंशिक द्विबंध बन जाता है
🔹 यह बंध मजबूत होता है और टूटने में कठिनाई होती है
🔹 साथ ही, बेंजीन रिंग के समतल ढांचे के कारण न्यूक्लियोफाइल के लिए पीछे से आक्रमण कठिन होता है
✔️ इसलिए क्लोरोबेंज़ीन SN अभिक्रियाओं में निष्क्रिय रहता है
प्रश्न 29. SN1 अभिक्रिया के लिए उपयुक्त सब्सट्रेट कौन-से हैं?
उत्तर:
🔹 वे सब्सट्रेट जो कार्बोकैटायन को स्थिर बना सकें
▪️ तृतीयक हैलोएल्केन (3°)
▪️ एलाइलिक, बेन्जाइलिक, और अरोमैटिक यौगिक
🔹 अधिक शाखा वाले सब्सट्रेट
✔️ क्योंकि इनसे बने कार्बोकैटायन अधिक स्थिर होते हैं
प्रश्न 30. SN2 अभिक्रिया में प्राथमिक हैलोएल्केन सबसे अधिक सक्रिय क्यों होते हैं?
उत्तर:
🔹 SN2 अभिक्रिया में न्यूक्लियोफाइल पीछे से आक्रमण करता है
🔹 यदि कार्बन अधिक भीड़ वाला (steric hindered) हो तो यह आक्रमण कठिन हो जाता है
▪️ प्राथमिक हैलोएल्केन में कार्बन कम भीड़ वाला होता है
✔️ इसलिए SN2 के लिए सर्वाधिक उपयुक्त होते हैं
प्रश्न 31. क्लोरोबेंज़ीन से फिनोल बनाने की विधि लिखिए।
उत्तर:
🔹 क्लोरोबेंज़ीन को NaOH के साथ उच्च ताप (623 K) और उच्च दाब (300 atm) में गरम करते हैं:
C₆H₅Cl + NaOH → C₆H₅OH + NaCl
✔️ इस प्रक्रिया में न्यूक्लियोफिलिक प्रतिस्थापन द्वारा फिनोल बनता है
प्रश्न 32. DDT का निर्माण कैसे होता है?
उत्तर:
🔹 क्लोरोबेंज़ीन और क्लोरल (CCl₃CHO) के संक्षालन से DDT प्राप्त होता है:
2 C₆H₅Cl + CCl₃CHO → DDT + H₂O
✔️ यह अभिक्रिया अम्लीय माध्यम में होती है
प्रश्न 33. हेलोएल्केन के उपयोग लिखिए।
उत्तर:
🔹 हेलोएल्केन का प्रयोग:
▪️ औषधियों में (जैसे क्लोरोफॉर्म)
▪️ कीटनाशकों में (जैसे DDT)
▪️ विलायक के रूप में (जैसे CCl₄)
▪️ अग्निशामकों में (जैसे CBrCl₃)
▪️ जैव रसायन संश्लेषण में
✔️ ये यौगिक उद्योग व चिकित्सा दोनों में उपयोगी हैं
————————————————————————————————————————————————————————————————————————————
अन्य महत्वपूर्ण प्रश्न
(CBSE MODEL प्रश्न पत्र)
सिर्फ इसी पाठ से निर्मित CBSE MODEL प्रश्न पत्र।
Q1. किसी गैल्वैनिक कोशिका में निम्नलिखित में से कौन-सी प्रक्रिया स्वैच्छिक होती है?
(A) ऑक्सीकरण
(B) अपचयन
(C) दोनों
(D) कोई नहीं
उत्तर: (C)
Q2. विद्युत अपघटन के समय, इलेक्ट्रोड क्षमता को किससे व्यक्त किया जाता है?
(A) वोल्ट
(B) एम्पीयर
(C) ओम
(D) जूल
उत्तर: (A)
Q3. निम्नलिखित में से कौन-सी धातु सबसे अधिक अपचयशील होती है?
(A) सोना
(B) चांदी
(C) लोहा
(D) पोटैशियम
उत्तर: (D)
Q4. फ़ैराडे का द्वितीय नियम निम्न में से किससे संबंधित है?
(A) विद्युत धारा
(B) आयनन ऊर्जा
(C) इलेक्ट्रोड क्षमता
(D) इलेक्ट्रोलाइट द्वारा मुक्त पदार्थ का द्रव्यमान
उत्तर: (D)
Q5. मानक इलेक्ट्रोड विभव का मात्रक क्या है?
(A) कूलॉम्ब
(B) वोल्ट
(C) एम्पीयर
(D) सेकंड
उत्तर: (B)
Q6. निम्नलिखित में से कौन-सा कथन सही है?
(A) एनोड पर अपचयन होता है
(B) कैथोड पर ऑक्सीकरण होता है
(C) एनोड पर ऑक्सीकरण और कैथोड पर अपचयन होता है
(D) दोनों इलेक्ट्रोड पर ऑक्सीकरण होता है
उत्तर: (C)
Q7. यदि किसी कोशिका का विभव धनात्मक है, तो इसका अर्थ है:
(A) अभिक्रिया स्वतः नहीं होगी
(B) अभिक्रिया स्वतः होगी
(C) कोई प्रतिक्रिया नहीं होगी
(D) उपरोक्त सभी
उत्तर: (B)
Q8. निम्नलिखित में से कौन-सा सेल एक प्राथमिक सेल है?
(A) लेड-एसिड बैटरी
(B) निकेल-कैडमियम सेल
(C) वोल्टाइक सेल
(D) लिथियम आयन बैटरी
उत्तर: (C)
Q9. विद्युत अपघटन में मुक्त होने वाले पदार्थ की मात्रा किस पर निर्भर करती है?
(A) विद्युत धारा
(B) समय
(C) विद्युत धारा और समय
(D) तापमान
उत्तर: (C)
Q10. निम्नलिखित में से कौन-सी इकाई विद्युत चालकता के लिए प्रयुक्त होती है?
(A) S·cm⁻¹
(B) Ω
(C) A
(D) V·s
उत्तर: (A)
Q11.
अभिकथन (Assertion): जस्ता की इलेक्ट्रोड क्षमता ऋणात्मक होती है।
कारण (Reason): जस्ता आसानी से इलेक्ट्रॉन त्यागता है।
(A) A और R दोनों सही हैं और R, A की सही व्याख्या है।
(B) A और R दोनों सही हैं, पर R, A की सही व्याख्या नहीं है।
(C) A सही है, R गलत है।
(D) A गलत है, R सही है।
उत्तर: (A)
Q12.
अभिकथन (Assertion): फ्यूल सेल प्रदूषण मुक्त होते हैं।
कारण (Reason): इनमें जल ही एकमात्र उत्पाद होता है।
(A) A और R दोनों सही हैं और R, A की सही व्याख्या है।
(B) A और R दोनों सही हैं, पर R, A की सही व्याख्या नहीं है।
(C) A सही है, R गलत है।
(D) A गलत है, R सही है।
उत्तर: (A)
Q13. सेल विभव को प्रभावित करने वाला प्रमुख कारक क्या है?
(A) तापमान
(B) दाब
(C) सांद्रता
(D) उपरोक्त सभी
उत्तर: (D)
Q14. नर्न्स्ट समीकरण किस स्थिति में प्रयुक्त नहीं होती?
(A) मानक परिस्थितियों में
(B) जब तापमान बहुत अधिक हो
(C) जब एक इलेक्ट्रोड निष्क्रिय हो
(D) जब सेल संतुलन में हो
उत्तर: (D)
Q15. यदि किसी कोशिका का EMF = 0 हो, तो इसका अर्थ है:
(A) प्रतिक्रिया आगे बढ़ेगी
(B) प्रतिक्रिया पिछे जाएगी
(C) प्रतिक्रिया संतुलन में है
(D) प्रतिक्रिया बहुत तीव्र है
उत्तर: (C)
Q16.
स्थिति: एक विद्युत अपघटन अभिक्रिया में 2 फॅराडे विद्युत प्रवाहित की गई।
प्रश्न: यदि पदार्थ की समतुल्य द्रव्यमान 27 हो, तो मुक्त धातु का द्रव्यमान कितना होगा?
(A) 54 g
(B) 13.5 g
(C) 27 g
(D) 108 g
उत्तर: (A)
Q17.
स्थिति: एक कोपर इलेक्ट्रोड को किसी अम्लीय घोल में डुबोया गया।
प्रश्न: किस स्थिति में ऑक्सीकरण होगा?
(A) यदि इलेक्ट्रोड क्षमता ऋणात्मक हो
(B) यदि इलेक्ट्रोड क्षमता धनात्मक हो
(C) यदि कोई धारा प्रवाहित न हो
(D) यदि सेल में इलेक्ट्रोलाइट न हो
उत्तर: (A)
Q18.
Q: किसी विद्युत अपघटन में 1 फॅराडे विद्युत प्रवाहित की गई। Cu²⁺ + 2e⁻ → Cu के अनुसार मुक्त तांबे का द्रव्यमान क्या होगा?
(A) 31.75 g
(B) 63.5 g
(C) 127 g
(D) 1 g
उत्तर: (B)
Q19. दो तत्व A और B की मानक अपचय क्षमताएँ क्रमशः -0.76 V और +0.34 V हैं। बताइए कि इनसे बनी गैल्वैनिक सेल में कौन-सा तत्व एनोड होगा?
उत्तर:
जिस तत्व की अपचय क्षमता अधिक ऋणात्मक होती है, वही अधिक आसानी से ऑक्सीकरण करता है और एनोड पर होता है।
यहाँ A की अपचय क्षमता -0.76 V है जो B (+0.34 V) से अधिक ऋणात्मक है।
इसलिए, A एनोड होगा और B कैथोड।
Q20. 1 फॅराडे विद्युत प्रवाहित करने पर किस तत्व से 1 ग्राम समतुल्य द्रव्यमान मुक्त होता है? इसे सिद्ध कीजिए।
उत्तर:
फैरेडे का प्रथम नियम कहता है कि मुक्त पदार्थ का द्रव्यमान विद्युत की मात्रा के समानुपाती होता है।
मास = (Eq. wt × Q) / F
यहाँ Q = 1 F, Eq. wt = E
∴ मास = E × 1 / 1 = E
इसलिए, 1 फॅराडे विद्युत प्रवाह से 1 समतुल्य द्रव्यमान मुक्त होता है।
Q21.
प्रश्न: यदि किसी सेल की EMF = 1.1 V है, तो बताइए कि क्या यह प्रतिक्रिया स्वतः होगी या नहीं?
उत्तर:
यदि किसी गैल्वैनिक सेल का EMF धनात्मक होता है, तो प्रतिक्रिया स्वतः चलती है।
यहाँ EMF = +1.1 V है ⇒ प्रतिक्रिया स्वतः होगी।
Q22.
प्रश्न: विद्युत चालकता और मोलर चालकता में अंतर स्पष्ट कीजिए।
उत्तर:
🔹 विद्युत चालकता (κ): संपूर्ण घोल की इकाई आयतन की चालकता। इकाई: S·cm⁻¹
🔹 मोलर चालकता (Λₘ): 1 मोल इलेक्ट्रोलाइट से प्राप्त चालकता।
Λₘ = κ × 1000 / C
जहाँ C = सांद्रता (mol/L)
मोलर चालकता, संख्यात्मक दृष्टि से इलेक्ट्रोलाइट की प्रकृति और उसका हद तक आयनन दर्शाती है।
Q23.
प्रश्न: द्रव्यमान क्रिया का नियम उपयोग कर के दर्शाइए कि सेल विभव कैसे सांद्रता पर निर्भर करता है।
उत्तर:
द्रव्यमान क्रिया का नियम के अनुसार:
E = E° – (0.0591 / n) × log([Red]/[Ox])
यहाँ, E सेल विभव है, जो स्पष्टतः सांद्रता पर निर्भर करता है।
जैसे-जैसे सांद्रता घटती है, log([Red]/[Ox]) का मान बढ़ता है जिससे E घटता है।
∴ सेल विभव सांद्रता के साथ परिवर्तित होता है।
🔷 भाग C – प्रश्न 24 से 28 (प्रत्येक 3 अंक)
(मध्यम लंबाई के संख्यात्मक या तर्क आधारित प्रश्न)
Q24.
प्रश्न: 0.01 M CH₃COOH का मोलर चालकता 4.95 × 10⁻⁴ S·cm²/mol है और इसका Λₘ⁰ = 390.5 S·cm²/mol है।
आयनन की डिग्री (α) एवं आयनिक स्थिरांक (Ka) ज्ञात कीजिए।
उत्तर:
α = Λₘ / Λₘ⁰
= (4.95 × 10⁻⁴) / (390.5)
≈ 1.27 × 10⁻⁶
Ka = Cα² / (1 – α)
≈ (0.01)(1.27 × 10⁻⁶)² / (1)
≈ 1.61 × 10⁻¹⁴
उत्तर: α ≈ 1.27 × 10⁻⁶, Ka ≈ 1.61 × 10⁻¹⁴
Q25.
प्रश्न: एक विद्युत अपघटन प्रक्रिया में 2 फॅराडे विद्युत प्रवाहित की गई। यदि Zn²⁺ + 2e⁻ → Zn, तो कितने ग्राम Zn मुक्त होगा? (Zn = 65.38)
उत्तर:
1 फॅराडे ⇒ 1 समतुल्य द्रव्यमान ⇒ Zn / 2 = 65.38 / 2 = 32.69 g
2 फॅराडे ⇒ 2 × 32.69 = 65.38 g
उत्तर: 65.38 ग्राम जिंक मुक्त होगा।
Q26.
प्रश्न: यदि किसी Zn-Cu सेल में Zn²⁺ की सांद्रता 1.0 M तथा Cu²⁺ की 0.01 M है, तो नर्न्स्ट समीकरण द्वारा EMF ज्ञात कीजिए।
E° = 1.10 V, n = 2
उत्तर:
E = E° – (0.0591/n) × log([Cu²⁺]/[Zn²⁺])
E = 1.10 – (0.0591/2) × log(0.01/1)
= 1.10 – 0.02955 × (–2)
= 1.10 + 0.0591
= 1.1591 V
उत्तर: 1.1591 V
Q27.
प्रश्न: किसी विलयन की विद्युत चालकता 2.0 × 10⁻³ S·cm⁻¹ है और सांद्रता 0.001 mol/L है। मोलर चालकता ज्ञात कीजिए।
उत्तर:
Λₘ = κ × 1000 / C
= (2.0 × 10⁻³) × 1000 / 0.001
= 2.0 × 10³ S·cm²/mol
उत्तर: 2000 S·cm²/mol
Q28.
प्रश्न: एक बैटरी 3.0 A धारा 2 घंटे तक देती है। कितने फॅराडे विद्युत प्रवाहित हुई?
उत्तर:
Q = I × t = 3.0 × (2 × 3600) = 21600 C
1 फॅराडे = 96500 C
⇒ F = 21600 / 96500 ≈ 0.224 F
उत्तर: 0.224 फॅराडे
Q29.
स्थिति: एक गैल्वैनिक सेल बनाया गया है जिसमें Zn और Ag का प्रयोग किया गया है।
आवर्त सारणी के अनुसार:
E°(Zn²⁺/Zn) = –0.76 V,
E°(Ag⁺/Ag) = +0.80 V
(a) इस सेल की सेल अभिक्रिया लिखिए।
(b) इस सेल की EMF ज्ञात कीजिए।
(c) बताइए कि सेल में ऑक्सीकरण और अपचयन कहाँ होगा।
(d) यदि Zn²⁺ = 1.0 M और Ag⁺ = 0.01 M है, तो EMF ज्ञात कीजिए।
उत्तर:
(a) Zn(s) + 2Ag⁺(aq) → Zn²⁺(aq) + 2Ag(s)
(b) E°cell = E°(cathode) – E°(anode)
= 0.80 – (–0.76) = 1.56 V
(c) ऑक्सीकरण Zn पर (एनोड), अपचयन Ag⁺ पर (कैथोड) होता है।
(d) Nernst समीकरण:
E = E° – (0.0591 / n) log([Zn²⁺]/[Ag⁺]²)
E = 1.56 – (0.0591 / 2) log(1 / (0.01)²)
= 1.56 – 0.02955 × log(1 / 10⁻⁴)
= 1.56 – 0.02955 × 4
= 1.56 – 0.1182 = 1.4418 V
Q30.
स्थिति: एक बैटरी से 5.0 A धारा 30 मिनट तक प्रवाहित की जाती है। बैटरी से Cu²⁺ आयनों का अपघटन होता है।
(a) कुल आवेश (Q) ज्ञात कीजिए।
(b) कितने ग्राम ताँबा मुक्त होगा? (Cu = 63.5 g/mol)
(c) इस क्रिया में कितने मोल इलेक्ट्रॉन प्रवाहित होते हैं?
(d) प्रतिक्रिया का समीकरण लिखिए।
उत्तर:
(a) Q = I × t = 5 × (30 × 60) = 9000 C
(b) Cu²⁺ + 2e⁻ → Cu
n = 2
m = (E × Q) / (n × F)
= (63.5 × 9000) / (2 × 96500)
≈ 2.96 g
(c) n = Q / F = 9000 / 96500 ≈ 0.093 mol
(d) Cu²⁺ + 2e⁻ → Cu (अपचयन)
Q31.
स्थिति: एक विद्युत अपघटन सेल में NaCl के जलीय विलयन का अपघटन किया जाता है।
(a) एनोड और कैथोड पर क्या प्रतिक्रियाएँ होंगी?
(b) उत्पाद गैसों की पहचान कीजिए।
(c) कैथोड पर H₂ बनने के लिए कितने फॅराडे विद्युत की आवश्यकता है?
(d) प्रतिक्रिया का पूर्ण समीकरण लिखिए।
उत्तर:
(a)
एनोड: 2Cl⁻ → Cl₂(g) + 2e⁻
कैथोड: 2H₂O + 2e⁻ → H₂(g) + 2OH⁻
(b) एनोड पर Cl₂ गैस, कैथोड पर H₂ गैस उत्पन्न होती है।
(c) H₂ के लिए 2e⁻ ⇒ 1 F (1 mol e⁻ per H atom)
∴ 1 mol H₂ हेतु 1 F
(d) पूर्ण अभिक्रिया:
2Cl⁻ + 2H₂O → Cl₂(g) + H₂(g) + 2OH⁻
🔷 Section E: प्रश्न 32 से 35 (प्रत्येक 5 अंक)
(दीर्घ उत्तर / संख्यात्मक समाधान वाले प्रश्न)
Q32.
प्रश्न: नर्न्स्ट समीकरण की व्युत्पत्ति कीजिए और यह स्पष्ट कीजिए कि EMF किस प्रकार सांद्रता पर निर्भर करता है।
उत्तर:
कोई सामान्य रेडॉक्स अभिक्रिया:
aA + bB ⇌ cC + dD
Nernst समीकरण:
E = E° – (RT / nF) ln([C]^c [D]^d / [A]^a [B]^b)
25°C पर:
E = E° – (0.0591 / n) log([C]^c [D]^d / [A]^a [B]^b)
🌟 यदि उत्पादों की सांद्रता बढ़ेगी, तो log(Q) का मान बढ़ेगा ⇒ EMF घटेगा।
🌟 यदि अभिकारकों की सांद्रता बढ़ेगी ⇒ EMF बढ़ेगा।
निष्कर्ष:
सेल विभव सीधा सम्बन्ध रखता है सांद्रता अनुपात से।
Q33.
प्रश्न: फैरेडे के द्वितीय नियम की व्युत्पत्ति कीजिए और स्पष्ट कीजिए कि जब एक ही विद्युत मात्रा कई इलेक्ट्रोलाइटों में प्रवाहित की जाती है, तो मुक्त द्रव्यमान कैसे जुड़े होते हैं।
उत्तर:
फैरेडे द्वितीय नियम:
यदि एक ही मात्रा की विद्युत अलग-अलग पदार्थों पर प्रवाहित की जाए, तो मुक्त द्रव्यमान उनके रासायनिक समतुल्यता के अनुपात में होगा।
m₁ / E₁ = m₂ / E₂ = … = Q / F
जहाँ m = द्रव्यमान, E = समतुल्यता द्रव्यमान = Atomic Mass / Valency
🌿 उदाहरण:
Cu²⁺ और Ag⁺ को एक साथ विद्युत अपघटन किया जाए:
E(Cu) = 63.5 / 2 = 31.75
E(Ag) = 108 / 1 = 108
m(Cu)/31.75 = m(Ag)/108
∴ द्रव्यमान रासायनिक समतुल्यता के अनुपात में निकलते हैं।
Q34.
प्रश्न:
0.01 M CH₃COOH विलयन की मोलर चालकता 4.95 × 10⁻⁴ S·cm²/mol है।
Λₘ⁰ = 390.5 S·cm²/mol
आयनन डिग्री और आयनिक स्थिरांक ज्ञात कीजिए।
उत्तर:
α = Λₘ / Λₘ⁰
= (4.95 × 10⁻⁴) / 390.5
≈ 1.27 × 10⁻⁶
Ka = Cα² / (1 – α)
≈ (0.01)(1.27 × 10⁻⁶)² / (1)
≈ 1.61 × 10⁻¹⁴
उत्तर: α ≈ 1.27 × 10⁻⁶, Ka ≈ 1.61 × 10⁻¹⁴
Q35.
प्रश्न: निम्नलिखित इलेक्ट्रोड संभावनाओं के लिए Daniell सेल की EMF ज्ञात कीजिए, साथ ही उसका उपयोग करते हुए कार्य सिद्ध कीजिए।
E°(Zn²⁺/Zn) = –0.76 V
E°(Cu²⁺/Cu) = +0.34 V
उत्तर:
(a) EMF = E°(Cu²⁺/Cu) – E°(Zn²⁺/Zn)
= 0.34 – (–0.76) = 1.10 V
(b) कार्य = nFE
= 2 × 96500 × 1.10 = 212300 J = 212.3 kJ
उत्तर: EMF = 1.10 V, अधिकतम कार्य = 212.3 kJ
————————————————————————————————————————————————————————————————————————————
