Class 11 : Chemistry (In Hindi) – Lesson 7. अपचय अभिक्रियाएँ
पाठ का विश्लेषण एवं विवेचन
🎯 पाठ का उद्देश्य
🔸 विद्यार्थियों को अपचयन (Reduction) और ऑक्सीकरण (Oxidation) की परिभाषा, प्रकार और अभिक्रियाओं की पहचान करना सिखाना।
🔸 रेडॉक्स अभिक्रिया का विश्लेषण करना – जहाँ ऑक्सीकरण और अपचयन साथ-साथ होते हैं।
🔸 ऑक्सीकरण अवस्था (Oxidation Number) को ज्ञात करना और अर्ध अभिक्रिया विधि (Half-Reaction Method) द्वारा समीकरण संतुलित करना।
🔸 जीवन, पर्यावरण और तकनीक में रेडॉक्स अभिक्रियाओं की उपयोगिता को समझना।
🔍 मुख्य विषयवस्तु (Detailed Explanation – लगभग 1700 शब्दों में)
📌 1. अपचयन और ऑक्सीकरण की परिभाषाएं
🔹 ऑक्सीकरण (Oxidation): किसी तत्व द्वारा
✅ ऑक्सीजन ग्रहण करना
✅ हाइड्रोजन का त्याग करना
✅ इलेक्ट्रॉन का त्याग करना
✅ ऑक्सीकरण अवस्था में वृद्धि
🔹 अपचयन (Reduction):
✅ ऑक्सीजन का त्याग करना
✅ हाइड्रोजन ग्रहण करना
✅ इलेक्ट्रॉन ग्रहण करना
✅ ऑक्सीकरण अवस्था में कमी
🧪 उदाहरण:
CuO + H₂ → Cu + H₂O
➡️ CuO का अपचयन (Cu बनता है)
➡️ H₂ का ऑक्सीकरण (H₂O बनता है)
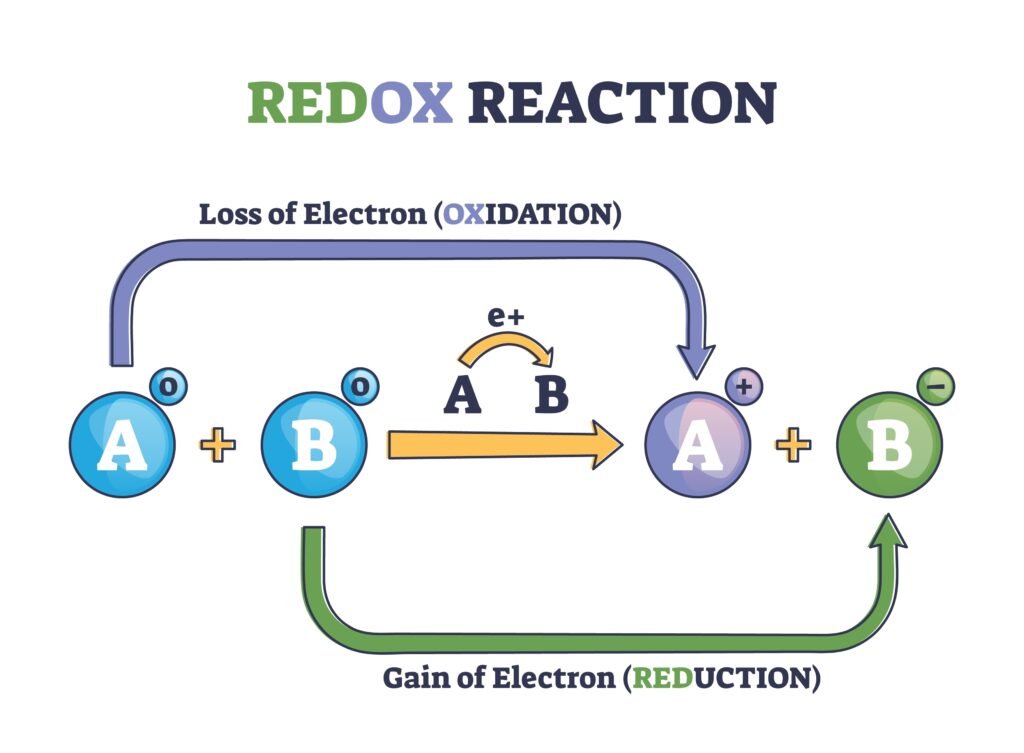
⚖️ 2. रेडॉक्स अभिक्रिया (Redox Reactions)
🔸 वे अभिक्रियाएं जिनमें एक ही समय पर किसी पदार्थ का ऑक्सीकरण और किसी अन्य का अपचयन होता है।
🔸 ये अभिक्रियाएं जोड़ (Coupled) होती हैं – एक के बिना दूसरा संभव नहीं।
🧪 उदाहरण:
Zn + Cu²⁺ → Zn²⁺ + Cu
➡️ Zn का ऑक्सीकरण, Cu²⁺ का अपचयन
🧠 3. ऑक्सीकरण अवस्था (Oxidation Number)
🟢 यह दर्शाती है कि किसी परमाणु पर आभासी आवेश कितना है यदि सभी बंध आयनिक माने जाएं।
🔹 कुछ सामान्य नियम:
✔️ मुक्त तत्वों की ऑक्सीकरण अवस्था = 0
✔️ H = +1 (अधिकतर), O = -2 (अधिकतर)
✔️ आयन की ऑक्सीकरण अवस्था = आयन का आवेश
✔️ यौगिक में सभी परमाणुओं के ऑक्सीकरण अवस्था का योग = 0
✔️ पॉलीएणिक आयन में ऑक्सीकरण अवस्था का योग = कुल आयनिक आवेश
🧪 उदाहरण:
KMnO₄ में Mn की ऑक्सीकरण अवस्था = +7
🔄 4. ऑक्सीकरण अवस्था ज्ञात करने के नियम
🧩 उदाहरण-१:
H₂SO₄ में S की ऑक्सीकरण अवस्था?
H = +1, O = -2
→ 2(+1) + S + 4(-2) = 0
→ S = +6 ✅
🧩 उदाहरण-२:
Cr₂O₇²⁻ में Cr की ऑक्सीकरण अवस्था?
→ 2x + 7(-2) = -2
→ x = +6
🔍 5. संतुलन की विधियाँ (Balancing Redox Equations)
📘 दो प्रमुख विधियाँ:
🟠 ऑक्सीकरण संख्या विधि (Oxidation Number Method)
🟢 अर्ध-अभिक्रिया विधि (Half Reaction Method)
💡 Half-Reaction Method के चरण:
1️⃣ अर्ध अभिक्रियाएं लिखें (ऑक्सीकरण और अपचयन अलग-अलग)
2️⃣ ऑक्सीकरण अवस्था के अनुसार इलेक्ट्रॉन जोड़ें
3️⃣ परमाणु और आवेश संतुलित करें
4️⃣ दोनों अर्ध-अभिक्रियाओं को जोड़ें
🧪 उदाहरण:
MnO₄⁻ + Fe²⁺ → Mn²⁺ + Fe³⁺ (Acidic medium)
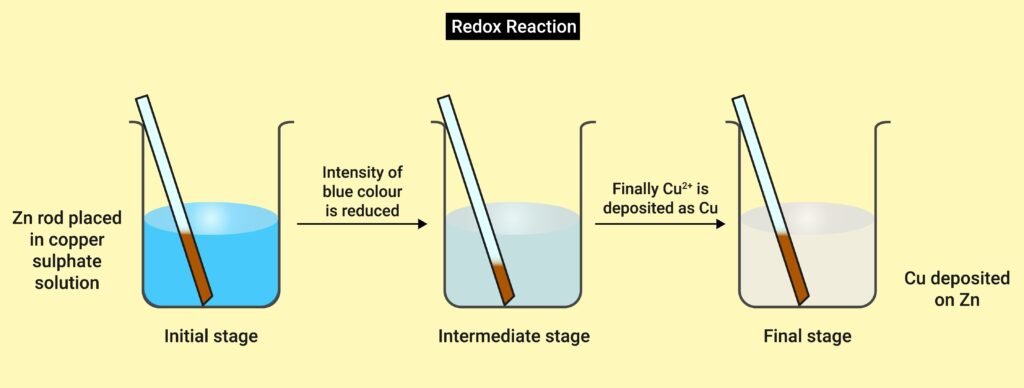
🔁 6. विस्थापन अभिक्रिया (Displacement Reactions)
🔸 एक तत्व किसी यौगिक से अन्य तत्व को विस्थापित कर देता है
🧪 Zn + CuSO₄ → ZnSO₄ + Cu
→ Zn का ऑक्सीकरण
→ Cu²⁺ का अपचयन
🧪 7. आंतरिक रेडॉक्स अभिक्रियाएं (Disproportionation Reactions)
🔹 एक ही पदार्थ में कुछ अणु ऑक्सीकरण और कुछ अपचयन करते हैं
🧪 2H₂O₂ → 2H₂O + O₂
→ O की ऑक्सीकरण अवस्था -1 से 0 और -2 दोनों में जा रही है
🌍 8. रेडॉक्स अभिक्रिया के अनुप्रयोग
🔹 कोशिका क्रियाएं (Cellular respiration)
🔹 फोटोसिंथेसिस
🔹 विद्युत अपघटन
🔹 गैल्वैनिक सेल
🔹 धातुओं का शुद्धिकरण
🔹 विस्फोटक अभिक्रियाएं
🔹 बैटरियों की क्रियाविधि
📝 सारांश
✅ अपचयन व ऑक्सीकरण रासायनिक अभिक्रियाओं के दो मूलभूत घटक हैं।
✅ ऑक्सीकरण में इलेक्ट्रॉन का त्याग और अपचयन में इलेक्ट्रॉन की प्राप्ति होती है।
✅ ऑक्सीकरण अवस्था परमाणु पर आभासी आवेश को दर्शाती है और किसी रासायनिक समीकरण में यह प्रमुख भूमिका निभाती है।
✅ रेडॉक्स अभिक्रिया वह होती है जिसमें एक साथ ऑक्सीकरण व अपचयन होते हैं।
✅ ऐसे समीकरणों को संतुलित करने हेतु ऑक्सीकरण संख्या विधि एवं अर्ध-अभिक्रिया विधि का प्रयोग किया जाता है।
✅ विस्थापन और आंतरिक रेडॉक्स अभिक्रियाएं इस श्रेणी के विशेष प्रकार हैं।
✅ रेडॉक्स अभिक्रियाएं जीवविज्ञान, इलेक्ट्रोरसायन, धातु निष्कर्षण, बैटरी तकनीक, उद्योग एवं पर्यावरण में अत्यंत महत्वपूर्ण हैं।
🔚 समाप्त
➡️ यह पाठ रसायन विज्ञान की नींव को मज़बूती देता है और आगामी विद्युत रसायन (Electrochemistry), तत्वों का निष्कर्षण (Metallurgy), और जैव रसायन (Biochemistry) के लिए मूल आधार बनाता है।
————————————————————————————————————————————————————————————————————————————
पाठ्यपुस्तक के प्रश्न
🔷 प्रश्न 7.1:
कोई दो दैनिक जीवन में घटित होने वाली ऑक्सीकरण-अपचयन अभिक्रियाओं के उदाहरण दीजिए।
🟢 उत्तर:
दैनिक जीवन में अपचय अभिक्रियाएँ सामान्यतः देखी जाती हैं।
📌 उदाहरण 1: लोहे का जंग लगना
Fe धातु वायुमंडल में नमी व ऑक्सीजन के संपर्क में आकर Fe²⁺ या Fe³⁺ में परिवर्तित हो जाता है। यह ऑक्सीकरण है।
📌 उदाहरण 2: शरीर में भोजन का चयापचयन
शरीर में ग्लूकोज़ का ऑक्सीकरण होता है जिससे ऊर्जा प्राप्त होती है – यह भी ऑक्सीकरण अभिक्रिया है।
🔷 प्रश्न 7.2:
निम्नलिखित अभिक्रिया में ऑक्सीकृत और अपचयित तत्वों की पहचान कीजिए:
Zn + HCl → ZnCl₂ + H₂
🟢 उत्तर:
Zn → Zn²⁺ ⇒ ऑक्सीकरण (ऑक्सीकरण संख्या बढ़ी)
H⁺ → H₂ ⇒ अपचयन (ऑक्सीकरण संख्या घटी)
अतः
📌 ऑक्सीकृत तत्व: Zn
📌 अपचयित तत्व: H⁺
🔷 प्रश्न 7.3:
ऑक्सीकरण संख्या में किस प्रकार का परिवर्तन ऑक्सीकरण और अपचयन को इंगित करता है?
🟢 उत्तर:
📌 जब किसी तत्व की ऑक्सीकरण संख्या बढ़ती है, तो वह ऑक्सीकृत होता है।
📌 जब किसी तत्व की ऑक्सीकरण संख्या घटती है, तो वह अपचयित होता है।
उदाहरण:
Fe²⁺ → Fe³⁺ (ऑक्सीकरण)
Cl₂ → Cl⁻ (अपचयन)
🔷 प्रश्न 7.4:
एक रेडॉक्स अभिक्रिया का उदाहरण दीजिए जिसमें एक ही तत्व का ऑक्सीकरण और अपचयन होता हो।
🟢 उत्तर:
📌 उदाहरण: Cl₂ + OH⁻ → Cl⁻ + ClO⁻ + H₂O
यहाँ Cl₂ का कुछ भाग Cl⁻ बनता है (अपचयन), जबकि कुछ भाग ClO⁻ में बदलता है (ऑक्सीकरण)।
इस प्रकार की अभिक्रियाओं को विसंयोजन (Disproportionation) कहा जाता है।
🔷 प्रश्न 7.5:
माना कि ऑक्सीकरण संख्या ज्ञात है, तो किस प्रकार यह ज्ञात किया जा सकता है कि कोई अभिक्रिया रेडॉक्स है या नहीं?
🟢 उत्तर:
यदि किसी अभिक्रिया में कम-से-कम दो तत्वों की ऑक्सीकरण संख्या क्रमशः बढ़ और घट रही हो, तो वह रेडॉक्स अभिक्रिया कहलाती है।
यदि सभी तत्वों की ऑक्सीकरण संख्याएँ अपरिवर्तित रहें, तो वह रेडॉक्स अभिक्रिया नहीं होगी।
🔷 प्रश्न 7.6:
किसी रासायनिक अभिक्रिया में ऑक्सीकृत और अपचयित तत्व की पहचान कैसे करें?
🟢 उत्तर:
📌 प्रत्येक तत्व की ऑक्सीकरण संख्या ज्ञात करें।
📌 जिसके लिए संख्या बढ़े – वह ऑक्सीकृत हुआ।
📌 जिसके लिए संख्या घटे – वह अपचयित हुआ।
उदाहरण:
Fe²⁺ → Fe³⁺ ⇒ ऑक्सीकरण
MnO₄⁻ → Mn²⁺ ⇒ अपचयन
🔷 प्रश्न 7.7:
उदाहरण सहित विसंयोजन अभिक्रिया को समझाइए।
🟢 उत्तर:
📌 विसंयोजन अभिक्रिया में एक ही तत्व का कुछ भाग ऑक्सीकृत होता है और कुछ भाग अपचयित।
📌 उदाहरण: Cl₂ + OH⁻ → Cl⁻ + ClO⁻ + H₂O
यहाँ Cl₂ का एक भाग Cl⁻ (अपचयन) और दूसरा भाग ClO⁻ (ऑक्सीकरण) में परिवर्तित होता है।
🔷 प्रश्न 7.8:
CuO + H₂ → Cu + H₂O में ऑक्सीकृत और अपचयित पदार्थों की पहचान कीजिए।
🟢 उत्तर:
CuO → Cu ⇒ अपचयन (Cu²⁺ → Cu)
H₂ → H₂O ⇒ ऑक्सीकरण (H⁰ → H⁺)
📌 ऑक्सीकृत: H₂
📌 अपचयित: CuO
🔷 प्रश्न 7.9:
Cu + 2AgNO₃ → Cu(NO₃)₂ + 2Ag में किस तत्व का ऑक्सीकरण एवं किसका अपचयन हुआ?
🟢 उत्तर:
Cu → Cu²⁺ ⇒ ऑक्सीकरण
Ag⁺ → Ag ⇒ अपचयन
📌 ऑक्सीकृत तत्व: Cu
📌 अपचयित तत्व: Ag⁺
🔷 प्रश्न 7.10:
हाइड्रोजन परॉक्साइड (H₂O₂) किस प्रकार की रेडॉक्स अभिक्रिया में भाग लेता है?
🟢 उत्तर:
H₂O₂ एक विसंयोजन क्रिया में भाग लेता है जिसमें:
H₂O₂ → H₂O + O₂
यहाँ O का एक भाग -1 से -2 में (ऑक्सीकरण) और एक भाग -1 से 0 में (अपचयन) जाता है।
अतः यह विसंयोजन अभिक्रिया है।
🔷 प्रश्न 7.11:
संतुलित रेडॉक्स अभिक्रिया प्राप्त कीजिए:
Fe²⁺ + Cr₂O₇²⁻ + H⁺ → Fe³⁺ + Cr³⁺ + H₂O
🟢 उत्तर:
स्टेप 1: अर्ध-अभिक्रियाएँ लिखें –
Fe²⁺ → Fe³⁺ (ऑक्सीकरण)
Cr₂O₇²⁻ → Cr³⁺ (अपचयन)
स्टेप 2: इलेक्ट्रॉनों की संख्या बराबर करें –
6Fe²⁺ → 6Fe³⁺ + 6e⁻
Cr₂O₇²⁻ + 14H⁺ + 6e⁻ → 2Cr³⁺ + 7H₂O
स्टेप 3: जोड़ें –
6Fe²⁺ + Cr₂O₇²⁻ + 14H⁺ → 6Fe³⁺ + 2Cr³⁺ + 7H₂O
🔷 प्रश्न 7.12:
अभिक्रिया KMnO₄ + HCl → KCl + MnCl₂ + Cl₂ + H₂O को संतुलित कीजिए।
🟢 उत्तर:
स्टेप 1: अर्ध-अभिक्रियाएँ –
MnO₄⁻ → Mn²⁺ (अपचयन)
Cl⁻ → Cl₂ (ऑक्सीकरण)
स्टेप 2: संतुलन कर –
2KMnO₄ + 16HCl → 2KCl + 2MnCl₂ + 5Cl₂ + 8H₂O
🔷 प्रश्न 7.13:
एक रेडॉक्स अभिक्रिया में कुल इलेक्ट्रॉनों का विनिमय क्या दर्शाता है?
🟢 उत्तर:
📌 यह दर्शाता है कि कितने इलेक्ट्रॉनों का एक तत्व ने त्याग किया और दूसरे ने ग्रहण किया।
📌 यह ऑक्सीकृत व अपचयित तत्वों के बीच संतुलन स्थापित करने में मदद करता है।
🔷 प्रश्न 7.14:
अम्लीय माध्यम में NO₃⁻ → NO को संतुलित कीजिए।
🟢 उत्तर:
स्टेप 1: N की ऑक्सीकरण संख्या में परिवर्तन:
NO₃⁻ (N = +5) → NO (N = +2)
स्टेप 2: अर्ध-अभिक्रिया:
NO₃⁻ + 4H⁺ + 3e⁻ → NO + 2H₂O
🔷 प्रश्न 7.15:
MnO₄⁻ को क्षारीय माध्यम में संतुलित कीजिए जब वह MnO₂ में परिवर्तित हो।
🟢 उत्तर:
स्टेप 1: MnO₄⁻ → MnO₂
Mn की ऑक्सीकरण संख्या: +7 → +4 (अपचयन)
अर्ध-अभिक्रिया:
MnO₄⁻ + 2H₂O + 3e⁻ → MnO₂ + 4OH⁻
🔷 प्रश्न 7.16:
Ni²⁺ आयन को क्षारीय माध्यम में Ni धातु में घटाने हेतु संतुलित अर्ध-अभिक्रिया लिखिए।
🟢 उत्तर:
अर्ध-अभिक्रिया: Ni²⁺ + 2e⁻ → Ni (ठोस)
(यह अपचयन अभिक्रिया है क्योंकि ऑक्सीकरण संख्या +2 से 0 हो रही है)
🔷 प्रश्न 7.17:
Cu²⁺ + Fe → Cu + Fe²⁺ को संतुलित कीजिए।
🟢 उत्तर:
Cu²⁺ + Fe → Cu + Fe²⁺
यह पहले से ही संतुलित है।
📌 Cu²⁺ + 2e⁻ → Cu (अपचयन)
📌 Fe → Fe²⁺ + 2e⁻ (ऑक्सीकरण)
🔷 प्रश्न 7.18:
Na₂S₂O₃ और I₂ के बीच क्रिया में Na₂S₄O₆ और NaI बनते हैं। इसे संतुलित कीजिए।
🟢 उत्तर:
2Na₂S₂O₃ + I₂ → Na₂S₄O₆ + 2NaI
📌 S₂O₃²⁻ → S₄O₆²⁻ (ऑक्सीकरण)
📌 I₂ → I⁻ (अपचयन)
🔷 प्रश्न 7.19:
Cr₂O₇²⁻ + I⁻ + H⁺ → Cr³⁺ + I₂ + H₂O को संतुलित कीजिए।
🟢 उत्तर:
Cr₂O₇²⁻ + 14H⁺ + 6I⁻ → 2Cr³⁺ + 3I₂ + 7H₂O
📌 Cr का अपचयन (+6 से +3)
📌 I⁻ का ऑक्सीकरण (–1 से 0)
🔷 प्रश्न 7.20:
Sn²⁺ + Fe³⁺ → Sn⁴⁺ + Fe²⁺ को संतुलित कीजिए।
🟢 उत्तर:
Sn²⁺ → Sn⁴⁺ + 2e⁻ (ऑक्सीकरण)
Fe³⁺ + e⁻ → Fe²⁺ (अपचयन)
संतुलन: 2Fe³⁺ + Sn²⁺ → 2Fe²⁺ + Sn⁴⁺
🔷 प्रश्न 7.21:
Zn + NO₃⁻ + H⁺ → Zn²⁺ + NH₄⁺ + H₂O को संतुलित कीजिए।
🟢 उत्तर:
अर्ध-अभिक्रियाएँ:
Zn → Zn²⁺ + 2e⁻ (ऑक्सीकरण)
NO₃⁻ + 10H⁺ + 8e⁻ → NH₄⁺ + 3H₂O (अपचयन)
पूरा संतुलन: 3Zn + 2NO₃⁻ + 16H⁺ → 3Zn²⁺ + 2NH₄⁺ + 5H₂O
🔷 प्रश्न 7.22:
C₂O₄²⁻ + MnO₄⁻ + H⁺ → CO₂ + Mn²⁺ + H₂O को संतुलित कीजिए।
🟢 उत्तर:
5C₂O₄²⁻ + 2MnO₄⁻ + 16H⁺ → 10CO₂ + 2Mn²⁺ + 8H₂O
📌 C₂O₄²⁻ का ऑक्सीकरण
📌 MnO₄⁻ का अपचयन
🔷 प्रश्न 7.23:
Cl₂ + OH⁻ → Cl⁻ + ClO⁻ + H₂O को संतुलित कीजिए।
🟢 उत्तर:
Cl₂ + 2OH⁻ → Cl⁻ + ClO⁻ + H₂O
📌 Cl का एक भाग ऑक्सीकरण और दूसरा भाग अपचयित होता है – यह विसंयोजन है।
🔷 प्रश्न 7.24:
NO₃⁻ + Zn → Zn²⁺ + NH₃ को संतुलित कीजिए।
🟢 उत्तर:
4Zn + NO₃⁻ + 10H⁺ → 4Zn²⁺ + NH₃ + 3H₂O
(संतुलन में NH₃ का निर्माण दर्शाता है कि N की ऑक्सीकरण संख्या +5 से –3 तक घटी)
🔷 प्रश्न 7.25:
MnO₄⁻ + H₂O₂ + H⁺ → Mn²⁺ + O₂ + H₂O को संतुलित कीजिए।
🟢 उत्तर:
2MnO₄⁻ + 5H₂O₂ + 6H⁺ → 2Mn²⁺ + 5O₂ + 8H₂O
📌 MnO₄⁻ का अपचयन
📌 H₂O₂ का ऑक्सीकरण
🔷 प्रश्न 7.26:
Na₂SO₃ + I₂ → Na₂SO₄ + NaI को संतुलित कीजिए।
🟢 उत्तर:
Na₂SO₃ + I₂ + H₂O → Na₂SO₄ + 2NaI + 2H⁺
📌 SO₃²⁻ → SO₄²⁻ (ऑक्सीकरण)
📌 I₂ → I⁻ (अपचयन)
🔷 प्रश्न 7.27:
Fe + HNO₃ → Fe(NO₃)₃ + NO को संतुलित कीजिए।
🟢 उत्तर:
3Fe + 8HNO₃ → 3Fe(NO₃)₃ + 2NO + 4H₂O
📌 Fe का ऑक्सीकरण
📌 NO₃⁻ का अपचयन
🔷 प्रश्न 7.28:
K₂Cr₂O₇ + SO₂ + H₂SO₄ → Cr₂(SO₄)₃ + K₂SO₄ + H₂O को संतुलित कीजिए।
🟢 उत्तर:
K₂Cr₂O₇ + 3SO₂ + 4H₂SO₄ → Cr₂(SO₄)₃ + K₂SO₄ + 3H₂O
📌 Cr का अपचयन (+6 → +3)
📌 SO₂ का ऑक्सीकरण (+4 → +6)
🔷 प्रश्न 7.29:
NO₃⁻ को क्षारीय माध्यम में NO₂⁻ में परिवर्तित करते हुए संतुलित कीजिए।
🟢 उत्तर:
NO₃⁻ + e⁻ → NO₂⁻
📌 यह अर्ध-अभिक्रिया क्षारीय माध्यम के लिए है (पूर्ण संतुलन माध्यम और अन्य आयनों पर निर्भर करता है)
🔷 प्रश्न 7.30:
H₂O₂ का ऑक्सीकरण भी हो सकता है और अपचयन भी – समझाइए।
🟢 उत्तर:
📌 H₂O₂ में ऑक्सीजन की ऑक्सीकरण संख्या –1 होती है।
📌 ऑक्सीकरण: H₂O₂ → O₂ (–1 → 0)
📌 अपचयन: H₂O₂ → H₂O (–1 → –2)
❖ इस प्रकार H₂O₂ दोहरी भूमिका निभाता है – ऑक्सीकृत और अपचयित दोनों होता है।
Question 7.31
अपरस और अपचायक एजेंट में क्या अंतर है?
उत्तर:
🔹 अपरस (Oxidation): वह प्रक्रिया जिसमें किसी तत्व की ऑक्सीकरण संख्या में वृद्धि होती है या इलेक्ट्रॉन त्यागे जाते हैं।
🔹 अपचायक अभिकर्ता (Reducing Agent): वह पदार्थ जो स्वयं ऑक्सीकरण होकर दूसरे पदार्थ का अपचयन करता है।
📌 भेद:
अपरस एक प्रक्रिया है जबकि अपचायक एजेंट एक पदार्थ है।
अपरस में इलेक्ट्रॉन खोना शामिल है, जबकि अपचायक एजेंट वह होता है जो इलेक्ट्रॉन प्रदान करता है।
Question 7.32
जस्ता धातु को तीव्रता से जलाने पर कौन-सा उत्पाद प्राप्त होता है? लिखिए:
(क) रासायनिक अभिक्रिया
(ख) ऑक्सीकरण अवस्था में परिवर्तन
उत्तर:
(क) रासायनिक अभिक्रिया:
Zn(s) + O₂(g) → 2ZnO(s)
(ख) ऑक्सीकरण अवस्था में परिवर्तन:
जस्ता की ऑक्सीकरण अवस्था 0 से +2 हो जाती है, जबकि ऑक्सीजन की 0 से –2।
Question 7.33
NO₃⁻ आयन को NH₃ में अपचयन किया गया है। इस अभिक्रिया में NO₃⁻ की ऑक्सीकरण अवस्था तथा NH₃ में नाइट्रोजन की ऑक्सीकरण अवस्था में परिवर्तन स्पष्ट कीजिए।
उत्तर:
🔹 NO₃⁻ में नाइट्रोजन की ऑक्सीकरण अवस्था = +5
🔹 NH₃ में नाइट्रोजन की ऑक्सीकरण अवस्था = –3
📌 परिवर्तन = +5 से –3 ⇒ कुल परिवर्तन = 8 की कमी
⇒ इसका अर्थ है NO₃⁻ का अपचयन हुआ है क्योंकि ऑक्सीकरण संख्या में कमी हुई।
————————————————————————————————————————————————————————————————————————————
अन्य महत्वपूर्ण प्रश्न
(CBSE MODEL प्रश्न पत्र)
सिर्फ इसी पाठ से निर्मित CBSE MODEL प्रश्न पत्र।
Section A: प्रश्न 1 से 18 (प्रत्येक 1 अंक)
Q1. निम्नलिखित में से कौन-सा युग्म एक रेडॉक्स अभिक्रिया का उदाहरण है?
(A) NaOH + HCl → NaCl + H₂O
(B) AgNO₃ + NaCl → AgCl + NaNO₃
(C) Zn + CuSO₄ → ZnSO₄ + Cu
(D) BaCl₂ + H₂SO₄ → BaSO₄ + 2HCl
उत्तर: (C)
स्पष्टीकरण: Zn ऑक्सीकरण करता है और Cu²⁺ आयन अपचयनित होता है।
Q2. एक रेडॉक्स अभिक्रिया में इलेक्ट्रॉनों का स्थानांतरण होता है:
(A) केवल धातुओं के बीच
(B) केवल अधातुओं के बीच
(C) ऑक्सीकरण और अपचयन के बीच
(D) किसी भी युग्म के बीच
उत्तर: (C)
Q3. Fe²⁺ → Fe³⁺ परिवर्तन किस प्रकार की प्रक्रिया है?
(A) अपचयन
(B) अपरस
(C) युग्मन
(D) उदासीनीकरण
उत्तर: (B)
Q4. निम्नलिखित में से कौन-सा यौगिक अपचायक के रूप में कार्य करता है?
(A) H₂O₂
(B) KMnO₄
(C) O₃
(D) SO₂
उत्तर: (D)
Q5. किसी तत्व की ऑक्सीकरण अवस्था को दर्शाया जाता है:
(A) आयन भार से
(B) परमाणु संख्या से
(C) परमाणु भार से
(D) ऑर्बिटल संकल्पना से
उत्तर: (A)
Q6. निम्नलिखित में से कौन-सा युग्म सही मेल नहीं है?
(A) अपरस → इलेक्ट्रॉनों की हानि
(B) अपचयन → इलेक्ट्रॉनों की प्राप्ति
(C) अपचायक → इलेक्ट्रॉन लेनेवाला
(D) उपचायक → इलेक्ट्रॉन देनेवाला
उत्तर: (C)
Q7. Zn → Zn²⁺ + 2e⁻ अभिक्रिया का प्रकार है:
(A) अपरस
(B) अपचयन
(C) संतुलन
(D) युग्मन
उत्तर: (A)
Q8. एक रेडॉक्स अभिक्रिया में, अपचायक पदार्थ क्या करता है?
(A) इलेक्ट्रॉन प्राप्त करता है
(B) ऑक्सीजन ग्रहण करता है
(C) इलेक्ट्रॉन देता है
(D) इलेक्ट्रॉन की आवश्यकता नहीं होती
उत्तर: (C)
Q9. निम्न में से कौन-सा पदार्थ अपचयन नहीं करता है?
(A) Zn
(B) Fe
(C) Cl₂
(D) Na
उत्तर: (C)
Q10. ऑक्सीकरण संख्या की गणना में H की मान्यता होती है:
(A) +2
(B) –1
(C) +1
(D) 0
उत्तर: (C)
Q11. निम्नलिखित में से कौन-सा युग्म “ऑक्सीकरण अवस्था में वृद्धि” को दर्शाता है?
(A) Fe²⁺ → Fe³⁺
(B) Mn⁴⁺ → Mn²⁺
(C) Cl₂ → Cl⁻
(D) Cu²⁺ → Cu
उत्तर: (A)
Q12. निम्नलिखित में से कौन सा एक युग्म रेडॉक्स अभिक्रिया नहीं है?
(A) Cu + AgNO₃ → Cu(NO₃)₂ + Ag
(B) Na + Cl₂ → NaCl
(C) HCl + NaOH → NaCl + H₂O
(D) Zn + H₂SO₄ → ZnSO₄ + H₂
उत्तर: (C)
Q13. ऑक्सीकरण अवस्था में वृद्धि दर्शाती है:
(A) अपरस
(B) अपचयन
(C) अम्लीयता
(D) क्षारीयता
उत्तर: (A)
Q14. H₂S + Cl₂ → 2HCl + S में कौन अपचायक है?
(A) H₂S
(B) Cl₂
(C) HCl
(D) S
उत्तर: (A)
Q15. निम्नलिखित में से कौन-सा ऑक्सीकरण संख्या को घटाता है?
(A) अपरस
(B) अपचयन
(C) जल अपघटन
(D) ऑक्सीकरण
उत्तर: (B)
Q16. निम्नलिखित में से किस युग्म में दोनों प्रक्रियाएँ एक साथ होती हैं?
(A) अपरस
(B) अपचयन
(C) रेडॉक्स
(D) निष्क्रियता
उत्तर: (C)
Q17. कौन-सा तत्व रेडॉक्स अभिक्रिया में उपचायक की भाँति कार्य नहीं कर सकता?
(A) Fe
(B) Cu
(C) Au
(D) Zn
उत्तर: (C)
Q18. “Fe³⁺ + e⁻ → Fe²⁺” में क्या हो रहा है?
(A) इलेक्ट्रॉन की हानि
(B) अपरस
(C) ऑक्सीकरण अवस्था में वृद्धि
(D) अपचयन
उत्तर: (D)
Section B: प्रश्न 19 से 23 (प्रत्येक 2 अंक)
Q19. H₂O₂ को अपचायक और उपचायक दोनों के रूप में कार्य करते हुए एक-एक उदाहरण सहित स्पष्ट कीजिए।
उत्तर:
📌 अपचायक के रूप में:
2KI + H₂O₂ → 2KOH + I₂
यहाँ H₂O₂ स्वयं ऑक्सीजन देता है, अतः यह अपचायक है।
📌 उपचायक के रूप में:
H₂S + H₂O₂ → S + 2H₂O
यहाँ H₂O₂ ने H₂S को ऑक्सीकरण किया, स्वयं अपचयित हुआ, अतः उपचायक है।
Q20. किसी रेडॉक्स अभिक्रिया में इलेक्ट्रॉनों का स्थानांतरण क्यों आवश्यक होता है?
उत्तर:
रेडॉक्स अभिक्रिया में एक तत्व इलेक्ट्रॉन खोता है (अपरस) तथा दूसरा इलेक्ट्रॉन प्राप्त करता है (अपचयन)। इस इलेक्ट्रॉन स्थानांतरण के बिना किसी का ऑक्सीकरण या अपचयन संभव नहीं होता। अतः यह आवश्यक है।
Q21. निम्न अभिक्रिया में किस पदार्थ की ऑक्सीकरण संख्या सबसे अधिक बदली है?
MnO₄⁻ + C₂O₄²⁻ → Mn²⁺ + CO₂
उत्तर:
📌 Mn की ऑक्सीकरण संख्या: +7 से +2 → परिवर्तन = 5
📌 C की ऑक्सीकरण संख्या: +3 से +4 → परिवर्तन = 1 (प्रति C)
2 C परमाणु ⇒ कुल परिवर्तन = 2
⇒ Mn में परिवर्तन अधिक है: +5 की वृद्धि
Q22. KMnO₄ को अम्लीय माध्यम में अपचायक के साथ प्रयोग करने पर Mn²⁺ बनता है। इसका संतुलित अणुगणात्मक समीकरण लिखिए।
उत्तर:
2KMnO₄ + 5H₂C₂O₄ + 6H₂SO₄ → 2MnSO₄ + 10CO₂ + K₂SO₄ + 8H₂O
Q23. CH₄ + 2O₂ → CO₂ + 2H₂O अभिक्रिया में ऑक्सीकरण और अपचयन प्रक्रिया की पहचान कीजिए।
उत्तर:
📌 CH₄ में C की ऑक्सीकरण संख्या –4 है, CO₂ में +4 हो जाती है ⇒ अपरस
📌 O₂ की ऑक्सीकरण संख्या 0 से –2 हो जाती है ⇒ अपचयन
⇒ यह एक रेडॉक्स अभिक्रिया है।
Section C: प्रश्न 24 से 28 (प्रत्येक 3 अंक)
Q24. निम्नलिखित अभिक्रिया को आयन-आधारित (आयनिक) समीकरण के रूप में संतुलित कीजिए:
Fe²⁺ + Cr₂O₇²⁻ + H⁺ → Fe³⁺ + Cr³⁺ + H₂O
उत्तर:
संतुलित समीकरण:
6Fe²⁺ + Cr₂O₇²⁻ + 14H⁺ → 6Fe³⁺ + 2Cr³⁺ + 7H₂O
📌 Fe²⁺ → Fe³⁺ : इलेक्ट्रॉन खोता है (अपरस)
📌 Cr₂O₇²⁻ → Cr³⁺ : इलेक्ट्रॉन प्राप्त करता है (अपचयन)
Q25. निम्नलिखित के लिए ऑक्सीकरण संख्या का निर्धारण कीजिए:
(a) MnO₄⁻
(b) Cr₂O₇²⁻
(c) H₂O₂
उत्तर:
(a) MnO₄⁻ : O = –2 ⇒ Mn = +7
(b) Cr₂O₇²⁻ : O = –2 ⇒ Cr = +6
(c) H₂O₂ : O = –1 (विशेष स्थिति)
Q26. निम्नलिखित अभिक्रिया में संतुलन स्थापित कीजिए और यह दर्शाइए कि कौन अपरस और कौन अपचायक है:
Cl₂ + SO₂ + 2H₂O → H₂SO₄ + 2HCl
उत्तर:
संतुलित समीकरण:
Cl₂ + SO₂ + 2H₂O → H₂SO₄ + 2HCl
📌 SO₂ → H₂SO₄ : ऑक्सीकरण संख्या +4 → +6 ⇒ अपरस
📌 Cl₂ → HCl : ऑक्सीकरण संख्या 0 → –1 ⇒ अपचयन
⇒ SO₂ उपचायक, Cl₂ अपचायक
Q27. यह सिद्ध कीजिए कि Zn + Cu²⁺ → Zn²⁺ + Cu एक रेडॉक्स अभिक्रिया है।
उत्तर:
📌 Zn → Zn²⁺ : इलेक्ट्रॉन की हानि ⇒ अपरस
📌 Cu²⁺ → Cu : इलेक्ट्रॉन की प्राप्ति ⇒ अपचयन
⇒ एक तत्व इलेक्ट्रॉन देता है, दूसरा लेता है ⇒ यह एक रेडॉक्स अभिक्रिया है।
Q28. निम्नलिखित अभिक्रिया में ऑक्सीकरण और अपचयन प्रक्रिया की पहचान कीजिए:
2H₂ + O₂ → 2H₂O
उत्तर:
📌 H₂ → H₂O : H की ऑक्सीकरण संख्या 0 → +1 ⇒ अपरस
📌 O₂ → H₂O : O की ऑक्सीकरण संख्या 0 → –2 ⇒ अपचयन
⇒ यह एक रेडॉक्स अभिक्रिया है।
Section D: प्रश्न 29 से 31 (प्रत्येक 4 अंक, केस-आधारित)
Q29. नीचे दी गई जानकारी के आधार पर प्रश्नों के उत्तर दीजिए:
एक छात्र ने अम्लीय माध्यम में KMnO₄ और FeSO₄ की अभिक्रिया कराई।
(i) अभिक्रिया का प्रकार क्या है?
(ii) इसमें कौन अपचायक और कौन उपचायक है?
(iii) Mn की ऑक्सीकरण संख्या कितनी बदलती है?
(iv) संतुलित समीकरण लिखिए।
उत्तर:
(i) यह एक रेडॉक्स अभिक्रिया है।
(ii) KMnO₄ अपचायक है, FeSO₄ उपचायक है।
(iii) Mn : +7 → +2 ⇒ परिवर्तन = 5
(iv) संतुलित समीकरण:
2KMnO₄ + 10FeSO₄ + 8H₂SO₄ → K₂SO₄ + 2MnSO₄ + 5Fe₂(SO₄)₃ + 8H₂O
Q30. दी गई अभिक्रिया का विश्लेषण करें:
Cl₂ + 2NaOH → NaCl + NaOCl + H₂O
उत्तर दीजिए:
(i) कौन-सा तत्व अपरस और कौन अपचयित हो रहा है?
(ii) NaOCl में Cl की ऑक्सीकरण संख्या क्या है?
(iii) क्या यह एक अनुप्रस्थ रेडॉक्स अभिक्रिया है?
(iv) ऐसे अभिक्रियाओं के एक अनुप्रयोग का उल्लेख कीजिए।
उत्तर:
(i) Cl₂ का एक अणु NaCl में → –1 ⇒ अपचयन
दूसरा Cl NaOCl में → +1 ⇒ अपरस
(ii) NaOCl में Cl की ऑक्सीकरण संख्या = +1
(iii) हाँ, यह अनुप्रस्थ रेडॉक्स अभिक्रिया (Disproportionation Reaction) है।
(iv) NaOCl का प्रयोग ब्लीचिंग एजेंट के रूप में होता है।
Q31. नीचे दी गई स्थिति के आधार पर प्रश्नों के उत्तर दें:
Fe²⁺ + H₂O₂ + H⁺ → Fe³⁺ + H₂O
(i) H₂O₂ किस रूप में कार्य कर रहा है?
(ii) Fe की ऑक्सीकरण संख्या में कितना परिवर्तन हुआ?
(iii) क्या यह रेडॉक्स अभिक्रिया है?
(iv) इसका अनुप्रयोग कहाँ होता है?
उत्तर:
(i) H₂O₂ उपचायक के रूप में कार्य कर रहा है।
(ii) Fe: +2 → +3 ⇒ परिवर्तन = +1
(iii) हाँ, एक घटक इलेक्ट्रॉन खो रहा है, दूसरा पा रहा है ⇒ रेडॉक्स अभिक्रिया
(iv) इस प्रकार की अभिक्रिया रक्त के विश्लेषण (ब्लड टेस्ट) में उपयोगी होती है।
Section E: प्रश्न 32 से 35 (प्रत्येक 5 अंक, दीर्घ उत्तर)
Q32. रेडॉक्स अभिक्रिया को आधे अभिक्रियाओं में विभाजित करने की विधि को समझाइए। निम्नलिखित अभिक्रिया को इस पद्धति से संतुलित कीजिए:
Cr₂O₇²⁻ + Fe²⁺ + H⁺ → Cr³⁺ + Fe³⁺ + H₂O
उत्तर:
📌 Step 1: ऑक्सीकरण एवं अपचयन आधी अभिक्रियाएँ:
Fe²⁺ → Fe³⁺ + e⁻
Cr₂O₇²⁻ + 14H⁺ + 6e⁻ → 2Cr³⁺ + 7H₂O
📌 Step 2: इलेक्ट्रॉन संख्या बराबर करना:
Fe²⁺ से कुल 6e⁻ चाहिए ⇒ 6Fe²⁺
📌 Final balanced equation:
Cr₂O₇²⁻ + 6Fe²⁺ + 14H⁺ → 2Cr³⁺ + 6Fe³⁺ + 7H₂O
📌 यह आयनिक रेडॉक्स अभिक्रिया है जिसमें Fe अपचयित और Cr अपरस होता है।
Q33. अनुप्रस्थ रेडॉक्स अभिक्रिया क्या होती है? उदाहरण सहित समझाइए। ऐसी दो और अभिक्रियाएँ लिखिए।
उत्तर:
📌 अनुप्रस्थ रेडॉक्स अभिक्रिया वह होती है जिसमें एक ही तत्व की ऑक्सीकरण संख्या बढ़ती और घटती है।
📌 उदाहरण:
Cl₂ + 2NaOH → NaCl + NaOCl + H₂O
यहाँ Cl एक भाग में –1 (अपचयन), दूसरे में +1 (अपरस) ⇒ अनुप्रस्थ अभिक्रिया
📌 अन्य उदाहरण:
(1) 3Cl₂ + 6KOH → 5KCl + KClO₃ + 3H₂O
(2) P₄ + 4OH⁻ + 4H₂O → 2H₂PO₂⁻ + 2PH₃
Q34. निम्नलिखित अभिक्रिया में ऑक्सीकरण संख्या पद्धति से समीकरण को संतुलित कीजिए:
MnO₄⁻ + C₂O₄²⁻ + H⁺ → Mn²⁺ + CO₂
उत्तर:
📌 Step 1: Mn की ऑक्सीकरण संख्या:
MnO₄⁻ में Mn = +7, Mn²⁺ में = +2 ⇒ परिवर्तन = 5
📌 C की ऑक्सीकरण संख्या:
C₂O₄²⁻ में = +3, CO₂ में = +4 ⇒ परिवर्तन = 1 प्रति C ⇒ 2 कुल ⇒ 2e⁻
📌 LCM = 10 ⇒ गुणक:
MnO₄⁻ × 2, C₂O₄²⁻ × 5
📌 Final balanced equation:
2MnO₄⁻ + 5C₂O₄²⁻ + 16H⁺ → 2Mn²⁺ + 10CO₂ + 8H₂O
📌 यह एक आयन-आधारित रेडॉक्स अभिक्रिया है।
Q35. H₂O₂ एक द्वैत स्वभाव (Dual Nature) रखने वाला यौगिक है। समझाइए और दो-दो उदाहरण दीजिए।
उत्तर:
📌 H₂O₂ एक द्वैतीय अभिकर्मक है अर्थात यह अपचायक और उपचायक दोनों के रूप में कार्य करता है।
🔹 अपचायक के रूप में:
2KI + H₂O₂ → 2KOH + I₂
🔹 उपचायक के रूप में:
H₂S + H₂O₂ → S + 2H₂O
📌 यह उसकी ऑक्सीजन की ऑक्सीकरण संख्या (–1) के कारण है, जो बदलकर +1 या –2 हो सकती है।
📌 इसका उपयोग ब्लीचिंग, कीटाणु नाशक और प्रयोगशालाओं में किया जाता है।
————————————————————————————————————————————————————————————————————————————
