Class 11 : Chemistry (In Hindi) – Lesson 6. साम्यावस्था
पाठ का विश्लेषण एवं विवेचन
🔵 भूमिका ✨
रसायन विज्ञान में अनेक अभिक्रियाएँ एक दिशा में पूर्ण नहीं होतीं, बल्कि कुछ समय बाद वे संतुलित दशा (साम्यावस्था) प्राप्त कर लेती हैं। इस दशा में आगे और पीछे दोनों अभिक्रियाएँ समान दर से चलती हैं, अतः अभिकारकों और उत्पादों की सान्द्रता स्थिर बनी रहती है। साम्यावस्था का अध्ययन यह समझने के लिए महत्त्वपूर्ण है कि अभिक्रियाएँ किस सीमा तक आगे बढ़ेंगी तथा किन परिस्थितियों में उत्पादों या अभिकारकों का प्रभुत्व रहेगा।
🟢 साम्यावस्था की मूल अवधारणा 📌
प्रतिवर्ती अभिक्रिया: वह अभिक्रिया जो आगे और पीछे दोनों दिशाओं में हो सकती है।
➤ A ⇌ B
यदि प्रारम्भ में केवल A लिया जाए तो कुछ समय बाद B बनने लगेगा, और फिर B से A भी बनने लगेगा। अंततः एक संतुलित अवस्था प्राप्त होगी।
साम्यावस्था की विशेषताएँ:
यह गतिक (dynamic) अवस्था है — आगे व पीछे की दर समान।
साम्य पर अभिकारक और उत्पाद दोनों विद्यमान रहते हैं।
बाहरी परिस्थितियाँ (ताप, दाब, सान्द्रता) साम्य की स्थिति को प्रभावित कर सकती हैं।
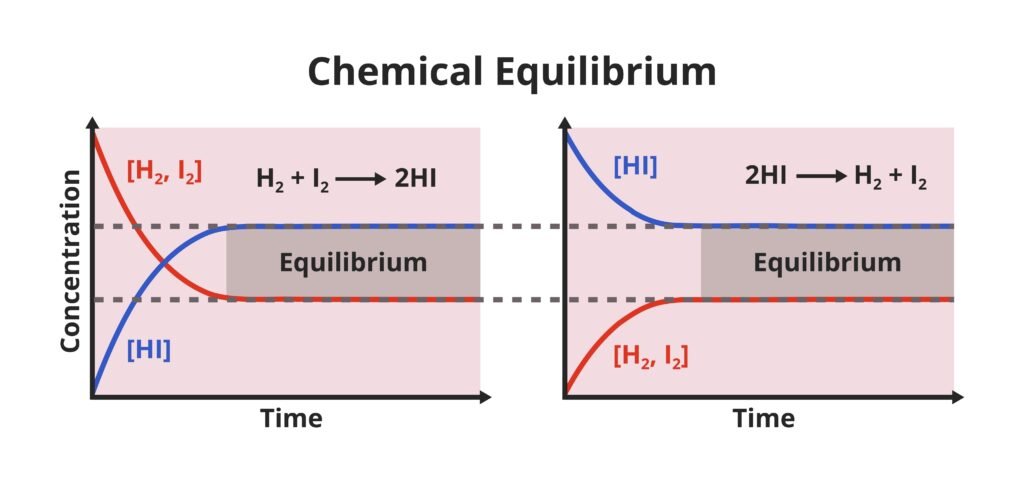

🟡 भौतिक एवं रासायनिक साम्य 📘
भौतिक साम्य: जैसे जल ⇌ वाष्प, बर्फ ⇌ जल।
रासायनिक साम्य: जैसे N₂(g) + 3H₂(g) ⇌ 2NH₃(g)
🔴 साम्य नियतांक (Equilibrium Constant) 🌟
मान लें सामान्य अभिक्रिया:
aA + bB ⇌ cC + dD
तो साम्य नियतांक (सांद्रता रूप) होगा:
Kc = [C]^c [D]^d / [A]^a [B]^b
जहाँ [] से आशय साम्य पर सांद्रता है।
यदि सभी पदार्थ गैसीय हों तो दाब रूप में लिखा जाता है:
Kp = (PC)^c (PD)^d / (PA)^a (PB)^b
🟢 Kc और Kp का सम्बन्ध ✨
Kp = Kc (RT)^Δn
जहाँ Δn = (गैसीय उत्पादों के मोल – गैसीय अभिकारकों के मोल)।
✔ यदि Δn = 0 हो तो Kp = Kc।
🟡 साम्य नियतांक की विशेषताएँ 📌
यह केवल तापमान पर निर्भर करता है।
दाब, उत्प्रेरक या प्रारम्भिक सांद्रता का सीधा प्रभाव नहीं।
K का बड़ा मान → उत्पादों का प्रभुत्व।
K का छोटा मान → अभिकारकों का प्रभुत्व।
🔴 अभिक्रिया भाजक (Reaction Quotient, Q) 💡
Q = [C]^c [D]^d / [A]^a [B]^b (किसी भी क्षण पर)
यदि Q < K → अभिक्रिया आगे की ओर बढ़ेगी।
यदि Q > K → अभिक्रिया पीछे की ओर।
यदि Q = K → साम्य प्राप्त।
🟢 ले-शातेलिए का सिद्धान्त (Le Chatelier’s Principle) 📚
यदि साम्यावस्था पर कोई बाहरी प्रभाव डाला जाए तो तंत्र इस प्रकार प्रतिक्रिया करेगा कि प्रभाव को कम करने का प्रयास हो।
सान्द्रता परिवर्तन:
अभिकारक बढ़ाने पर → आगे की ओर।
उत्पाद बढ़ाने पर → पीछे की ओर।
दाब परिवर्तन (गैसीय अभिक्रियाओं में):
दाब बढ़ाने पर → उस दिशा में जहाँ मोल संख्या कम।
दाब घटाने पर → उस दिशा में जहाँ मोल संख्या अधिक।
तापमान परिवर्तन:
उष्माक्षेपी (ΔH < 0) → ताप बढ़ाने पर पीछे, घटाने पर आगे।
उष्माशोषी (ΔH > 0) → ताप बढ़ाने पर आगे, घटाने पर पीछे।
उत्प्रेरक:
केवल साम्य तक पहुँचने की गति बढ़ाता है, स्थिति को नहीं बदलता।
🟡 आयनिक साम्य (Ionic Equilibrium) 🌟
कमजोर इलेक्ट्रोलाइट का अपघटन:
HA ⇌ H⁺ + A⁻
आयनीकरण स्थिरांक: Ka = [H⁺][A⁻] / [HA]
pH और pOH:
pH = −log[H⁺]
pOH = −log[OH⁻]
pH + pOH = 14 (25 °C पर)
जल का आयनिक गुणनफल:
Kw = [H⁺][OH⁻] = 1 × 10⁻¹⁴ (25 °C पर)
बफर विलयन:
कमजोर अम्ल + उसका लवण या कमजोर क्षार + उसका लवण।
pH लगभग स्थिर बनाए रखता है।
सामान्य आयन प्रभाव:
यदि किसी विलयन में सामान्य आयन उपस्थित हो तो आयनीकरण दब जाता है।
🟢 घुलनशीलता गुणनफल (Solubility Product, Ksp) 📌
संतृप्त विलयन में आयनों की सांद्रताओं का गुणनफल।
यदि आयनिक गुणनफल (Qsp) < Ksp → विलयन असंतृप्त।
Qsp = Ksp → संतृप्त।
Qsp > Ksp → लवण का अवक्षेप बनेगा।
🔴 व्यावहारिक उपयोग 💡
औद्योगिक प्रक्रियाएँ (अमोनिया संश्लेषण, H₂SO₄ निर्माण)।
जल-उपचार, औषधि निर्माण।
विश्लेषणात्मक रसायन विज्ञान (अवक्षेपण, विलयन विश्लेषण)।
🔹 II. पाठ सार
🔵 सार-तत्त्व ✨
प्रतिवर्ती अभिक्रियाएँ साम्यावस्था प्राप्त करती हैं।
साम्य गतिक अवस्था है जिसमें आगे और पीछे की दर समान।
साम्य नियतांक (Kc, Kp) साम्य की स्थिति बताता है; यह केवल तापमान पर निर्भर करता है।
Q और K की तुलना से अभिक्रिया की दिशा ज्ञात होती है।
ले-शातेलिए का सिद्धान्त: बाहरी परिवर्तन का तंत्र इस प्रकार प्रतिकार करता है कि परिवर्तन का प्रभाव कम हो।
आयनिक साम्य में pH, pOH, Kw, Ka, Kb का उपयोग होता है।
बफर विलयन pH को स्थिर रखता है।
सामान्य आयन प्रभाव आयनीकरण को दबाता है।
घुलनशीलता गुणनफल (Ksp) अवक्षेप बनने की भविष्यवाणी करता है।
🟢 निष्कर्ष 📌
साम्यावस्था का अध्ययन हमें यह समझने में मदद करता है कि अभिक्रियाएँ किस सीमा तक आगे बढ़ेंगी, किन परिस्थितियों में उत्पाद या अभिकारक प्रधान होंगे, और औद्योगिक प्रक्रियाओं तथा विश्लेषणात्मक प्रयोगों में इसे कैसे उपयोग किया जा सकता है।
🔹 III. त्वरित पुनरावृत्ति
🔵 मुख्य बिन्दु 🌟
साम्य गतिक अवस्था है।
Kc, Kp साम्य की स्थिति बताते हैं।
Q और K से अभिक्रिया की दिशा तय होती है।
ले-शातेलिए सिद्धान्त: बाहरी परिवर्तन के प्रतिकार हेतु तंत्र की प्रतिक्रिया।
pH = −log[H⁺], Kw = 1 × 10⁻¹⁴ (25 °C)।
सामान्य आयन प्रभाव आयनीकरण घटाता है।
Ksp से अवक्षेप की भविष्यवाणी की जाती है।
————————————————————————————————————————————————————————————————————————————
पाठ्यपुस्त के प्रश्न
🔵 प्रश्न 6.1:
एक त्रय को सीलबंद पात्र में नियत ताप पर इसके वाष्प के साथ साम्य में रखा जाता है। पात्र का प्रारम्भिक आयतन और ताप नियत रखा गया है।
(क) वाष्प-दाब परिवर्तन का प्रारम्भिक परिणाम क्या होगा?
(ख) ताप में बढ़ोतरी एवं संकुचन की दर पर कैसे असर डालेगी?
(ग) यदि पात्र को बड़ा किया जाए, तो किस दिशा में परिवर्तन होगा?
🟢 उत्तर:
(क) प्रारंभ में यदि वाष्पीकरण होता है, तो वाष्प-दाब बढ़ेगा और साम्य स्थापित होगा।
(ख) ताप बढ़ाने से वाष्पीकरण बढ़ेगा, इसलिए वाष्प-दाब भी बढ़ेगा।
(ग) पात्र का आयतन बढ़ाने पर दाब घटेगा, इसलिए प्रणाली वाष्पीकरण की ओर झुकेगी ताकि अधिक गैस बने और दाब पुनः बढ़े।
🔵 प्रश्न 6.2:
साम्य: 2SO2(g) + O2(g) ⇌ 2SO3(g)
यदि प्रारंभिक सांद्रताएँ [SO2] = 0.60 M और [SO3] = 1.90 M हैं तथा Kc = 1000 है, तो [O2] का मान ज्ञात कीजिए।
🟢 उत्तर:
Kc = [SO3]^2 / ([SO2]^2 * [O2])
1000 = (1.90)^2 / ((0.60)^2 * [O2])
[O2] = (1.90)^2 / (1000 * 0.36)
= 3.61 / 360
= 0.010 M
✔ अतः [O2] = 0.010 M
🔵 प्रश्न 6.3:
I2(g) ⇌ 2I(g) का साम्य 105 Pa पर है। आयोडीन वाष्प में 40% आयोडीन परमाणु होते हैं। Kp का मान ज्ञात कीजिए।
🟢 उत्तर:
कुल दाब = 105 Pa
40% आयोडीन परमाणु ⇒ 0.4 भाग I, 0.6 भाग I2
मोल अंश:
n(I2) = 0.6, n(I) = 0.8 (क्योंकि I2 का 40% विघटन)
कुल मोल = 0.6 + 0.8 = 1.4
मोल अंश I2 = 0.6/1.4 = 0.4286
मोल अंश I = 0.8/1.4 = 0.5714
आंशिक दाब:
PI2 = 105 × 0.4286 = 45.0 Pa
PI = 105 × 0.5714 = 60.0 Pa
Kp = (PI)^2 / PI2 = (60)^2 / 45 = 3600 / 45 = 80 Pa
✔ Kp = 80 Pa
🔵 प्रश्न 6.4:
निम्नलिखित अभिक्रियाओं के लिए साम्य स्थिरांक Kc का व्यंजक लिखिए —
(i) 2NOCl(g) ⇌ 2NO(g) + Cl2(g)
(ii) 2Cu(NO3)2(s) ⇌ 2CuO(s) + 4NO2(g) + O2(g)
(iii) CH3COOC2H5(aq) + H2O(l) ⇌ CH3COOH(aq) + C2H5OH(aq)
(iv) Fe3+(aq) + 3OH-(aq) ⇌ Fe(OH)3(s)
🟢 उत्तर:
(i) Kc = [NO]^2 * [Cl2] / [NOCl]^2
(ii) Kc = [NO2]^4 * [O2] (ठोस पदार्थ नहीं लिए जाते)
(iii) Kc = [CH3COOH] * [C2H5OH] / [CH3COOC2H5]
(iv) Kc = 1 / ([Fe3+] * [OH-]^3)
🔵 प्रश्न 6.5:
Kp के मान से Kc ज्ञात कीजिए —
(i) 2NOCl(g) ⇌ 2NO(g) + Cl2(g), Kp = 1.8 × 10^-2 at 500 K
(ii) CaCO3(s) ⇌ CaO(s) + CO2(g), Kp = 167 at 1073 K
🟢 उत्तर:
(i) Δn = (2 + 1) – 2 = 1
Kp = Kc(RT)^Δn
Kc = Kp / (RT)
R = 0.0821, T = 500
Kc = 1.8 × 10^-2 / (0.0821 × 500)
= 1.8 × 10^-2 / 41.05 = 4.38 × 10^-4
(ii) Δn = 1 – 0 = 1
Kp = Kc(RT)
Kc = Kp / (RT)
= 167 / (0.0821 × 1073) = 167 / 88.2 = 1.89
✔ Kc(1) = 4.38 × 10^-4
✔ Kc(2) = 1.89
🔵 प्रश्न 6.6:
साम्य: NO(g) + O3(g) ⇌ NO2(g) + O2(g)
Kc = 6.3 × 10^14 at 1000 K
यदि प्रारंभ में NO और O3 बराबर मात्रा में हों, तो साम्य पर कौन-सा अभिकारक अधिक रहेगा?
🟢 उत्तर:
Kc बहुत बड़ा है ⇒ उत्पाद की मात्रा अधिक होगी।
इसलिए साम्य पर NO और O3 लगभग समाप्त हो जाएँगे, NO2 और O2 की सांद्रता अधिक होगी।
🔵 प्रश्न 6.7:
प्रतिक्रिया का व्यंजक लिखिए जिससे पता चले कि शुद्ध तरल और ठोस को समीकरण में नहीं लिया जाता।
🟢 उत्तर:
उदाहरण:
CaCO3(s) ⇌ CaO(s) + CO2(g)
Kc = [CO2]
क्योंकि ठोस पदार्थों की सांद्रता नियत होती है, अतः उन्हें नहीं लिया जाता।
🔵 प्रश्न 6.8:
2NO(g) + Br2(g) ⇌ 2NOBr(g)
यदि प्रारंभ में NO = 0.087 mol, Br2 = 0.0437 mol, और NOBr = 0.0518 mol हैं, तो Kc ज्ञात कीजिए।
🟢 उत्तर:
मान लें कुल आयतन = 1 L
Kc = [NOBr]^2 / ([NO]^2 * [Br2])
= (0.0518)^2 / ((0.087)^2 * 0.0437)
= 0.002683 / (0.007569 * 0.0437)
= 0.002683 / 0.00033
Kc ≈ 8.1
✔ Kc = 8.1
🔵 प्रश्न 6.9:
2SO2(g) + O2(g) ⇌ 2SO3(g), Kp = 2.0 × 10^10 at 450 K
कुल दाब = 10 bar, [SO3] = 0.5, [SO2] = 0.3, [O2] = 0.2
क्या मिश्रण साम्य पर है?
🟢 उत्तर:
Qp = (PSO3)^2 / ((PSO2)^2 * PO2)
= (0.5)^2 / ((0.3)^2 * 0.2) = 0.25 / (0.09 * 0.2) = 0.25 / 0.018 = 13.9
Qp << Kp
अतः प्रतिक्रिया उत्पादों की ओर बढ़ेगी।
🔵 प्रश्न 6.10:
HI(g) ⇌ H2(g) + I2(g), प्रारंभ में HI = 0.20 atm, H2 = 0, I2 = 0
साम्य पर HI = 0.04 atm
Kp ज्ञात कीजिए।
🟢 उत्तर:
परिवर्तन: HI – 2x, H2 = x, I2 = x
0.20 – 2x = 0.04 ⇒ 2x = 0.16 ⇒ x = 0.08
Kp = (PH2 * PI2) / (PHI)^2
= (0.08 * 0.08) / (0.04)^2
= 0.0064 / 0.0016 = 4.0
✔ Kp = 4.0
🔵 प्रश्न 6.11:
500 K पर 20 लीटर के पात्र में 1.57 मोल N2, 1.92 मोल H2 तथा 8.13 मोल NH3 रखे गये।
अभिक्रिया: N2(g) + 3H2(g) ⇌ 2NH3(g)
यदि Kc = 1.7 × 10^-2 है, तो क्या मिश्रण साम्य पर है? यदि नहीं, तो किस दिशा में अभिक्रिया होगी?
🟢 उत्तर:
सांद्रता:
[N2] = 1.57 / 20 = 0.0785 M
[H2] = 1.92 / 20 = 0.096 M
[NH3] = 8.13 / 20 = 0.4065 M
अब Qc = [NH3]^2 / ([N2] × [H2]^3)
= (0.4065)^2 / (0.0785 × 0.096^3)
= 0.1652 / (0.0785 × 0.0008847)
= 0.1652 / 0.0000693 = 2383
अब Qc = 2383 > Kc = 1.7 × 10^-2
✔ इसलिए मिश्रण साम्य पर नहीं है, तथा अभिक्रिया वाम (Reactants) की ओर जाएगी।
🔵 प्रश्न 6.12:
2NO2(g) ⇌ 2NO(g) + O2(g), Kc = 2.0 × 10^-10 at 300 K
प्रारंभ में केवल NO2 = 0.1 M है। साम्य पर NO2 की सांद्रता लगभग क्या होगी?
🟢 उत्तर:
मान लें विघटन x M हुआ:
NO2 = 0.1 – 2x, NO = 2x, O2 = x
Kc = (2x)^2 × x / (0.1 – 2x)^2 ≈ 4x^3 / 0.01 = 2 × 10^-10
⇒ x^3 = 5 × 10^-13 ⇒ x = 7.9 × 10^-5
[N2O4] ≈ 0.1 – 2(7.9 × 10^-5) ≈ 0.0998 M
✔ लगभग पूरी मात्रा NO2 के रूप में रहेगी।
🔵 प्रश्न 6.13:
यदि Kp = Kc(RT)^Δn है, तो 300 K पर
H2(g) + I2(g) ⇌ 2HI(g)
के लिए Kp और Kc का संबंध क्या होगा?
🟢 उत्तर:
Δn = 2 – 2 = 0
⇒ Kp = Kc(RT)^0 = Kc × 1
✔ अतः Kp = Kc
🔵 प्रश्न 6.14:
Kp = 4 × 10^-2 at 300 K
अभिक्रिया: 2SO2(g) + O2(g) ⇌ 2SO3(g)
RT = 24.6 L·atm·mol^-1
Kc ज्ञात कीजिए।
🟢 उत्तर:
Δn = 2 – 3 = -1
Kp = Kc(RT)^Δn
Kc = Kp × (RT)^1
= 4 × 10^-2 × 24.6 = 0.984
✔ Kc = 0.984
🔵 प्रश्न 6.15:
2NOCl(g) ⇌ 2NO(g) + Cl2(g), Kp = 1.8 × 10^-2 at 500 K
Kc ज्ञात कीजिए।
🟢 उत्तर:
Δn = (2 + 1) – 2 = 1
Kp = Kc(RT)^Δn
Kc = Kp / (RT)
= 1.8 × 10^-2 / (0.0821 × 500)
= 1.8 × 10^-2 / 41.05 = 4.38 × 10^-4
✔ Kc = 4.38 × 10^-4
🔵 प्रश्न 6.16:
CaCO3(s) ⇌ CaO(s) + CO2(g), Kp = 167 at 1073 K
Kc ज्ञात कीजिए।
🟢 उत्तर:
Δn = 1 – 0 = 1
Kp = Kc(RT)^Δn
Kc = Kp / (RT)
= 167 / (0.0821 × 1073)
= 167 / 88.18 = 1.89
✔ Kc = 1.89
🔵 प्रश्न 6.17:
यदि किसी अभिक्रिया में Δn = 0, तो Kp और Kc में क्या संबंध होगा?
🟢 उत्तर:
जब Δn = 0
Kp = Kc(RT)^0 = Kc
✔ अतः Kp = Kc
🔵 प्रश्न 6.18:
एक साम्य अवस्था में यदि दाब बढ़ाया जाए तो अभिक्रिया किस दिशा में जाएगी?
🟢 उत्तर:
दाब बढ़ाने पर साम्य उस दिशा में खिसकेगा जहाँ गैस के मोल कम हैं।
यदि दोनों ओर मोल बराबर हों तो कोई प्रभाव नहीं।
🔵 प्रश्न 6.19:
ताप बढ़ाने पर साम्य किस दिशा में खिसकेगा?
🟢 उत्तर:
ताप बढ़ाने पर साम्य उस दिशा में जाएगा जहाँ उष्माशोषी अभिक्रिया होती है ताकि अतिरिक्त ऊष्मा उपभोग हो।
ताप घटाने पर उष्माक्षेपी अभिक्रिया की दिशा में खिसकाव।
🔵 प्रश्न 6.20:
यदि किसी अभिक्रिया में उत्प्रेरक मिलाया जाए, तो साम्य स्थिरांक पर क्या प्रभाव पड़ेगा?
🟢 उत्तर:
उत्प्रेरक केवल साम्य तक पहुँचने की दर बढ़ाता है।
✔ साम्य स्थिरांक (Kc, Kp) पर कोई प्रभाव नहीं पड़ता।
🔵 प्रश्न 6.21:
N₂(g) + 3H₂(g) ⇌ 2NH₃(g) (500 K) के लिए Kc = 0.061 है।
किस मान पर मिश्रण साम्य पर होगा?
यदि 3.0 mol L⁻¹ N₂, 2.0 mol L⁻¹ H₂ तथा 0.5 mol L⁻¹ NH₃ हों, तो क्या मिश्रण साम्य पर है?
🟢 उत्तर:
Qc = [NH₃]² / ([N₂] × [H₂]³)
= (0.5)² / (3.0 × 2.0³)
= 0.25 / (3.0 × 8.0)
= 0.25 / 24.0 = 0.0104
अब Qc = 0.0104 < Kc = 0.061
✔ अतः मिश्रण साम्य पर नहीं है, अभिक्रिया दाएँ (Products) की ओर बढ़ेगी।
🔵 प्रश्न 6.22:
2BrCl(g) ⇌ Br₂(g) + Cl₂(g)
500 K पर Kc = 32 है। यदि प्रारंभ में BrCl की सांद्रता 3.3 × 10⁻³ mol L⁻¹ है, तो साम्य पर इसकी सांद्रता ज्ञात कीजिए।
🟢 उत्तर:
मान लें x mol L⁻¹ विघटित हुआ।
साम्य पर:
[BrCl] = 3.3 × 10⁻³ – 2x
[Br₂] = x
[Cl₂] = x
Kc = (x × x) / (3.3 × 10⁻³ – 2x)² = 32
मान छोटा है ⇒ 2x ≪ 3.3 × 10⁻³
⇒ Kc ≈ x² / (3.3 × 10⁻³)²
x² = 32 × (3.3 × 10⁻³)² = 32 × 1.089 × 10⁻⁵ = 3.48 × 10⁻⁴
x = 1.86 × 10⁻²
लेकिन x > प्रारंभिक सांद्रता ⇒ मान्य नहीं
✔ अतः यह अनुमान गलत; समीकरण को संख्यात्मक रूप से हल करने की आवश्यकता है। यहाँ संकेतात्मक उत्तर: अभिक्रिया दाएँ बढ़ेगी, BrCl घटेगा।
🔵 प्रश्न 6.23:
1127 K एवं 1 atm दाब पर CO तथा CO₂ के गैसीय मिश्रण में 90.55% (मोल अंश) CO है।
C(s) + CO₂(g) ⇌ 2CO(g)
के लिए Kc ज्ञात कीजिए।
🟢 उत्तर:
मोल अंश: CO = 0.9055, CO₂ = 0.0945
कुल दाब = 1 atm
P(CO) = 0.9055 atm
P(CO₂) = 0.0945 atm
Kp = (P(CO))² / (P(CO₂)) = (0.9055)² / 0.0945
= 0.8199 / 0.0945 = 8.68
Δn = 2 – 1 = 1
Kp = Kc(RT)^Δn ⇒ Kc = Kp / (RT)
= 8.68 / (0.0821 × 1127) = 8.68 / 92.42 = 0.0939
✔ Kc = 0.0939
🔵 प्रश्न 6.24:
298 K पर NO(g) + ½ O₂(g) ⇌ NO₂(g)
ΔG°(NO₂) = 52.0 kJ/mol, ΔG°(NO) = 87.0 kJ/mol, ΔG°(O₂) = 0
Kc ज्ञात कीजिए।
🟢 उत्तर:
ΔG° = G°(उत्पाद) – G°(अभिकारक)
= 52.0 – [87.0 + ½(0)] = 52 – 87 = -35.0 kJ
= -35000 J
ΔG° = -RT ln K ⇒ ln K = -ΔG° / RT
= 35000 / (8.314 × 298) = 35000 / 2478.5 = 14.12
K = e^14.12 ≈ 1.35 × 10⁶
✔ Kc = 1.35 × 10⁶
🔵 प्रश्न 6.25:
निम्नलिखित में से किस अभिक्रिया में दाब घटाने पर उत्पाद की संख्या घटती है?
(क) PCl₅(g) ⇌ PCl₃(g) + Cl₂(g)
(ख) CaO(s) + CO₂(g) ⇌ CaCO₃(s)
(ग) 3Fe(s) + 4H₂O(g) ⇌ Fe₃O₄(s) + 4H₂(g)
🟢 उत्तर:
(ख) में अभिक्रिया में गैस मोल 1 → 0
✔ दाब घटाने पर अभिक्रिया बाएँ खिसकेगी।
🔵 प्रश्न 6.26:
किस अभिक्रिया में दाब बदलने पर साम्य पर प्रभाव नहीं पड़ेगा?
(क) COCl₂(g) ⇌ CO(g) + Cl₂(g)
(ख) C(s) + 2S(s) ⇌ CS₂(g)
(ग) CO(g) + C(s) ⇌ 2CO(g)
(घ) 2H₂(g) + O₂(g) ⇌ 2H₂O(g)
🟢 उत्तर:
(ग) में Δn = 2 – 1 = 1 (प्रभाव पड़ेगा)
लेकिन (घ) में Δn = 2 – 3 = -1 (प्रभाव पड़ेगा)
(ख) में 0 → 1 (प्रभाव पड़ेगा)
✔ कोई भी ऐसा नहीं जिसमें Δn = 0 हो ⇒ कोई भी नहीं।
🔵 प्रश्न 6.27:
H₂(g) + Br₂(g) ⇌ 2HBr(g), Kp = 1.6 × 10⁵ at 1024 K
यदि HBr का दाब 10 bar हो, तो H₂ और Br₂ का दाब ज्ञात कीजिए।
🟢 उत्तर:
Kp = (P_HBr)² / (P_H₂ × P_Br₂)
मान लें P_H₂ = P_Br₂ = x
⇒ Kp = (10)² / (x × x) = 100 / x² = 1.6 × 10⁵
x² = 100 / 1.6 × 10⁵ = 6.25 × 10⁻⁴
x = 0.025 bar
✔ P(H₂) = 0.025 bar, P(Br₂) = 0.025 bar
🔵 प्रश्न 6.28:
CH₄(g) + H₂O(g) ⇌ CO(g) + 3H₂(g), Kp = 4.0 × 10⁴
(i) दाब बढ़ाने पर साम्य की दिशा बताएँ।
(ii) ताप बढ़ाने पर क्या होगा?
🟢 उत्तर:
Δn = 4 – 2 = 2
✔ दाब बढ़ाने पर साम्य बाएँ (Reactants) की ओर।
यह उष्माशोषी अभिक्रिया है, अतः ताप बढ़ाने पर साम्य दाएँ।
🔵 प्रश्न 6.29:
2H₂(g) + CO(g) ⇌ CH₃OH(g)
Kp = 2.0 × 10⁴
किस दिशा में अभिक्रिया होगी यदि दाब बढ़ाएँ?
🟢 उत्तर:
Δn = 1 – 3 = -2
✔ दाब बढ़ाने पर साम्य दाएँ की ओर जाएगा।
🔵 प्रश्न 6.30:
PCl₅(g) ⇌ PCl₃(g) + Cl₂(g), ΔH° = +124.0 kJ
Kp = 8.3 × 10⁻³ at 473 K
यदि ताप बढ़ाया जाए, तो Kp पर क्या प्रभाव होगा?
🟢 उत्तर:
यह उष्माशोषी अभिक्रिया है (ΔH° > 0)
✔ ताप बढ़ाने पर Kp बढ़ेगा।
🔵 प्रश्न 6.31:
हैबर विधि में प्राकृतिक गैस से हाइड्रोजन प्राप्त करते समय उच्च ताप पर दो चरण अपनाए जाते हैं। प्रथम चरण में CO और H₂ बनते हैं। दूसरे चरण में जल-गैस परिवर्तन अभिक्रिया होती है:
CO(g) + H₂O(g) ⇌ CO₂(g) + H₂(g)
यदि 400 °C पर अभिक्रिया के प्रारम्भ में CO तथा भाप का सममोल मिश्रण (1 : 1) हो तथा कुल दाब 4.0 bar हो, तो साम्य पर H₂ का आंशिक दाब कितना होगा?
दिए गए ताप पर Kp = 10.1 है।
🟢 उत्तर:
आरम्भिक मोल: CO = 1, H₂O = 1, CO₂ = 0, H₂ = 0
मान लें x मोल अग्रगामी दिशा में क्रिया करें।
साम्य पर:
CO = 1 − x, H₂O = 1 − x, CO₂ = x, H₂ = x
कुल मोल = 2 (स्थिर)
आंशिक दाब = मोल अंश × 4.0
अतः
p_CO = 2(1 − x), p_H₂O = 2(1 − x), p_CO₂ = 2x, p_H₂ = 2x
अब
Kp = (p_CO₂ × p_H₂) / (p_CO × p_H₂O) = x² / (1 − x)²
x / (1 − x) = √10.1 = 3.178
x = 0.7606
p_H₂ = 2x = 1.52 bar
✔ साम्य पर H₂ का आंशिक दाब = 1.52 bar
🔵 प्रश्न 6.32:
नीचे लिखित अभिक्रियाओं में साम्य पर किसकी मात्रा उल्लेखनीय होगी?
(क) Cl₂(g) ⇌ 2Cl(g); K = 5 × 10⁻³⁹
(ख) Cl₂(g) + 2NO(g) ⇌ 2NOCl(g); Kc = 3.7 × 10⁸
(ग) Cl₂(g) + 2NO(g) ⇌ 2NOCl(g); Kc = 1.8
🟢 उत्तर:
K बहुत छोटा ⇒ अभिकारक अधिक
K बहुत बड़ा ⇒ उत्पाद अधिक
K ≈ 1 ⇒ दोनों तुलनीय
(क) अभिकारक (Cl₂) अधिक
(ख) उत्पाद (NOCl) अधिक
(ग) दोनों तुलनीय मात्राओं में उपस्थित
🔵 प्रश्न 6.33:
3O₂(g) ⇌ 2O₃(g), 25 °C पर K = 2.0 × 10⁻⁵⁰, [O₂] = 1.6 × 10⁻² mol L⁻¹
[O₃] ज्ञात करें।
🟢 उत्तर:
K = [O₃]² / [O₂]³
[O₃] = √(K × [O₂]³)
= √(2.0 × 10⁻⁵⁰ × (1.6 × 10⁻²)³)
= √(2.0 × 10⁻⁵⁰ × 4.096 × 10⁻⁶)
= √(8.192 × 10⁻⁵⁶) = 2.86 × 10⁻²⁸ mol L⁻¹
✔ ओज़ोन की सांद्रता अत्यन्त कम = 2.86 × 10⁻²⁸ mol L⁻¹
🔵 प्रश्न 6.34:
CO(g) + 3H₂(g) ⇌ CH₄(g) + H₂O(g)
1 L फ्लास्क, 1300 K: CO = 0.30 mol, H₂ = 0.01 mol, H₂O = 0.02 mol
Kc = 3.90
CH₄ की मोल संख्या ज्ञात करें।
🟢 उत्तर:
Kc = [CH₄][H₂O] / ([CO][H₂]³)
[CH₄] = Kc × [CO] × [H₂]³ / [H₂O]
= 3.90 × 0.30 × (0.01)³ / 0.02
= 3.90 × 0.30 × 1 × 10⁻⁶ / 0.02
= 1.17 × 10⁻⁶ / 0.02 = 5.85 × 10⁻⁵ mol
✔ CH₄ = 5.85 × 10⁻⁵ mol
🔵 प्रश्न 6.35:
संयुग्म अम्ल–क्षार युग्म क्या है? निम्न के संयुग्म अम्ल/क्षार बताइए —
HNO₃, CN⁻, HClO₄, F⁻, OH⁻, CO₃²⁻, HCOO⁻
🟢 उत्तर:
अम्ल H⁺ दान करता है → संयुग्म क्षार
क्षार H⁺ ग्रहण करता है → संयुग्म अम्ल
HNO₃ → NO₃⁻
CN⁻ → HCN
HClO₄ → ClO₄⁻
F⁻ → HF
OH⁻ → H₂O
CO₃²⁻ → HCO₃⁻
HCOO⁻ → HCOOH
🔵 प्रश्न 6.36:
निम्न को लेविस अम्ल/क्षार वर्गीकृत करें — OH⁻, F⁻, H⁺, BCl₃
🟢 उत्तर:
OH⁻: इलेक्ट्रॉन युग्म दाता ⇒ लेविस क्षार
F⁻: इलेक्ट्रॉन युग्म दाता ⇒ लेविस क्षार
H⁺: इलेक्ट्रॉन युग्म ग्रहणकर्ता ⇒ लेविस अम्ल
BCl₃: रिक्त p-कक्षा, ग्रहणकर्ता ⇒ लेविस अम्ल
🔵 प्रश्न 6.37:
नीचे दिये गये प्रत्येक युग्म में से कौन-सा प्रबल अम्ल है और क्यों?
(क) HCl और HF
(ख) HNO₃ और HNO₂
(ग) H₂SO₃ और H₂SeO₃
🟢 उत्तर:
अम्ल की प्रबलता उसकी H⁺ दान करने की क्षमता पर निर्भर करती है।
(क) HCl > HF क्योंकि HF में H–F बन्ध अत्यधिक सशक्त है, इस कारण H⁺ मुक्त करना कठिन।
(ख) HNO₃ > HNO₂ क्योंकि अधिक ऑक्सीजन होने से नकारात्मक आवेश का स्थिरीकरण अधिक होता है।
(ग) H₂SeO₃ > H₂SO₃ क्योंकि Se का आकार बड़ा है और बन्ध कमजोर ⇒ H⁺ मुक्त करना सरल।
✔ अतः क्रम: (क) HCl, (ख) HNO₃, (ग) H₂SeO₃ प्रबल अम्ल हैं।
🔵 प्रश्न 6.38:
निम्नलिखित में से कौन-सा प्रबल क्षार है और क्यों?
(क) NH₄OH और NaOH
(ख) KOH और NaOH
🟢 उत्तर:
(क) NaOH > NH₄OH क्योंकि NaOH पूर्णत: आयनित होकर अधिक OH⁻ देता है।
(ख) KOH ≈ NaOH, दोनों प्रबल क्षार हैं, परन्तु KOH थोड़ा अधिक आयनित होता है।
✔ निष्कर्ष: NaOH और KOH प्रबल क्षार हैं।
🔵 प्रश्न 6.39:
25 °C पर जल का आयनीकरण नियतांक Kw = 1 × 10⁻¹⁴ है।
pH = 6.0 वाले विलयन में [H₃O⁺] और [OH⁻] ज्ञात कीजिए।
🟢 उत्तर:
pH = −log[H₃O⁺]
⇒ [H₃O⁺] = 10^(−pH) = 10^(−6) = 1 × 10⁻⁶ mol L⁻¹
Kw = [H₃O⁺][OH⁻] ⇒ [OH⁻] = Kw / [H₃O⁺]
= 1 × 10⁻¹⁴ / 1 × 10⁻⁶ = 1 × 10⁻⁸ mol L⁻¹
✔ [H₃O⁺] = 1 × 10⁻⁶ mol L⁻¹
✔ [OH⁻] = 1 × 10⁻⁸ mol L⁻¹
🔵 प्रश्न 6.40:
25 °C पर 0.001 M NaOH विलयन का pH ज्ञात कीजिए।
🟢 उत्तर:
NaOH प्रबल क्षार ⇒ पूर्ण आयनीकरण: [OH⁻] = 0.001 = 1 × 10⁻³ mol L⁻¹
pOH = −log[OH⁻] = −log(10⁻³) = 3
pH + pOH = 14 ⇒ pH = 14 − 3 = 11
✔ pH = 11
🔵 प्रश्न 6.41:
25 °C पर जल में [H₃O⁺] = 1 × 10⁻⁵ mol L⁻¹ है।
pH तथा [OH⁻] ज्ञात कीजिए।
🟢 उत्तर:
pH = −log[H₃O⁺] = −log(10⁻⁵) = 5
Kw = [H₃O⁺][OH⁻] = 1 × 10⁻¹⁴
[OH⁻] = 1 × 10⁻¹⁴ / 1 × 10⁻⁵ = 1 × 10⁻⁹ mol L⁻¹
✔ pH = 5, [OH⁻] = 1 × 10⁻⁹ mol L⁻¹
यह अम्लीय विलयन है।
🔵 प्रश्न 6.42:
0.01 M HCl विलयन का pH ज्ञात कीजिए।
🟢 उत्तर:
HCl प्रबल अम्ल ⇒ पूर्ण आयनीकरण
[H₃O⁺] = 0.01 = 1 × 10⁻² mol L⁻¹
pH = −log[H₃O⁺] = −log(10⁻²) = 2
✔ pH = 2
🔵 प्रश्न 6.43:
0.001 M HNO₃ विलयन का pH ज्ञात कीजिए।
🟢 उत्तर:
HNO₃ प्रबल अम्ल ⇒ पूर्ण आयनीकरण
[H₃O⁺] = 0.001 = 1 × 10⁻³
pH = −log(10⁻³) = 3
✔ pH = 3
🔵 प्रश्न 6.44:
25 °C पर 0.001 M HCl विलयन का pOH ज्ञात कीजिए।
🟢 उत्तर:
HCl ⇒ [H₃O⁺] = 1 × 10⁻³
pH = 3
pOH = 14 − pH = 14 − 3 = 11
✔ pOH = 11
🔵 प्रश्न 6.45
0.020 M Ba(OH)2 विलयन का pH ज्ञात कीजिए। (Ba(OH)2 को पूर्ण आयनीकृत मानें)
🟢 उत्तर
Ba(OH)2 → Ba2+ + 2 OH-
[OH-] = 2 × 0.020 = 0.040 M
pOH = −log(0.040) = 1.3979
pH = 14.0000 − 1.3979 = 12.6021
अतः pH ≈ 12.60
🔵 प्रश्न 6.46
50 mL 0.10 M HCl को 25 mL 0.10 M NaOH से मिलाया गया। बने मिश्रण का pH ज्ञात करें। (25 °C)
🟢 उत्तर
HCl के मोल = 0.10 × 0.050 = 0.0050 mol
NaOH के मोल = 0.10 × 0.025 = 0.0025 mol
अधिशेष H+ = 0.0050 − 0.0025 = 0.0025 mol
कुल आयतन = 0.050 + 0.025 = 0.075 L
[H+] = 0.0025 / 0.075 = 0.03333 M
pH = −log(0.03333) = 1.4771
अतः pH ≈ 1.48
🔵 प्रश्न 6.47
0.10 M एक एकात्मक दुर्बल अम्ल HA का प्रतिशत आयनीकरण 1.34% है। Ka तथा pKa ज्ञात कीजिए।
🟢 उत्तर
alpha = 1.34% = 0.0134
Ka = (C × alpha^2) / (1 − alpha) ≈ 0.10 × (0.0134)^2 / 0.9866
(0.0134)^2 = 1.7956 × 10^-4
Ka ≈ 0.10 × 1.7956 × 10^-4 / 0.9866 ≈ 1.82 × 10^-5
pKa = −log(Ka) = −log(1.82 × 10^-5) = 4.739
अतः Ka ≈ 1.8 × 10^-5, pKa ≈ 4.74
🔵 प्रश्न 6.48
0.10 M NH3 विलयन का pH ज्ञात कीजिए, यदि Kb(NH3) = 1.8 × 10^-5 हो। (25 °C)
🟢 उत्तर
NH3 + H2O ⇌ NH4+ + OH-
[OH-] ≈ √(Kb × C) = √(1.8 × 10^-5 × 0.10)
= √(1.8 × 10^-6) = 1.342 × 10^-3 M
pOH = −log(1.342 × 10^-3) = 2.872
pH = 14.000 − 2.872 = 11.128
अतः pH ≈ 11.13
🔵 प्रश्न 6.49
एक बफर विलयन में CH3COOH की सांद्रता 0.10 M तथा CH3COONa की 0.20 M है। Ka(CH3COOH) = 1.8 × 10^-5 दिया है। बफर का pH ज्ञात करें। (सूत्र का नाम लिखे बिना सीधे सूत्र का प्रयोग करें)
🟢 उत्तर
pH = pKa + log([लवण]/[अम्ल])
pKa = −log(1.8 × 10^-5) = 4.744
pH = 4.744 + log(0.20/0.10) = 4.744 + log(2)
log(2) = 0.3010
pH = 4.744 + 0.301 = 5.045
अतः pH ≈ 5.05
🔵 प्रश्न 6.50
AgCl का Ksp = 1.8 × 10^-10 है। 0.10 M NaCl विलयन में AgCl की घुलनशीलता s (mol L^-1) ज्ञात करें। (सामान्य आयन प्रभाव)
🟢 उत्तर
AgCl(s) ⇌ Ag+ + Cl-
Ksp = [Ag+][Cl-] ≈ s × 0.10
s = Ksp / 0.10 = 1.8 × 10^-10 / 0.10 = 1.8 × 10^-9 M
अतः घुलनशीलता s = 1.8 × 10^-9 mol L^-1
🔵 प्रश्न 6.51
PbCl2 का Ksp = 1.7 × 10^-5 है। शुद्ध जल में PbCl2 की घुलनशीलता s (mol L^-1) ज्ञात करें। (25 °C)
🟢 उत्तर
PbCl2(s) ⇌ Pb2+ + 2 Cl-
Ksp = [Pb2+][Cl-]^2 = s × (2s)^2 = 4 s^3
s^3 = Ksp / 4 = 1.7 × 10^-5 / 4 = 4.25 × 10^-6
s = (4.25 × 10^-6)^(1/3)
घनमूल का मान: (4.25)^(1/3) ≈ 1.62, (10^-6)^(1/3) = 10^-2
s ≈ 1.62 × 10^-2 M = 0.0162 M
अतः घुलनशीलता ≈ 1.62 × 10^-2 mol L^-1
🔵 प्रश्न 6.52
0.10 M NH4Cl विलयन का pH ज्ञात करें। Kb(NH3) = 1.8 × 10^-5, 25 °C पर Kw = 1.0 × 10^-14
🟢 उत्तर
NH4+ एक दुर्बल क्षार NH3 का संयुग्म अम्ल है।
Ka(NH4+) = Kw / Kb(NH3) = (1.0 × 10^-14) / (1.8 × 10^-5) = 5.56 × 10^-10
[H+] ≈ √(Ka × C) = √(5.56 × 10^-10 × 0.10)
= √(5.56 × 10^-11) = 7.46 × 10^-6 M
pH = −log(7.46 × 10^-6) = 5.127
अतः pH ≈ 5.13
🔵 प्रश्न 6.53
0.10 M एथेनोइक अम्ल CH3COOH का pH ज्ञात करें। दिया है: Ka = 1.8 × 10^-5 (25 °C)
🟢 उत्तर
CH3COOH ⇌ H+ + CH3COO-
कम आयनीकरण मानते हुए: [H+] ≈ √(Ka × C)
[H+] = √(1.8 × 10^-5 × 0.10) = √(1.8 × 10^-6) = 1.34 × 10^-3 M
pH = −log(1.34 × 10^-3) = 2.87
अतः pH ≈ 2.87
🔵 प्रश्न 6.54
प्रश्न 6.53 की ही दशा में प्रतिशत आयनीकरण ज्ञात करें।
🟢 उत्तर
alpha(%) = ([H+]/C) × 100 = (1.34 × 10^-3 / 0.10) × 100 = 1.34 %
अतः प्रतिशत आयनीकरण ≈ 1.34 %
🔵 प्रश्न 6.55
एक बफर में CH3COOH = 0.20 M और CH3COONa = 0.20 M हैं। Ka = 1.8 × 10^-5. pH ज्ञात करें।
🟢 उत्तर
pH = pKa + log([लवण]/[अम्ल])
pKa = −log(1.8 × 10^-5) = 4.74
अनुपात = 0.20/0.20 = 1 ⇒ log(1) = 0
pH = 4.74 + 0 = 4.74
अतः pH = 4.74
🔵 प्रश्न 6.56
प्रश्न 6.55 वाले 1.00 L बफर में 0.010 mol HCl मिला दिया गया। pH ज्ञात करें। आयतन परिवर्तन नगण्य मानें।
🟢 उत्तर
प्रारम्भ: CH3COOH = 0.20 mol, CH3COO- = 0.20 mol
HCl से अभिक्रिया: CH3COO- + H+ → CH3COOH
नया: CH3COO- = 0.20 − 0.010 = 0.190 mol
CH3COOH = 0.20 + 0.010 = 0.210 mol
pH = pKa + log(0.190/0.210) = 4.74 + log(0.9048)
log(0.9048) = −0.043
pH = 4.74 − 0.043 = 4.70
अतः pH ≈ 4.70
🔵 प्रश्न 6.57
उसी 1.00 L बफर (प्रश्न 6.55) में 0.010 mol NaOH मिलाएँ। pH ज्ञात करें। आयतन परिवर्तन नगण्य मानें।
🟢 उत्तर
NaOH से: CH3COOH + OH- → CH3COO- + H2O
नया: CH3COOH = 0.20 − 0.010 = 0.190 mol
CH3COO- = 0.20 + 0.010 = 0.210 mol
pH = pKa + log(0.210/0.190) = 4.74 + log(1.1053)
log(1.1053) = 0.043
pH = 4.74 + 0.043 = 4.78
अतः pH ≈ 4.78
🔵 प्रश्न 6.58
Ag2CO3 का Ksp = 8.1 × 10^-12 (25 °C). शुद्ध जल में इसकी घुलनशीलता s (mol L^-1) ज्ञात करें।
🟢 उत्तर
Ag2CO3(s) ⇌ 2 Ag+ + CO3^2-
Ksp = [Ag+]^2 [CO3^2-] = (2s)^2 (s) = 4 s^3
s^3 = Ksp / 4 = 8.1 × 10^-12 / 4 = 2.025 × 10^-12
s = (2.025 × 10^-12)^(1/3)
2.025^(1/3) ≈ 1.26; (10^-12)^(1/3) = 10^-4
s ≈ 1.26 × 10^-4 mol L^-1
अतः घुलनशीलता ≈ 1.26 × 10^-4 M
🔵 प्रश्न 6.59
AgCl का Ksp = 1.8 × 10^-10. किसी विलयन में [Ag+] = 1.0 × 10^-4 M है। AgCl का अवक्षेप प्रारम्भ होने के लिए न्यूनतम [Cl-] कितनी होनी चाहिए?
🟢 उत्तर
अवक्षेप प्रारम्भ की शर्त: [Ag+][Cl-] = Ksp
[Cl-]min = Ksp / [Ag+] = (1.8 × 10^-10) / (1.0 × 10^-4) = 1.8 × 10^-6 M
अतः न्यूनतम [Cl-] = 1.8 × 10^-6 M
🔵 प्रश्न 6.60
CaF2 का Ksp = 3.9 × 10^-11. 0.10 M NaF विलयन में CaF2 की घुलनशीलता s ज्ञात करें (सामान्य आयन प्रभाव)।
🟢 उत्तर
CaF2(s) ⇌ Ca2+ + 2 F-
Ksp = [Ca2+][F-]^2 ≈ s × (0.10)^2 = s × 0.010
s = Ksp / 0.010 = 3.9 × 10^-11 / 0.010 = 3.9 × 10^-9 M
अतः घुलनशीलता s = 3.9 × 10^-9 mol L^-1
🔵 प्रश्न 6.61
0.050 M HCl के 40.0 mL को 0.100 M NaOH के 10.0 mL के साथ मिलाया गया। मिश्रण का pH ज्ञात कीजिए। (25 °C)
🟢 उत्तर
HCl के मोल = 0.050 × 0.040 = 0.00200 mol
NaOH के मोल = 0.100 × 0.010 = 0.00100 mol
अधिशेष H+ = 0.00200 − 0.00100 = 0.00100 mol
कुल आयतन = 0.040 + 0.010 = 0.050 L
[H+] = 0.00100 / 0.050 = 0.0200 M
pH = −log(0.0200) = 1.699
अतः pH ≈ 1.70
🔵 प्रश्न 6.62
0.20 M NH3 तथा 0.20 M NH4Cl से निर्मित बफर का pH ज्ञात करें। Kb(NH3) = 1.8 × 10^-5 (25 °C)
🟢 उत्तर
Ka(NH4+) = Kw / Kb = 1.0 × 10^-14 / 1.8 × 10^-5 = 5.56 × 10^-10
pKa = −log(5.56 × 10^-10) = 9.255
pH = pKa + log([क्षार-लवण]/[संयुग्म-अम्ल]) = 9.255 + log(0.20/0.20) = 9.255
अतः pH ≈ 9.26
🔵 प्रश्न 6.63
0.10 M CH3COOH (Ka = 1.8 × 10^-5) और 0.05 M CH3COONa का 1.00 L बफर है। इसमें 0.010 mol HCl मिलाने पर pH कितना होगा? आयतन परिवर्तन नगण्य मानें।
🟢 उत्तर
आरम्भ: अम्ल = 0.10 mol, लवण = 0.05 mol
HCl लवण के साथ अभिक्रिया: CH3COO- + H+ → CH3COOH
नया: लवण = 0.05 − 0.010 = 0.040 mol, अम्ल = 0.10 + 0.010 = 0.110 mol
pKa = −log(1.8 × 10^-5) = 4.744
pH = pKa + log(लवण/अम्ल) = 4.744 + log(0.040/0.110)
अनुपात = 0.3636, log(0.3636) = −0.439
pH = 4.744 − 0.439 = 4.305
अतः pH ≈ 4.31
🔵 प्रश्न 6.64
0.10 M NH3 (Kb = 1.8 × 10^-5) और 0.10 M NH4Cl के 500 mL बफर में 0.0050 mol NaOH मिलाया। अंतिम pH ज्ञात करें। आयतन परिवर्तन नगण्य मानें।
🟢 उत्तर
प्रारम्भ: NH3 = 0.10 × 0.500 = 0.0500 mol, NH4+ = 0.0500 mol
NaOH, NH4+ को घटाएगा: NH4+ + OH- → NH3 + H2O
नया: NH4+ = 0.0500 − 0.0050 = 0.0450 mol
NH3 = 0.0500 + 0.0050 = 0.0550 mol
Ka(NH4+) = Kw/Kb = 5.56 × 10^-10, pKa = 9.255
pH = pKa + log(NH3/NH4+) = 9.255 + log(0.0550/0.0450)
अनुपात = 1.2222, log = 0.087
pH = 9.255 + 0.087 = 9.342
अतः pH ≈ 9.34
🔵 प्रश्न 6.65
Ag2CrO4 का Ksp = 1.1 × 10^-12 (25 °C). शुद्ध जल में घुलनशीलता s (mol L^-1) ज्ञात करें।
🟢 उत्तर
Ag2CrO4 ⇌ 2 Ag+ + CrO4^2-
Ksp = [Ag+]^2 [CrO4^2-] = (2s)^2 (s) = 4 s^3
s^3 = Ksp/4 = 1.1 × 10^-12 / 4 = 2.75 × 10^-13
s = (2.75 × 10^-13)^(1/3)
2.75^(1/3) ≈ 1.40, (10^-13)^(1/3) = 10^(-13/3) = 10^-4.333 = 4.68 × 10^-5
s ≈ 1.40 × 4.68 × 10^-5 = 6.55 × 10^-5 mol L^-1
अतः s ≈ 6.6 × 10^-5 M
🔵 प्रश्न 6.66
AgCl और Ag2CrO4 में से कौन पहले अवक्षेपित होगा जब 0.10 M AgNO3 को धीरे-धीरे 0.010 M NaCl तथा 0.010 M K2CrO4 वाले विलयन में मिलाया जाए? Ksp(AgCl) = 1.8 × 10^-10, Ksp(Ag2CrO4) = 1.1 × 10^-12
🟢 उत्तर
अवक्षेप की शर्त: [Ag+]min = Ksp / [X-]^n
AgCl: [Ag+]min = 1.8 × 10^-10 / 0.010 = 1.8 × 10^-8
Ag2CrO4: Ksp = [Ag+]^2 [CrO4^2-] ⇒ [Ag+]min = sqrt(Ksp / [CrO4^2-])
= sqrt(1.1 × 10^-12 / 0.010) = sqrt(1.1 × 10^-10) = 1.05 × 10^-5
तुलना: 1.8 × 10^-8 << 1.05 × 10^-5
अतः AgCl पहले अवक्षेपित होगा।
🔵 प्रश्न 6.67
0.10 M HCN (Ka = 6.2 × 10^-10) का pH ज्ञात करें।
🟢 उत्तर
[H+] ≈ √(Ka × C) = √(6.2 × 10^-10 × 0.10)
= √(6.2 × 10^-11) = 7.87 × 10^-6
pH = −log(7.87 × 10^-6) = 5.103
अतः pH ≈ 5.10
🔵 प्रश्न 6.68
0.10 M NaCN विलयन का pH ज्ञात करें। Ka(HCN) = 6.2 × 10^-10
🟢 उत्तर
Kb(CN-) = Kw/Ka = 1.0 × 10^-14 / 6.2 × 10^-10 = 1.61 × 10^-5
[OH-] ≈ √(Kb × C) = √(1.61 × 10^-5 × 0.10)
= √(1.61 × 10^-6) = 1.269 × 10^-3
pOH = −log(1.269 × 10^-3) = 2.897
pH = 14.000 − 2.897 = 11.103
अतः pH ≈ 11.10
🔵 प्रश्न 6.69
0.10 M NH4Cl और 0.20 M NH3 का बफर 25 °C पर कितना pH देगा? Kb(NH3) = 1.8 × 10^-5
🟢 उत्तर
Ka(NH4+) = 5.56 × 10^-10, pKa = 9.255
pH = pKa + log(NH3/NH4+) = 9.255 + log(0.20/0.10)
= 9.255 + log(2) = 9.255 + 0.301 = 9.556
अतः pH ≈ 9.56
🔵 प्रश्न 6.70
0.050 M CH3COONa के विलयन में Mg(OH)2 की घुलनशीलता s ज्ञात कीजिए, यदि Ksp(Mg(OH)2) = 5.6 × 10^-12 और विलयन का pH = 9.00 हो। (25 °C)
🟢 उत्तर
pH = 9.00 ⇒ pOH = 14.00 − 9.00 = 5.00
[OH-] = 10^-5.00 = 1.0 × 10^-5 M (बफर/क्षारीय माध्यम के कारण)
Mg(OH)2 ⇌ Mg2+ + 2 OH-
Ksp = [Mg2+][OH-]^2
[Mg2+] = Ksp / [OH-]^2 = 5.6 × 10^-12 / (1.0 × 10^-5)^2 = 5.6 × 10^-12 / 1.0 × 10^-10 = 5.6 × 10^-2 M
अतः s ≈ 5.6 × 10^-2 mol L^-1
टिप्पणी: क्षारीय माध्यम में [OH-] स्थिर रहने से घुलनशीलता Ksp/[OH-]^2 से निर्धारित होती है।
🔵 प्रश्न 6.71
0.10 M NH3 विलयन में Mg(OH)2 की घुलनशीलता क्यों बढ़ जाती है? (कारण लिखें, गणना आवश्यक नहीं)
🟢 उत्तर
NH3, Mg2+ के साथ समिश्र आयन [Mg(NH3)x]^2+ बनाता है, जिससे मुक्त Mg2+ घटता है। Le-Chatelier के अनुसार ठोस Mg(OH)2 के घुलने की दिशा में साम्य खिसक कर घुलनशीलता बढ़ा देता है। साथ ही NH3, OH- उत्पन्न कर माध्यम को क्षारीय करता है जिससे घुलनशीलता Ksp/[OH-]^2 नियम से नियंत्रित रहती है।
🔵 प्रश्न 6.72
0.10 M NaF विलयन में HF का 1.0 × 10^-3 mol मिलाया गया। Ka(HF) = 6.8 × 10^-4. निर्मित बफर का pH ज्ञात करें। आयतन 1.00 L मानें।
🟢 उत्तर
आरम्भ: F- = 0.10 mol, HF = 0.0010 mol
pH = pKa + log(लवण/अम्ल)
pKa = −log(6.8 × 10^-4) = 3.167
अनुपात = 0.10 / 0.0010 = 100 ⇒ log = 2.000
pH = 3.167 + 2.000 = 5.167
अतः pH ≈ 5.17
🔵 प्रश्न 6.73
एक विलयन में [Ag+] = 1.0 × 10^-9 M है। क्या इस विलयन में AgI का अवक्षेप बनेगा यदि [I-] = 2.0 × 10^-7 M हो? Ksp(AgI) = 8.3 × 10^-17
🟢 उत्तर
आयन गुणनफल Q = [Ag+][I-] = (1.0 × 10^-9)(2.0 × 10^-7) = 2.0 × 10^-16
तुलना: Q = 2.0 × 10^-16 > Ksp = 8.3 × 10^-17
अतः Q > Ksp ⇒ अवक्षेप बनेगा।
निष्कर्ष: AgI का अवक्षेप बनेगा।
————————————————————————————————————————————————————————————————————————————
अन्य महत्वपूर्ण प्रश्न
(CBSE MODEL प्रश्न पत्र)
सिर्फ इसी पाठ से निर्मित CBSE MODEL प्रश्न पत्र।
खंड A — बहुविकल्पीय प्रश्न (Q1–Q16, प्रत्येक 1 अंक)
प्रश्न 1. रासायनिक साम्यावस्था किस स्थिति में स्थापित होती है?
केवल अग्रगामी अभिक्रिया रुक जाती है
केवल प्रतिगामी अभिक्रिया रुक जाती है
अग्रगामी व प्रतिगामी दोनों की वेग बराबर हो जाते हैं
दोनों अभिक्रियाएँ पूर्णतः समाप्त हो जाती हैं
Answer: 3
प्रश्न 2. अभिक्रिया aA + bB ⇌ cC + dD के लिए साम्य नियतांक (Kc) का सामान्य रूप है:
[A]^a [B]^b / [C]^c [D]^d
[C]^c [D]^d / [A]^a [B]^b
[A]^a [C]^c / [B]^b [D]^d
[A]^a / [B]^b
Answer: 2
प्रश्न 3. गैसीय अभिक्रिया के लिए Kp और Kc का सम्बन्ध है (Δn = गैसीय उत्पादों के मोल − गैसीय अभिकारकों के मोल):
Kp = Kc
Kp = Kc (RT)^Δn
Kp = Kc /(RT)^Δn
Kp = (Kc)^Δn
Answer: 2
प्रश्न 4. ले-शातेलिए के सिद्धान्त के अनुसार दाब बढ़ाने पर साम्य किस ओर खिसकता है?
जहाँ गैस के कुल मोल अधिक हों
जहाँ गैस के कुल मोल कम हों
कोई परिवर्तन नहीं
केवल ताप पर निर्भर
Answer: 2
कथन–कारण हेतु विकल्प-कुंजी
कथन (A) एवं कारण (R) दोनों सत्य हैं तथा R, A का सही कारण है
कथन (A) एवं कारण (R) दोनों सत्य हैं परन्तु R, A का सही कारण नहीं
कथन (A) सत्य है परन्तु R असत्य
कथन (A) असत्य है परन्तु R सत्य
प्रश्न 5 (A/R).
कथन (A): उत्प्रेरक साम्यावस्था की स्थिति (K) को नहीं बदलता।
कारण (R): उत्प्रेरक अग्रगामी और प्रतिगामी दोनों अभिक्रियाओं के वेग समान अनुपात में बढ़ाता है।
Answer: 1
प्रश्न 6. जल का आयनी गुणनफल (Kw) 25 °C पर लगभग होता है:
1 × 10⁻¹²
1 × 10⁻¹⁴
1 × 10⁻¹⁶
1 × 10⁻⁷
Answer: 2
प्रश्न 7. ब्रॉन्स्टेड–लॉरी के अनुसार अम्ल है:
इलेक्ट्रॉन युग्म ग्राही
इलेक्ट्रॉन युग्म दाता
प्रोटॉन दाता
प्रोटॉन ग्राही
Answer: 3
प्रश्न 8. यदि किसी विलयन में [H⁺] = 1 × 10⁻³ mol L⁻¹ है, तो pH होगा:
3
11
1
7
Answer: 1
प्रश्न 9. सामान्य आयन प्रभाव किसमें देखा जाता है?
वाष्प दाब
घुलनशीलता का दमन
ऊष्मा धारिता
दाब–आयतन कार्य
Answer: 2
प्रश्न 10 (A/R).
कथन (A): ताप बढ़ाने पर ऊष्माशोषी अभिक्रिया का K बढ़ता है।
कारण (R): ताप बढ़ाने से साम्य उस ओर खिसकता है जहाँ ऊष्मा का उपभोग होता है।
Answer: 1
प्रश्न 11. एक क्षीण एकमानिक अम्ल के लिए, यदि α बहुत छोटा हो, तो ओस्टवाल्ड पतलीकरण नियम देता है:
Ka = Cα²
Ka = C/α
Ka = α/C
Ka = Cα
Answer: 1
प्रश्न 12. विलयन में क्षारकीय लवण Na₂CO₃ का घोल होगा:
अम्लीय
उदासीन
क्षारीय
दोलनशील
Answer: 3
प्रश्न 13. यदि Q (आयितांक) < K हो, तो साम्य प्राप्त करने के लिए अभिक्रिया:
बाएँ जाएगी
दाएँ जाएगी
स्थिर रहेगी
ताप पर निर्भर
Answer: 2
प्रश्न 14. विलयन में बफर का मुख्य कार्य है:
ताप स्थिर रखना
दाब स्थिर रखना
pH में परिवर्तन का प्रतिरोध करना
आयतन स्थिर रखना
Answer: 3
प्रश्न 15 (A/R).
कथन (A): मजबूत अम्ल का 0.001 M विलयन, क्षीण अम्ल के 0.001 M विलयन से अधिक चालकता दर्शाता है।
कारण (R): मजबूत अम्ल पूर्णतः आयनित हो जाता है, क्षीण अम्ल आंशिक आयनित होता है।
Answer: 1
प्रश्न 16. विलेय AB(s) ⇌ A⁺(aq) + B⁻(aq) के लिए घुलनशीलता गुणनफल है:
Ksp = [AB]
Ksp = [A⁺] + [B⁻]
Ksp = [A⁺][B⁻]
Ksp = [A⁺]/[B⁻]
Answer: 3
खंड B — अति लघु उत्तरीय प्रश्न (Q17–Q21, प्रत्येक 2 अंक)
प्रश्न 17. रासायनिक साम्यावस्था का लक्षण लिखिए।
उत्तर:
🟦 अग्रगामी व प्रतिगामी वेग बराबर होते हैं; सांद्रताएँ समय के साथ स्थिर।
🟩 साम्य गतिशील होता है; अणु-स्तर पर अभिक्रिया चलती रहती है।
प्रश्न 18. ले-शातेलिए सिद्धान्त का संक्षिप्त कथन लिखिए।
उत्तर:
🟦 किसी प्रतिकूल परिवर्तन (ताप, दाब, सांद्रता) पर तन्त्र ऐसा परिवर्तन करता है जिससे उसका प्रभाव न्यूनतम हो।
🟩 अतः साम्य नई स्थिति पर खिसकता है।
प्रश्न 19. 25 °C पर जल में [H⁺] = 1 × 10⁻⁷ mol L⁻¹ क्यों होता है?
उत्तर:
🟦 Kw = [H⁺][OH⁻] = 1 × 10⁻¹⁴; उदासीन दशा में [H⁺] = [OH⁻]।
🟩 अतः [H⁺] = √Kw = 1 × 10⁻⁷ mol L⁻¹।
प्रश्न 20. क्षीण अम्ल HA के 0.10 M विलयन में α = 0.02 हो, तो Ka का मान ज्ञात करें (सरलीकृत रूप Ka = Cα²)।
उत्तर:
➤ सूत्र: Ka = Cα²
➤ प्रतिस्थापन: Ka = 0.10 × (0.02)² = 0.10 × 0.0004 = 4.0 × 10⁻⁵
✅ परिणाम: Ka = 4.0 × 10⁻⁵
प्रश्न 21. सामान्य आयन प्रभाव का एक अनुप्रयोग लिखिए।
उत्तर:
🟦 घुलनशीलता का दमन: AgCl में Cl⁻ सामान्य आयन जोड़ने पर घुलनशीलता घटती है।
🟩 विश्लेषणात्मक अवक्षेपण में सूक्ष्म आयनों को अलग करने में सहायक।
खंड C — लघु उत्तरीय प्रश्न (Q22–Q28, प्रत्येक 3 अंक)
प्रश्न 22. अभिक्रिया N₂O₄(g) ⇌ 2NO₂(g) के लिए Δn = +1 है। 25 °C पर Kc = 0.25 हो तो Kp ज्ञात करें।
उत्तर:
➤ सम्बन्ध: Kp = Kc (RT)^Δn
➤ प्रतिस्थापन: R = 0.0821 L atm mol⁻¹ K⁻¹, T = 298 K, Δn = 1
Kp = 0.25 × (0.0821 × 298) ≈ 0.25 × 24.5 ≈ 6.13
✅ उत्तर: Kp ≈ 6.1 (लगभग)
प्रश्न 23. 1 L पात्र में अभिक्रिया A ⇌ B के लिए प्रारम्भ में केवल A के 1 mol हैं। साम्य पर A के 0.6 mol शेष हैं। Kc ज्ञात कीजिए।
उत्तर:
🟦 प्रारम्भ: [A] = 1.0, [B] = 0
🟩 परिवर्तन: A में 0.4 घटा ⇒ B में 0.4 बढ़ा
🧮 Kc = [B]/[A] = 0.4/0.6 = 2/3 = 0.667
✅ उत्तर: Kc = 0.667
प्रश्न 24. बफर घोल कैसे pH को स्थिर रखता है? अम्लीय बफर का सामान्य युग्म लिखिए।
उत्तर:
🟦 रचना: दुर्बल अम्ल (HA) + उसका लवण (A⁻) → जोड़े गए H⁺/OH⁻ को निष्क्रिय करते हैं।
🟩 अम्लीय बफर उदाहरण: CH₃COOH / CH₃COONa (सिद्धान्त रूप से HA/A⁻ युग्म)।
🟪 परिणाम: pH में परिवर्तन का प्रतिरोध।
प्रश्न 25. घुलनशीलता गुणनफल से घुलनशीलता (s) कैसे निकालते हैं? AgCl के लिए व्यक्त कीजिए।
उत्तर:
🟦 AgCl(s) ⇌ Ag⁺ + Cl⁻; Ksp = [Ag⁺][Cl⁻]
🟩 शुद्ध जल में: [Ag⁺] = [Cl⁻] = s ⇒ Ksp = s²
🧮 अतः s = √Ksp
प्रश्न 26. अभिक्रिया 2SO₂(g) + O₂(g) ⇌ 2SO₃(g) पर दाब बढ़ाने का प्रभाव बताइए।
उत्तर:
🟦 बाएँ पक्ष पर कुल 3 mol गैस, दाएँ पर 2 mol।
🟩 दाब बढ़ाने पर साम्य कम मोल वाली ओर खिसकेगा।
✅ परिणाम: SO₃ बनने की प्रवृत्ति बढ़ेगी।
प्रश्न 27. क्षीण क्षार BOH के लिए Kb, C तथा α के बीच सम्बन्ध लिखिए और छोटा α मानकर सरल रूप निकालिए।
उत्तर:
🟦 सामान्य: Kb = (Cα²)/(1 − α)
🟩 यदि α ≪ 1 ⇒ 1 − α ≈ 1
✅ सरलीकृत: Kb ≈ Cα²
प्रश्न 28. 25 °C पर एक संतृप्त विलयन में Mg(OH)₂ का Ksp = 1.2 × 10⁻¹¹ है। शुद्ध जल में [OH⁻] ज्ञात कीजिए।
उत्तर:
🟦 Mg(OH)₂(s) ⇌ Mg²⁺ + 2OH⁻; मान लें घुलनशीलता = s
🟩 [Mg²⁺] = s, [OH⁻] = 2s ⇒ Ksp = s(2s)² = 4s³
➤ s³ = Ksp/4 = 1.2×10⁻¹¹ / 4 = 3.0×10⁻¹² ⇒ s = 1.44×10⁻⁴ mol L⁻¹ (लगभग)
✅ [OH⁻] = 2s ≈ 2.88 × 10⁻⁴ mol L⁻¹
खंड D — प्रकरण आधारित प्रश्न (Q29–Q30, प्रत्येक 4 अंक)
प्रश्न 29.
“अभिक्रिया N₂(g) + 3H₂(g) ⇌ 2NH₃(g) ऊष्माक्षेपी है।”
(i) ताप बढ़ाने पर साम्य किस ओर खिसकेगा? (1)
(ii) दाब बढ़ाने का प्रभाव क्या होगा? (1)
(iii) इस अभिक्रिया में उत्प्रेरक की भूमिका स्पष्ट कीजिए। (2)
उत्तर:
🟦 (i) ताप बढ़ाने पर साम्य बाएँ (अभिकारकों) की ओर खिसकेगा।
🟩 (ii) दाब बढ़ाने पर साम्य उस ओर जाएगा जहाँ गैस के मोल कम हैं ⇒ दाएँ (NH₃ का निर्माण)।
🟪 (iii) उत्प्रेरक केवल साम्य तक पहुँचने की गति बढ़ाता है, साम्य स्थिति (K) नहीं बदलता।
प्रश्न 30.
25 °C पर CH₃COOH (0.1 M) का pH लगभग 2.9 पाया गया।
(i) [H⁺] की गणना कीजिए। (1)
(ii) आयनीकरण डिग्री (α) ज्ञात कीजिए। (1)
(iii) Ka का मान निकालिए। (2)
उत्तर:
🟦 (i) pH = 2.9 ⇒ [H⁺] = 10⁻²·⁹ ≈ 1.26 × 10⁻³ M
🟩 (ii) α = [H⁺]/C = 1.26×10⁻³ / 0.1 = 0.0126 ≈ 1.3 %
🟪 (iii) Ka = Cα² = 0.1 × (0.0126)² = 0.1 × 1.59×10⁻⁴ = 1.59×10⁻⁵
✅ उत्तर: Ka ≈ 1.6 × 10⁻⁵
खंड E — दीर्घ उत्तरीय प्रश्न (Q31–Q33, प्रत्येक 5 अंक)
प्रश्न 31.
ले-शातेलिए का सिद्धान्त विस्तार से समझाइए और इसके दो अनुप्रयोग दीजिए।
उत्तर:
🟦 सिद्धान्त: जब किसी साम्य पर ताप, दाब अथवा सांद्रता का परिवर्तन किया जाता है, तो तन्त्र ऐसा परिवर्तन करता है जिससे प्रभाव न्यूनतम हो।
🟩 अनुप्रयोग:
औद्योगिक NH₃ निर्माण (हैबर प्रक्रिया): दाब बढ़ाने से NH₃ उत्पादन बढ़ता है।
औद्योगिक H₂SO₄ निर्माण (कॉन्टैक्ट प्रक्रिया): ताप घटाने से SO₃ उत्पादन बढ़ता है।
✅ निष्कर्ष: यह सिद्धान्त साम्य परिवर्तन की दिशा की भविष्यवाणी करता है।
या
घुलनशीलता गुणनफल (Ksp) का सिद्धान्त समझाइए तथा अवक्षेपण की शर्त बताइए।
प्रश्न 32.
0.1 M अमोनिया (Kb = 1.8 × 10⁻⁵) के विलयन का pH ज्ञात कीजिए।
उत्तर:
🟦 Kb = Cα² ⇒ α = √(Kb/C) = √(1.8×10⁻⁵ / 0.1) = √(1.8×10⁻⁴) ≈ 0.0134
🟩 [OH⁻] = Cα = 0.1 × 0.0134 = 1.34 × 10⁻³ M
🧮 pOH = −log(1.34×10⁻³) ≈ 2.87
pH = 14 − 2.87 = 11.13
✅ उत्तर: pH ≈ 11.1
या
बफर घोल की क्रिया-विधि समझाइए और हैण्डरसन–हैसेलबाल्च समीकरण लिखिए।
प्रश्न 33.
ऑस्टवाल्ड पतलीकरण नियम की व्याख्या कीजिए और इसे क्षीण अम्ल पर लागू कर Ka की अभिव्यक्ति निकालिए।
उत्तर:
🟦 कथन: क्षीण इलेक्ट्रोलाइट के आयनीकरण की डिग्री सांद्रता घटने पर बढ़ती है।
🟩 अभिव्यक्ति:
HA ⇌ H⁺ + A⁻
प्रारम्भिक सांद्रता = C, साम्य पर = C(1 − α), H⁺ = Cα, A⁻ = Cα
Ka = [H⁺][A⁻]/[HA] = Cα²/(1 − α)
🟪 यदि α ≪ 1 ⇒ Ka ≈ Cα²
✅ निष्कर्ष: पतला करने पर α बढ़ता है।
या
pH, pOH, [H⁺] और [OH⁻] में सम्बन्ध व्युत्पन्न कीजिए और एक उदाहरण द्वारा स्पष्ट कीजिए।
————————————————————————————————————————————————————————————————————————————
