Class 11 : Chemistry (In Hindi) – Lesson 5. उष्मागतिकी
पाठ का विश्लेषण एवं विवेचन
🔵 भूमिका ✨
ऊष्मागतिकी (Thermodynamics) रसायन विज्ञान की वह शाखा है जो ऊर्जा के विभिन्न रूपों, विशेषकर ऊष्मा (heat) और कार्य (work), तथा उनके आपसी परिवर्तन और संरक्षण के नियमों का अध्ययन करती है। यह अध्याय भौतिक और रासायनिक प्रक्रियाओं में ऊर्जा के प्रवाह और संतुलन को समझने के लिए मूलभूत है।
🟢 मूल अवधारणाएँ 📌
तंत्र और परिवेश:
➤ तंत्र वह अंश है जिस पर हम अध्ययन कर रहे हैं।
➤ परिवेश वह सबकुछ है जो तंत्र के बाहर है।
➤ प्रकार:
– उष्मारुद्ध (Isolated): ऊर्जा व पदार्थ का आदान-प्रदान नहीं।
– संपूर्ण (Closed): केवल ऊर्जा का आदान-प्रदान।
– मुक्त (Open): ऊर्जा व पदार्थ दोनों का आदान-प्रदान।
अवस्था और अवस्था-फलन:
➤ अवस्था: तंत्र को परिभाषित करने वाले गुण जैसे दाब (P), आयतन (V), तापमान (T)।
➤ अवस्था-फलन: केवल आरम्भिक और अंतिम अवस्था पर निर्भर (जैसे U, H, G, S)।
➤ पथ-फलन: मार्ग पर निर्भर (जैसे कार्य W और ऊष्मा Q)।
आन्तरिक ऊर्जा (U): तंत्र में सभी कणों की गतिज और स्थितिज ऊर्जा का योग।
🟡 ऊष्मागतिकी का प्रथम नियम (Energy Conservation Law) 🌟
सिद्धान्त: ऊर्जा न उत्पन्न होती है, न नष्ट होती है, केवल एक रूप से दूसरे रूप में परिवर्तित होती है।
गणितीय रूप: ΔU = q + w
जहाँ q = ऊष्मा, w = कार्य।
✔ उदाहरण:
यदि किसी तंत्र को स्थिर आयतन पर गरम किया जाए तो w = 0, अतः ΔU = qv।
यदि स्थिर दाब पर गरम किया जाए तो q = ΔH (एन्थैल्पी परिवर्तन)।
🟢 कार्य (Work) और ऊष्मा (Heat) ✏
विस्तार कार्य: w = −PΔV
यदि तंत्र फैलता है तो कार्य ऋणात्मक (तंत्र द्वारा परिवेश पर किया गया)।
यदि तंत्र सिकुड़ता है तो कार्य धनात्मक (परिवेश द्वारा तंत्र पर)।
ऊष्मा: ऊर्जा का प्रवाह तापमान के अन्तर के कारण।
🟡 एन्थैल्पी (H) 📍
H = U + PV
परिवर्तन: ΔH = ΔU + PΔV
स्थिर दाब पर q = ΔH।
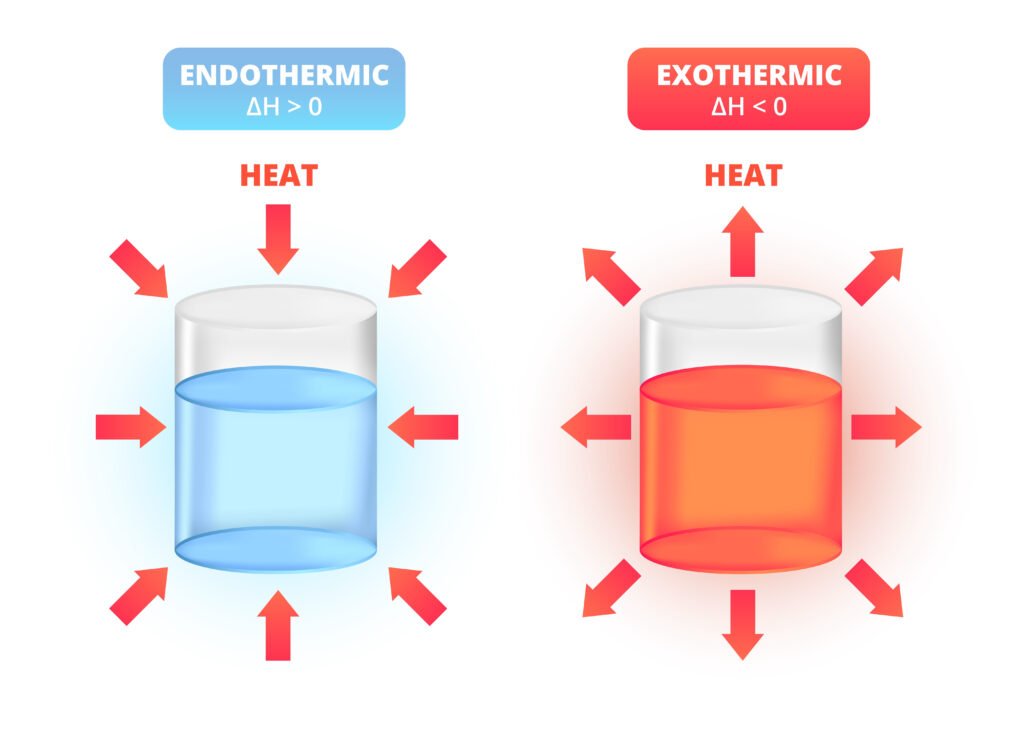
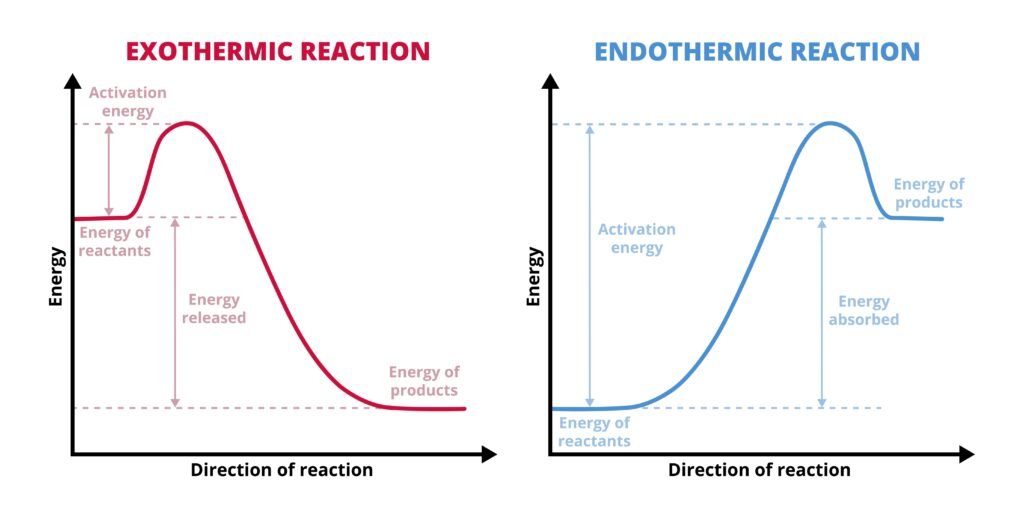
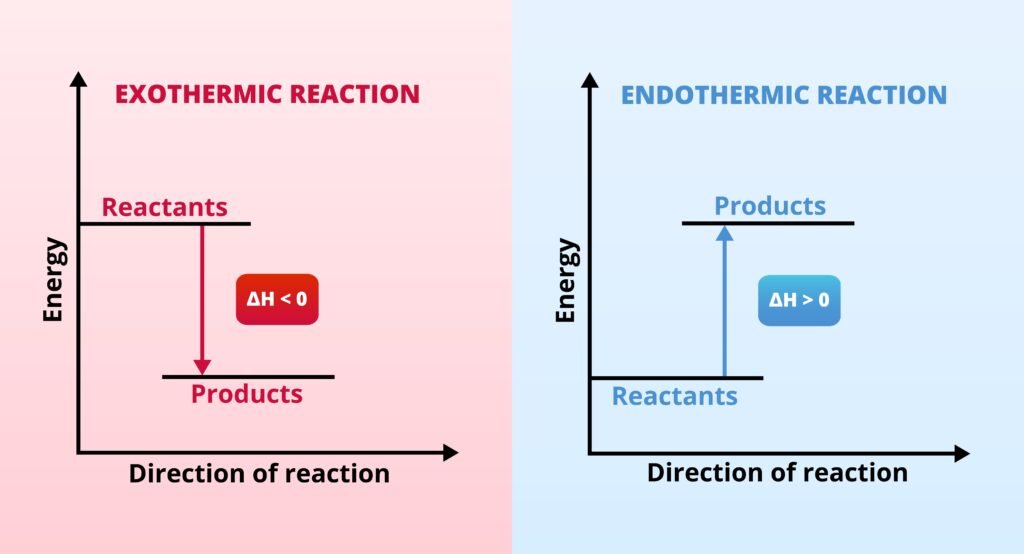
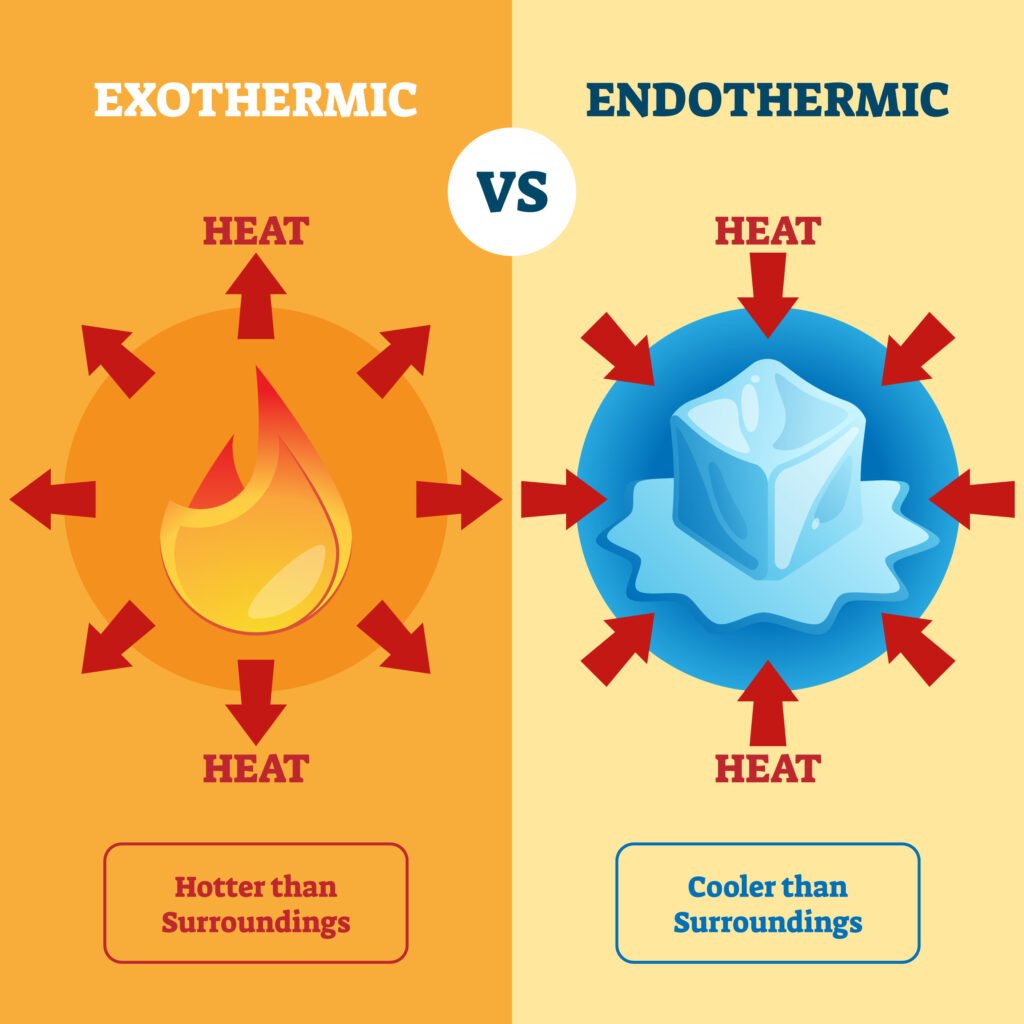
उष्माक्षेपी अभिक्रिया: ΔH < 0
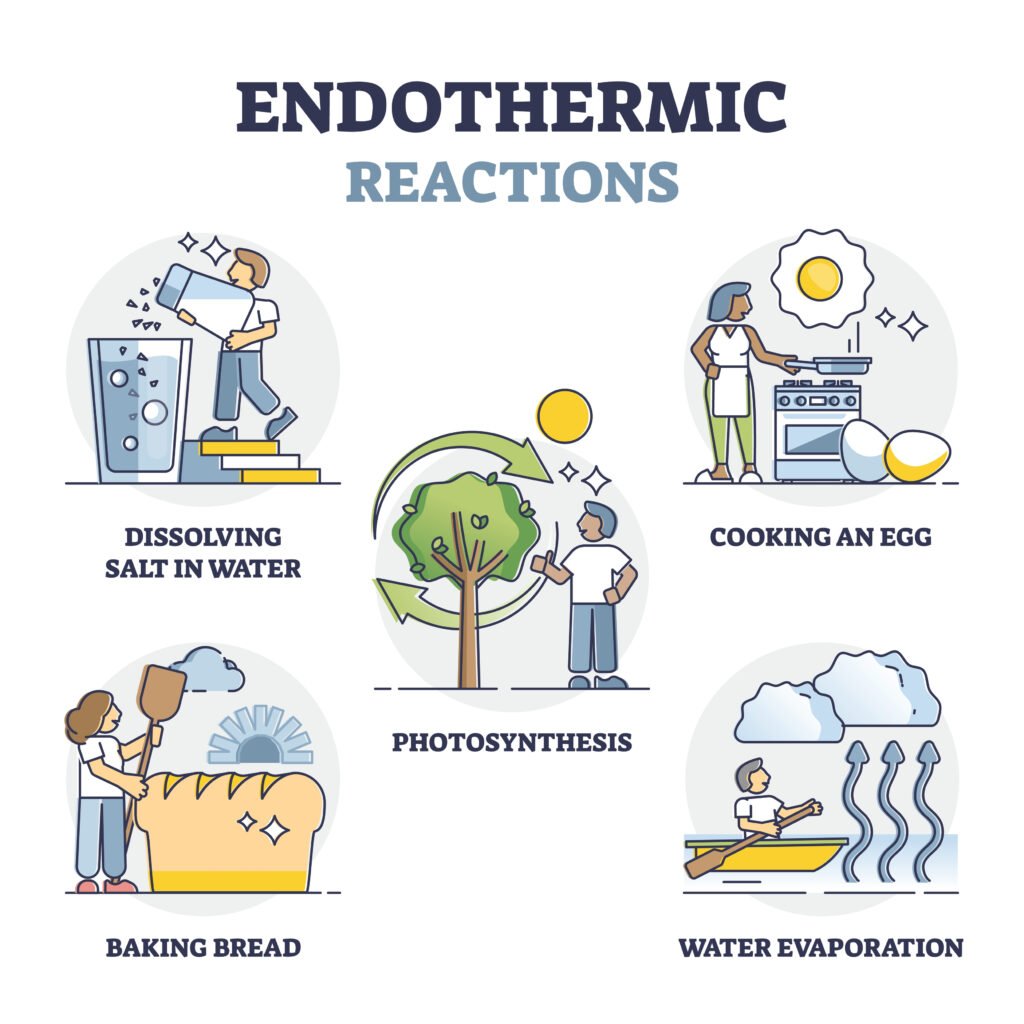
उष्माशोषी अभिक्रिया: ΔH > 0
🟢 ऊष्मागतिकी का द्वितीय नियम 💡
सिद्धान्त: कोई भी स्वस्फूर्त (spontaneous) प्रक्रिया तभी घटित होगी जब तंत्र + परिवेश की एंट्रॉपी बढ़ेगी।
एंट्रॉपी (S): अव्यवस्था या यादृच्छिकता का माप।
➤ ΔS > 0 → स्वस्फूर्त प्रवृत्ति।
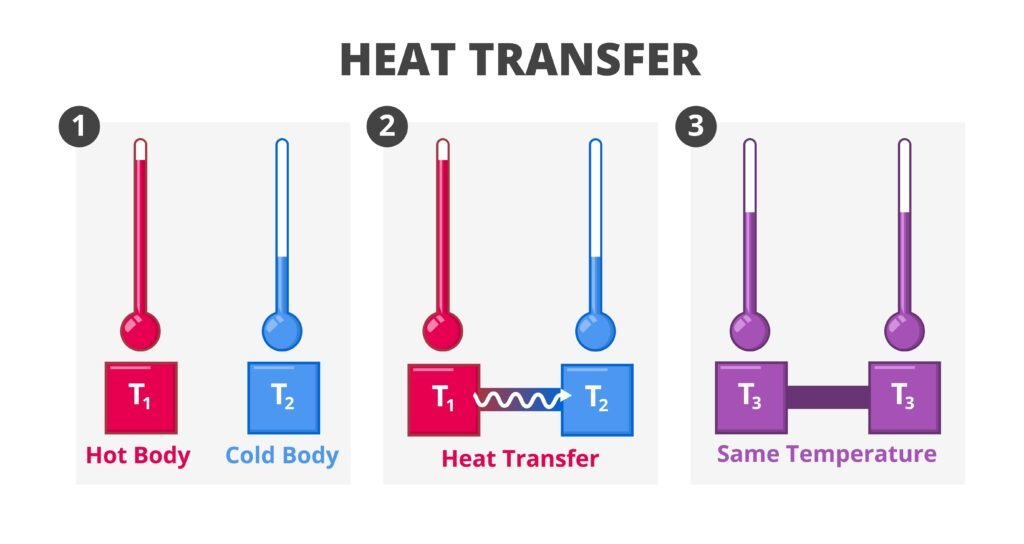
क्लॉज़ियस कथन: ऊष्मा स्वतः शीतल पिण्ड से उष्ण पिण्ड की ओर नहीं जा सकती।
केल्विन-प्लांक कथन: ऊष्मा को पूर्णतः कार्य में रूपान्तरित करना असम्भव है।
🟡 ऊष्मागतिकी का तृतीय नियम 📘
परिभाषा: शून्य केल्विन तापमान पर एक शुद्ध सुसंगठित क्रिस्टल की एंट्रॉपी शून्य होती है।
महत्व: यह हमें एंट्रॉपी के पूर्ण मान ज्ञात करने की अनुमति देता है।
🔴 गिब्स मुक्त ऊर्जा (G) 🌟
G = H − TS
परिवर्तन: ΔG = ΔH − TΔS
निष्कर्ष:
ΔG < 0 → अभिक्रिया स्वस्फूर्त।
ΔG = 0 → संतुलन।
ΔG > 0 → अभिक्रिया अस्वस्फूर्त।
🟢 अनुप्रयोग ✔
अभिक्रियाओं की दिशा व स्वस्फूर्तता का पूर्वानुमान।
एन्थैल्पी परिवर्तन से उष्माक्षेपी व उष्माशोषी अभिक्रियाओं का विभाजन।
गिब्स ऊर्जा का प्रयोग उद्योगों में, जैसे विद्युत-अपघटन की सम्भावना का निर्धारण।
एंट्रॉपी से मिश्रण, विलयन व चरण-परिवर्तन को समझना।
🔹 II. पाठ सार
🔵 सार-तत्त्व ✨
ऊष्मागतिकी ऊर्जा और उसके रूपान्तरण का अध्ययन है।
तंत्र तीन प्रकार के होते हैं: उष्मारुद्ध, संपूर्ण और मुक्त।
अवस्था-फलन जैसे U, H, G, S केवल प्रारम्भिक व अंतिम अवस्था पर निर्भर; जबकि Q और W पथ-फलन हैं।
प्रथम नियम: ΔU = q + w (ऊर्जा संरक्षण सिद्धान्त)।
एन्थैल्पी H = U + PV; स्थिर दाब पर q = ΔH।
द्वितीय नियम: स्वस्फूर्त प्रक्रिया में कुल एंट्रॉपी (ΔStotal) बढ़ती है।
एंट्रॉपी (S): अव्यवस्था का माप; ΔS > 0 → स्वस्फूर्त प्रवृत्ति।
तृतीय नियम: शुद्ध क्रिस्टल की एंट्रॉपी 0 K पर शून्य।
गिब्स ऊर्जा: ΔG = ΔH − TΔS;
➤ ΔG < 0 → स्वस्फूर्त, ➤ ΔG = 0 → संतुलन, ➤ ΔG > 0 → अस्वस्फूर्त।
व्यावहारिक उपयोग: अभिक्रियाओं की दिशा, उद्योगों में प्रक्रिया-निर्धारण, रासायनिक संतुलन, चरण-परिवर्तन, उष्मा और कार्य का आकलन।
🟢 निष्कर्ष 📌
ऊष्मागतिकी हमें रासायनिक प्रक्रियाओं के ऊर्जा संतुलन, स्वस्फूर्तता, संतुलन तथा व्यावहारिक उपयोग समझने का वैज्ञानिक आधार प्रदान करती है।
🔹 III. त्वरित पुनरावृत्ति
🔵 मुख्य बिन्दु 🌟
ऊष्मागतिकी ऊर्जा व उसके रूपान्तरण का विज्ञान है।
ΔU = q + w (प्रथम नियम)।
एन्थैल्पी (ΔH): स्थिर दाब पर ऊष्मा परिवर्तन।
एंट्रॉपी (ΔS): अव्यवस्था का माप; ΔS > 0 → स्वस्फूर्त।
गिब्स ऊर्जा: ΔG = ΔH − TΔS → स्वस्फूर्तता का निर्धारण।
तृतीय नियम: शून्य K पर शुद्ध क्रिस्टल की एंट्रॉपी शून्य।
————————————————————————————————————————————————————————————————————————————
पाठ्यपुस्त के प्रश्न
🔵 प्रश्न 5.1:
ऊष्मागतिकी अवस्था फलन एक राशि है —
(i) जो सभी परिस्थितियों के लिए स्थिर होती है।
(ii) जिसका मान पथ पर निर्भर नहीं करता है।
(iii) जो दाब-आयतन कार्य की गणना करने में सहायक होती है।
(iv) जिसका मान समय के साथ बदलता है।
🟢 उत्तर: (ii) जिसका मान पथ पर निर्भर नहीं करता है।
✏ व्याख्या:
ऊष्मागतिक राशियाँ जैसे आंतरिक ऊर्जा (U), एन्थैल्पी (H), एंट्रॉपी (S) आदि स्थिति फलन होती हैं।
इनका मान केवल प्रारंभिक और अंतिम अवस्थाओं पर निर्भर करता है।
✔ अतः यह पथ-निर्भर नहीं है।
🔵 प्रश्न 5.2:
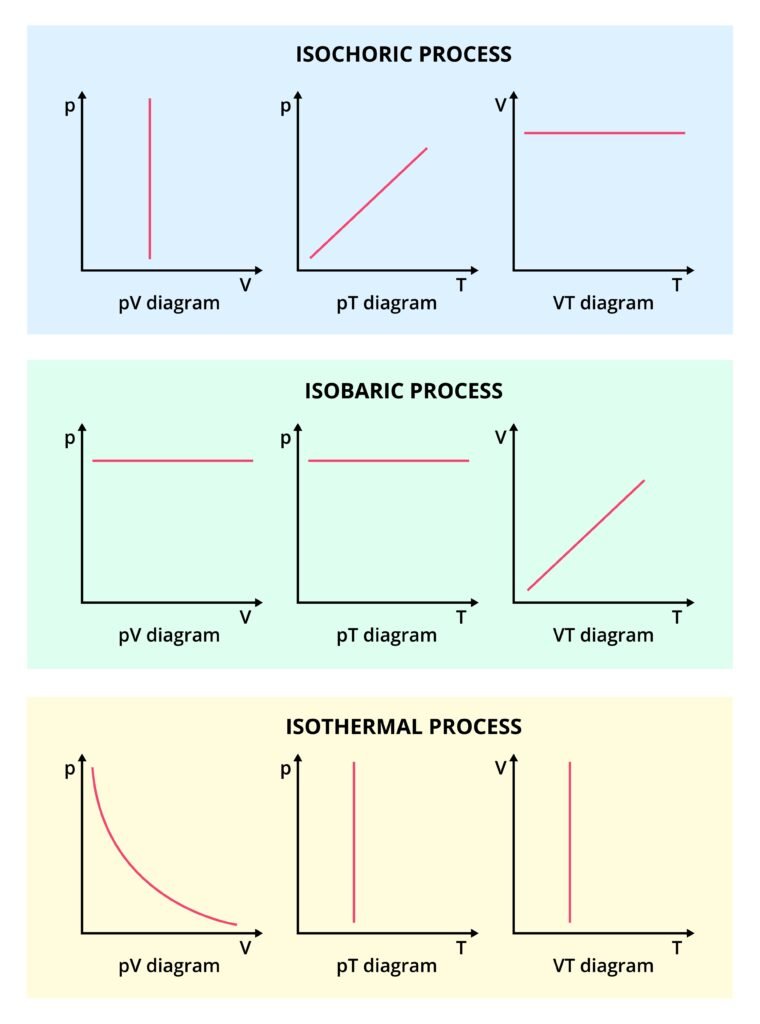
एक समतापीय प्रक्रिया (Isothermal process) के लिए —
(i) ΔT = 0
(ii) Δp = 0
(iii) q = 0
(iv) w = 0
🟢 उत्तर: (i) ΔT = 0
✏ व्याख्या:
समतापीय प्रक्रिया में तापमान स्थिर रहता है।
अतः ताप परिवर्तन (ΔT) = 0 होता है।
✔ दाब और कार्य बदल सकते हैं, लेकिन ताप स्थिर होता है।
🔵 प्रश्न 5.3:
सभी तत्वों की एन्थैल्पी उनकी संदर्भ अवस्था में होती है —
(i) शून्य
(ii) सत्य
(iii) ऋणात्मक
(iv) सभी तत्वों के लिए भिन्न
🟢 उत्तर: (i) शून्य
✏ व्याख्या:
किसी भी तत्व की मानक एन्थैल्पी (ΔH°) उसकी संदर्भ अवस्था (298 K, 1 atm) पर शून्य मानी जाती है।
✔ यह ऊष्मागतिक परिभाषा गणनाओं को सरल बनाती है।
🔵 प्रश्न 5.4:
मीथेन के दहन के लिए ΔU° = –X kJ mol⁻¹ है।
इस स्थिति में ΔH° होगा —
(i) = ΔU°
(ii) > ΔU°
(iii) < ΔU°
(iv) = 0
🟢 उत्तर: (ii) > ΔU°
✏ व्याख्या:
ऊष्मागतिक संबंध:
➡ ΔH = ΔU + Δn₍g₎RT
यदि उत्पादों के गैस मोल बढ़ते हैं, तो ΔH > ΔU।
✔ इसलिए यहाँ ΔH° > ΔU° होगा।
🔵 प्रश्न 5.5:
मीथेन के दहन की अभिक्रिया —
CH₄(g) + 2O₂(g) → CO₂(g) + 2H₂O(l)
दिए गए एन्थैल्पी मान:
CH₄(g): –74.8 kJ mol⁻¹
O₂(g): 0 kJ mol⁻¹
CO₂(g): –393.5 kJ mol⁻¹
H₂O(l): –285.8 kJ mol⁻¹
ऊष्मा परिवर्तन (ΔH°) ज्ञात कीजिए।
🟢 उत्तर:
✏ चरण 1:
उत्पादों की एन्थैल्पी = (–393.5) + 2(–285.8) = –393.5 – 571.6 = –965.1
✏ चरण 2:
अभिकारकों की एन्थैल्पी = (–74.8) + 2(0) = –74.8
✏ चरण 3:
ΔH° = उत्पाद – अभिकारक
= (–965.1) – (–74.8) = –890.3 kJ mol⁻¹
✔ अंतिम उत्तर: ΔH° = –890.3 kJ mol⁻¹ (ऊष्माक्षेपी प्रक्रिया)
🔵 प्रश्न 5.6:
एक अभिक्रिया A + B → C + D + q में q ऊष्मा निकलती है।
ऊष्मा परिवर्तन निर्भर करेगा —
(i) उच्च ताप पर
(ii) निम्न ताप पर
(iii) किसी भी ताप पर नहीं
(iv) केवल प्रारंभिक और अंतिम अवस्था पर
🟢 उत्तर: (iv) केवल प्रारंभिक और अंतिम अवस्था पर
✏ व्याख्या:
ऊष्मा परिवर्तन (ΔH) एक स्थिति फलन है।
इसका मान केवल अवस्था पर निर्भर करता है, पथ पर नहीं।
🔵 प्रश्न 5.7:
एक प्रक्रिया में 70 J ऊष्मा प्रणाली को दी गई तथा 394 J कार्य किया गया।
आंतरिक ऊर्जा का परिवर्तन ज्ञात कीजिए।
🟢 उत्तर:
✏ सूत्र: ΔU = q + w
q = +70 J (ऊष्मा प्राप्त)
w = –394 J (प्रणाली द्वारा कार्य)
ΔU = 70 – 394 = –324 J
✔ अंतिम उत्तर: ΔU = –324 J
(ऊर्जा घट रही है, इसलिए ऋणात्मक)
🔵 प्रश्न 5.8:
अभिक्रिया:
NH₄CN(s) → N₂(g) + CO(g) + 2H₂(g)
ΔH = –742.7 kJ mol⁻¹
ΔU = ? (298 K पर)
🟢 उत्तर:
✏ चरण 1:
Δn₍g₎ = (1 + 1 + 2) – 0 = 4
✏ चरण 2:
ΔH = ΔU + ΔnRT
ΔU = ΔH – ΔnRT
= –742.7 – (4 × 8.314 × 298 / 1000)
= –742.7 – 9.91 = –752.61 kJ mol⁻¹
✔ अंतिम उत्तर: ΔU = –752.61 kJ mol⁻¹
🔵 प्रश्न 5.9:
60 g एथेनॉल का ताप 35°C से 55°C तक बढ़ाने के लिए कितनी ऊष्मा चाहिए?
Cₚ(एथेनॉल) = 2.4 J g⁻¹ K⁻¹
🟢 उत्तर:
✏ सूत्र: q = m × Cₚ × ΔT
= 60 × 2.4 × (55 – 35)
= 60 × 2.4 × 20 = 2880 J
✔ अंतिम उत्तर: q = 2880 J = 2.88 kJ
🔵 प्रश्न 5.10:
10 g बर्फ को 0°C से –10°C पर ले जाने में एन्थैल्पी परिवर्तन ज्ञात कीजिए।
ΔₘH = 6.03 kJ mol⁻¹,
Cₚ(बर्फ) = 2.1 J g⁻¹ K⁻¹
🟢 उत्तर:
✏ चरण 1: बर्फ जमना (0°C पर) → ΔH₁ = –6.03 × 10/18 = –3.35 kJ
✏ चरण 2: ताप परिवर्तन → ΔH₂ = m × Cₚ × ΔT
= 10 × 2.1 × (–10) = –210 J = –0.21 kJ
✏ कुल ΔH = –3.35 – 0.21 = –3.56 kJ
✔ अंतिम उत्तर: ΔH = –3.56 kJ
🔵 प्रश्न 5.11:
CO₂(g) का मानक एन्थैल्पी निर्माण = –393.5 kJ mol⁻¹ है।
35.2 g CO₂ बनने पर ऊष्मा ज्ञात करें।
🟢 उत्तर:
✏ 1 mol CO₂ = 44 g → ऊष्मा = –393.5 kJ
✏ 35.2 g → ऊष्मा = –393.5 × 35.2 / 44 = –314.8 kJ
✔ अंतिम उत्तर: –314.8 kJ (ऊष्माक्षेपी)
🔵 प्रश्न 5.12:
अभिक्रिया :
CO(g) + ½O₂(g) → CO₂(g) , ΔH = –110 kJ mol⁻¹
N₂O(g) + 3CO(g) → N₂(g) + 3CO₂(g)
के लिए ΔH ज्ञात कीजिए।
🟢 उत्तर:
✏ चरण 1:
दी गई दूसरी अभिक्रिया में 3 mol CO से 3 mol CO₂ बनते हैं।
प्रत्येक CO → CO₂ के लिए ΔH = –110 kJ/mol
तो 3 mol के लिए ΔH = 3 × (–110) = –330 kJ
✏ चरण 2:
N₂O(g) → N₂(g) + ½O₂(g)
इसका उलटा लेने पर ΔH = +81 kJ mol⁻¹
✏ चरण 3:
कुल ΔH = (–330) + (+81) = –249 kJ
✔ अंतिम उत्तर: ΔH = –249 kJ (ऊष्माक्षेपी)
🔵 प्रश्न 5.13:
अभिक्रिया :
N₂(g) + 3H₂(g) → 2NH₃(g),
ΔH = –92.4 kJ mol⁻¹
1 mol NH₃ बनने पर ΔH = ?
🟢 उत्तर:
2 mol NH₃ बनने पर = –92.4 kJ
तो 1 mol के लिए = –92.4 ÷ 2 = –46.2 kJ
✔ अंतिम उत्तर: ΔH = –46.2 kJ mol⁻¹
🔵 प्रश्न 5.14:
CH₃OH(g) + 3/2 O₂(g) → CO₂(g) + 2H₂O(l)
के लिए ΔH ज्ञात कीजिए,
दिया गया:
ΔH°(CO₂) = –393 kJ mol⁻¹,
ΔH°(H₂O) = –286 kJ mol⁻¹,
ΔH°(CH₃OH) = –726 kJ mol⁻¹
🟢 उत्तर:
✏ उत्पादों की एन्थैल्पी = (–393) + 2(–286) = –393 – 572 = –965
✏ अभिकारकों की एन्थैल्पी = –726
ΔH = –965 – (–726) = –239 kJ
✔ अंतिम उत्तर: ΔH = –239 kJ mol⁻¹ (ऊष्माक्षेपी)
🔵 प्रश्न 5.15:
CCl₄(g) → C(g) + 4Cl(g)
के लिए ΔH ज्ञात कीजिए।
दिया गया:
ΔHf(CCl₄) = –135.5 kJ mol⁻¹
ΔHf(C) = 715.0 kJ mol⁻¹
ΔHf(Cl) = 242.0 kJ mol⁻¹
🟢 उत्तर:
✏ ΔH = [715 + 4(242)] – (–135.5)
= [715 + 968] + 135.5 = 1818.5 kJ mol⁻¹
✔ अंतिम उत्तर: ΔH = +1818.5 kJ mol⁻¹ (ऊष्माशोषी)
🔵 प्रश्न 5.16:
यदि किसी प्रक्रिया में ΔU = 0 है, तो ΔS क्या होगा?
🟢 उत्तर:
✏ ऊष्मागतिक संबंध:
ΔU = q + w
यदि ΔU = 0, तो q = –w
✔ अतः प्रणाली की कुल एंट्रॉपी (ΔS) शून्य होगी।
ΔS = 0
🔵 प्रश्न 5.17:
298 K पर अभिक्रिया:
2A + B → C
ΔH = 400 kJ mol⁻¹,
ΔS = 0.2 kJ mol⁻¹ K⁻¹
ΔG ज्ञात कीजिए।
🟢 उत्तर:
✏ सूत्र: ΔG = ΔH – TΔS
= 400 – (298 × 0.2)
= 400 – 59.6 = 340.4 kJ mol⁻¹
✔ अंतिम उत्तर: ΔG = +340.4 kJ mol⁻¹
(धनात्मक → अभिक्रिया स्वस्फूर्त नहीं)
🔵 प्रश्न 5.18:
अभिक्रिया : Cl₂(g) → 2Cl(g)
के लिए ΔS ज्ञात कीजिए।
🟢 उत्तर:
✏ गैस के मोल बढ़ने से अव्यवस्था बढ़ती है।
1 mol → 2 mol
✔ अतः ΔS = धनात्मक (+)
🔵 प्रश्न 5.19:
2A(g) + B(g) → 2D(g)
ΔU = –10.5 kJ, ΔS = –44.1 J K⁻¹
298 K पर ΔG ज्ञात कीजिए।
🟢 उत्तर:
✏ ΔG = ΔH – TΔS
ΔH ≈ ΔU (गैस मोल परिवर्तन नगण्य)
ΔG = –10.5 – 298(–0.0441)
= –10.5 + 13.15 = +2.65 kJ
✔ अंतिम उत्तर: ΔG = +2.65 kJ → अभिक्रिया स्वस्फूर्त नहीं।
🔵 प्रश्न 5.20:
300 K पर ΔS = 10 J K⁻¹, ΔH = 5 kJ
ΔG ज्ञात करें।
🟢 उत्तर:
ΔG = ΔH – TΔS
= 5 – 300 × 0.01 = 5 – 3 = 2 kJ
✔ अंतिम उत्तर: ΔG = +2 kJ → अस्वस्फूर्त अभिक्रिया
🔵 प्रश्न 5.21:
½ N₂(g) + ½ O₂(g) → NO(g), ΔH = 90 kJ mol⁻¹
NO(g) + ½ O₂(g) → NO₂(g), ΔH = –74 kJ mol⁻¹
NO₂(g) → ?
कुल ΔH ज्ञात कीजिए।
🟢 उत्तर:
पहली अभिक्रिया: +90 kJ
दूसरी: –74 kJ
कुल = +16 kJ
✔ अंतिम उत्तर: ΔH = +16 kJ mol⁻¹
🔵 प्रश्न 5.22:
1 mol H₂O(l) → H₂(g) + ½O₂(g)
के लिए ΔH ज्ञात करें।
दिया गया: ΔHf(H₂O) = –286 kJ mol⁻¹
🟢 उत्तर:
उल्टी अभिक्रिया के लिए ΔH = +286 kJ mol⁻¹
✔ अंतिम उत्तर: ΔH = +286 kJ mol⁻¹ (ऊष्माशोषी)
————————————————————————————————————————————————————————————————————————————
अन्य महत्वपूर्ण प्रश्न
(CBSE MODEL प्रश्न पत्र)
सिर्फ इसी पाठ से निर्मित CBSE MODEL प्रश्न पत्र।
खंड A — बहुविकल्पीय प्रश्न (Q1–Q16, प्रत्येक 1 अंक)
प्रश्न 1. ऊष्मागतिकी का प्रथम नियम किस रूप में व्यक्त किया जाता है?
ΔU = q − w
ΔU = q + w
ΔH = ΔU + PΔV
ΔG = ΔH − TΔS
Answer: 2
प्रश्न 2. एनथैल्पी (H) की परिभाषा है:
H = U − PV
H = U + PV
H = q − w
H = ΔE + ΔnRT
Answer: 2
प्रश्न 3. आइसोथर्मल प्रक्रिया में तापमान:
स्थिर
बढ़ता है
घटता है
अनन्त
Answer: 1
प्रश्न 4. ऐडियाबैटिक प्रक्रिया में किसका आदान–प्रदान नहीं होता?
कार्य
ऊष्मा
आयतन
दाब
Answer: 2
कथन–कारण हेतु विकल्प-कुंजी
कथन (A) एवं कारण (R) दोनों सत्य हैं तथा R, A का सही कारण है
कथन (A) एवं कारण (R) दोनों सत्य हैं परन्तु R, A का सही कारण नहीं
कथन (A) सत्य है परन्तु R असत्य
कथन (A) असत्य है परन्तु R सत्य
प्रश्न 5 (A/R).
कथन (A): ऊष्मागतिकी का प्रथम नियम ऊर्जा संरक्षण का नियम है।
कारण (R): ऊर्जा का न तो निर्माण होता है न विनाश, केवल रूपान्तरण होता है।
Answer: 1
प्रश्न 6. ΔU का चिह्न धनात्मक कब होता है?
जब तन्त्र ऊष्मा छोड़ता है
जब तन्त्र कार्य करता है
जब तन्त्र ऊर्जा प्राप्त करता है
जब ताप स्थिर रहता है
Answer: 3
प्रश्न 7. ऊष्मागतिकी का द्वितीय नियम मुख्यतः किससे सम्बन्धित है?
कार्य
एंट्रॉपी
दाब
एनथैल्पी
Answer: 2
प्रश्न 8. ΔH < 0 किस प्रकार की अभिक्रिया को सूचित करता है?
ऊष्माशोषी
ऊष्माक्षेपी
ऐडियाबैटिक
प्रतिवर्ती
Answer: 2
प्रश्न 9. मानक निर्माण एन्थैल्पी किसे कहते हैं?
1 mol यौगिक का निर्माण तत्वों से 298 K पर
1 g यौगिक का निर्माण
1 mol गैस का निर्माण
किसी भी मात्रा का निर्माण
Answer: 1
प्रश्न 10 (A/R).
कथन (A): स्वतःस्फूर्त अभिक्रिया में ΔG < 0 होता है।
कारण (R): गिब्स ऊर्जा का घटाव स्वतःस्फूर्तता की शर्त है।
Answer: 1
प्रश्न 11. एंट्रॉपी (S) किसका माप है?
ऊर्जा
कार्य
अव्यवस्था
एनथैल्पी
Answer: 3
प्रश्न 12. हेस का नियम किसके संरक्षण पर आधारित है?
द्रव्यमान
ऊर्जा
आवेश
दाब
Answer: 2
प्रश्न 13. ΔG = ΔH − TΔS समीकरण किसने दिया?
गिब्स
हेल्महोल्ट्ज़
रदरफोर्ड
डाल्टन
Answer: 1
प्रश्न 14. यदि ΔH = −40 kJ, ΔS = −100 J K⁻¹, T = 300 K, तो ΔG का मान kJ में होगा:
−10
−70
−10
+10
Answer: 4
प्रश्न 15 (A/R).
कथन (A): स्वतःस्फूर्त अभिक्रियाएँ प्रायः ऊष्माक्षेपी होती हैं।
कारण (R): ऊर्जा का उत्सर्जन स्थायित्व प्रदान करता है।
Answer: 2
प्रश्न 16. कार्य (w) का सूत्र आइसोथर्मल प्रसार के लिए है:
w = −PΔV
w = −nRT ln(V₂/V₁)
w = −ΔU
w = q + ΔU
Answer: 2
खंड B — अति लघु उत्तरीय प्रश्न (Q17–Q21, प्रत्येक 2 अंक)
प्रश्न 17. हेस का नियम लिखिए।
उत्तर:
🟦 कथन: किसी अभिक्रिया की एन्थैल्पी परिवर्तन प्रारम्भिक और अंतिम अवस्था पर निर्भर करता है, पथ पर नहीं।
🟩 परिणाम: ΔH कुल = ΔH₁ + ΔH₂ + …
प्रश्न 18. स्वतःस्फूर्तता की गिब्स शर्त लिखिए।
उत्तर:
🟦 यदि ΔG < 0 ⇒ अभिक्रिया स्वतःस्फूर्त। 🟩 यदि ΔG > 0 ⇒ अभिक्रिया अस्वतःस्फूर्त।
प्रश्न 19. एन्थैल्पी और आन्तरिक ऊर्जा में सम्बन्ध लिखिए।
उत्तर:
🟦 सूत्र: H = U + PV
🟩 अतः ΔH = ΔU + Δ(PV)
प्रश्न 20. एक मोल आदर्श गैस के लिए आइसोथर्मल प्रसार में कार्य का सूत्र लिखिए।
उत्तर:
🟦 w = −nRT ln(V₂/V₁)
🟩 n = 1 mol होने पर: w = −RT ln(V₂/V₁)
प्रश्न 21. एंट्रॉपी परिवर्तन (ΔS) का सूत्र लिखिए।
उत्तर:
🟦 ΔS = q_rev/T
🟩 यहाँ q_rev = प्रतिवर्ती ऊष्मा, T = ताप (K में)।
खंड C — लघु उत्तरीय प्रश्न (Q22–Q28, प्रत्येक 3 अंक)
प्रश्न 22. ऊष्मागतिकी का प्रथम नियम लिखिए और उसका महत्व समझाइए।
उत्तर:
🟦 प्रथम नियम: ΔU = q + w।
🟩 यह ऊर्जा संरक्षण का नियम है।
🟪 महत्व: किसी भी रासायनिक अथवा भौतिक प्रक्रिया में कुल ऊर्जा स्थिर रहती है।
प्रश्न 23. आइसोथर्मल तथा ऐडियाबैटिक प्रक्रिया में अन्तर बताइए।
उत्तर:
🟦 आइसोथर्मल: ताप स्थिर; q ≠ 0, ΔU = 0, w = −q।
🟩 ऐडियाबैटिक: q = 0; ΔU = w।
🟪 अन्तर: आइसोथर्मल में ऊष्मा आदान–प्रदान होता है, ऐडियाबैटिक में नहीं।
प्रश्न 24. 298 K पर H₂(g) + ½O₂(g) → H₂O(l) के लिए ΔH = −286 kJ mol⁻¹ है। इसका अर्थ समझाइए।
उत्तर:
🟦 1 mol द्रव जल बनने पर 286 kJ ऊष्मा मुक्त होती है।
🟩 यह ऊष्माक्षेपी प्रक्रिया है।
🟪 मानक निर्माण एन्थैल्पी = −286 kJ mol⁻¹।
प्रश्न 25. गिब्स समीकरण से स्वतःस्फूर्तता की शर्तें समझाइए।
उत्तर:
🟦 ΔG = ΔH − TΔS।
🟩 यदि ΔH < 0, ΔS > 0 ⇒ ΔG सदैव ऋणात्मक ⇒ स्वतःस्फूर्त।
🟪 यदि ΔH > 0, ΔS < 0 ⇒ स्वतःस्फूर्त नहीं।
प्रश्न 26. हेस का नियम प्रयोग करके C(graphite) से CO₂ के निर्माण की एन्थैल्पी ज्ञात करने का सिद्धान्त लिखिए।
उत्तर:
🟦 C + O₂ → CO₂ (ΔH = ?)
🟩 C + ½O₂ → CO (ΔH₁), CO + ½O₂ → CO₂ (ΔH₂)
🟪 कुल ΔH = ΔH₁ + ΔH₂।
प्रश्न 27. ऊष्माशोषी और ऊष्माक्षेपी अभिक्रियाओं में भेद उदाहरण सहित लिखिए।
उत्तर:
🟦 ऊष्माशोषी: ΔH > 0; उदाहरण – CaCO₃ → CaO + CO₂।
🟩 ऊष्माक्षेपी: ΔH < 0; उदाहरण – H₂ + Cl₂ → 2HCl।
🟪 अन्तर: पहली में ऊष्मा अवशोषित, दूसरी में उत्सर्जित।
प्रश्न 28. एक आदर्श गैस का 2 mol 300 K पर 10 L से 20 L तक आइसोथर्मल प्रसार करता है। R = 8.314 J mol⁻¹ K⁻¹। कार्य (w) ज्ञात कीजिए।
उत्तर:
🧮 w = −nRT ln(V₂/V₁)
= −2 × 8.314 × 300 × ln(20/10)
= −4988 J
✅ उत्तर: w ≈ −5.0 kJ
खंड D — प्रकरण आधारित प्रश्न (Q29–Q30, प्रत्येक 4 अंक)
प्रश्न 29.
“एक विद्यार्थी ने आदर्श गैस का आइसोथर्मल प्रसार 1 mol गैस के लिए 300 K पर 5 L से 10 L तक किया।”
(i) इस प्रक्रिया में आन्तरिक ऊर्जा परिवर्तन (ΔU) क्या होगा? (1)
(ii) कार्य (w) का सूत्र लिखिए। (1)
(iii) संख्यात्मक मान ज्ञात कीजिए। (2)
उत्तर:
🟦 (i) ΔU = 0 (आइसोथर्मल प्रक्रिया में)।
🟩 (ii) w = −nRT ln(V₂/V₁)।
🧮 (iii) w = −1 × 8.314 × 300 × ln(10/5)
= −2494 J × ln 2 ≈ −2494 × 0.693 = −1728 J ≈ −1.73 kJ
✅ उत्तर: w = −1.73 kJ
प्रश्न 30.
“किसी रासायनिक अभिक्रिया की एन्थैल्पी परिवर्तन −100 kJ तथा एंट्रॉपी परिवर्तन −200 J K⁻¹ mol⁻¹ है।”
(i) 298 K पर ΔG का मान ज्ञात कीजिए। (2)
(ii) यह अभिक्रिया स्वतःस्फूर्त है या नहीं? (1)
(iii) उच्च ताप पर इसका परिणाम क्या होगा? (1)
उत्तर:
🟦 (i) ΔG = ΔH − TΔS = (−100000 J) − 298 × (−200 J K⁻¹)
= −100000 + 59600 = −40400 J = −40.4 kJ
🟩 (ii) ΔG < 0 ⇒ अभिक्रिया स्वतःस्फूर्त।
🟪 (iii) उच्च ताप पर −TΔS धनात्मक बड़ा हो जाएगा ⇒ ΔG धनात्मक हो सकता है ⇒ स्वतःस्फूर्तता घटेगी।
खंड E — दीर्घ उत्तरीय प्रश्न (Q31–Q33, प्रत्येक 5 अंक)
प्रश्न 31.
ऊष्मागतिकी का द्वितीय नियम लिखिए और इसे एंट्रॉपी की दृष्टि से समझाइए।
उत्तर:
🟦 द्वितीय नियम: स्वतःस्फूर्त प्रक्रियाओं में ब्रह्माण्ड की एंट्रॉपी (ΔS_total) सदैव बढ़ती है।
🟩 गणितीय रूप: ΔS_universe = ΔS_system + ΔS_surroundings > 0।
🟪 उदाहरण: ऊष्मा का स्वतः उच्च ताप से निम्न ताप की ओर प्रवाह।
✅ निष्कर्ष: द्वितीय नियम ऊर्जा रूपान्तरण की दिशा व सम्भाव्यता निर्धारित करता है।
या
हेल्महोल्ट्ज़ मुक्त ऊर्जा (A = U − TS) की संकल्पना लिखिए और इसकी स्वतःस्फूर्तता की शर्त बताइए।
प्रश्न 32.
298 K पर N₂(g) + 3H₂(g) → 2NH₃(g) के लिए ΔH = −92 kJ mol⁻¹ और ΔS = −198 J K⁻¹ mol⁻¹ है। ΔG की गणना कीजिए और स्वतःस्फूर्तता पर टिप्पणी करें।
उत्तर:
🧮 ΔG = ΔH − TΔS = (−92000 J) − 298 × (−198 J K⁻¹)
= −92000 + 59000 = −33000 J = −33 kJ
🟦 ΔG < 0 ⇒ अभिक्रिया स्वतःस्फूर्त।
✅ परन्तु ΔS ऋणात्मक होने से उच्च ताप पर स्वतःस्फूर्तता घट सकती है।
या
“गिब्स ऊर्जा” की संकल्पना लिखिए और बताइए कि यह स्वतःस्फूर्तता का मानदण्ड क्यों है।
प्रश्न 33.
हेस के नियम की सहायता से C(graphite) से CO₂ की निर्माण एन्थैल्पी की गणना समझाइए।
उत्तर:
🟦 अभिक्रियाएँ:
C + ½O₂ → CO (ΔH₁)
CO + ½O₂ → CO₂ (ΔH₂)
🟩 हेस का नियम: ΔH_total = ΔH₁ + ΔH₂
🟪 अतः C + O₂ → CO₂ की एन्थैल्पी = ΔH₁ + ΔH₂।
✅ हेस के नियम से किसी भी जटिल अभिक्रिया की एन्थैल्पी ज्ञात की जा सकती है।
या
“मानक निर्माण एन्थैल्पी” की परिभाषा दीजिए और एक संख्यात्मक उदाहरण द्वारा समझाइए।
————————————————————————————————————————————————————————————————————————————
