Class 11 : Chemistry (In Hindi) – Lesson 1. रसायन विज्ञान की कुछ मूल अवधारणाएँ
पाठ का विश्लेषण एवं विवेचन
💠 💡 प्रस्तावना (Introduction):
📌 रसायन विज्ञान (Chemistry) पदार्थ के संघटन, उसकी संरचना, उसके गुण, और उसमें होने वाले परिवर्तनों का अध्ययन है।
📌 यह विषय जीवन के प्रत्येक क्षेत्र में उपस्थित है — भोजन, दवाइयाँ, कपड़े, ईंधन, और पर्यावरण तक।
💠 💡 पदार्थ और उसकी अवस्थाएँ (Matter and its States):
📌 पदार्थ वह है जिसका द्रव्यमान होता है और जो स्थान घेरता है।
📌 तीन मुख्य अवस्थाएँ होती हैं:
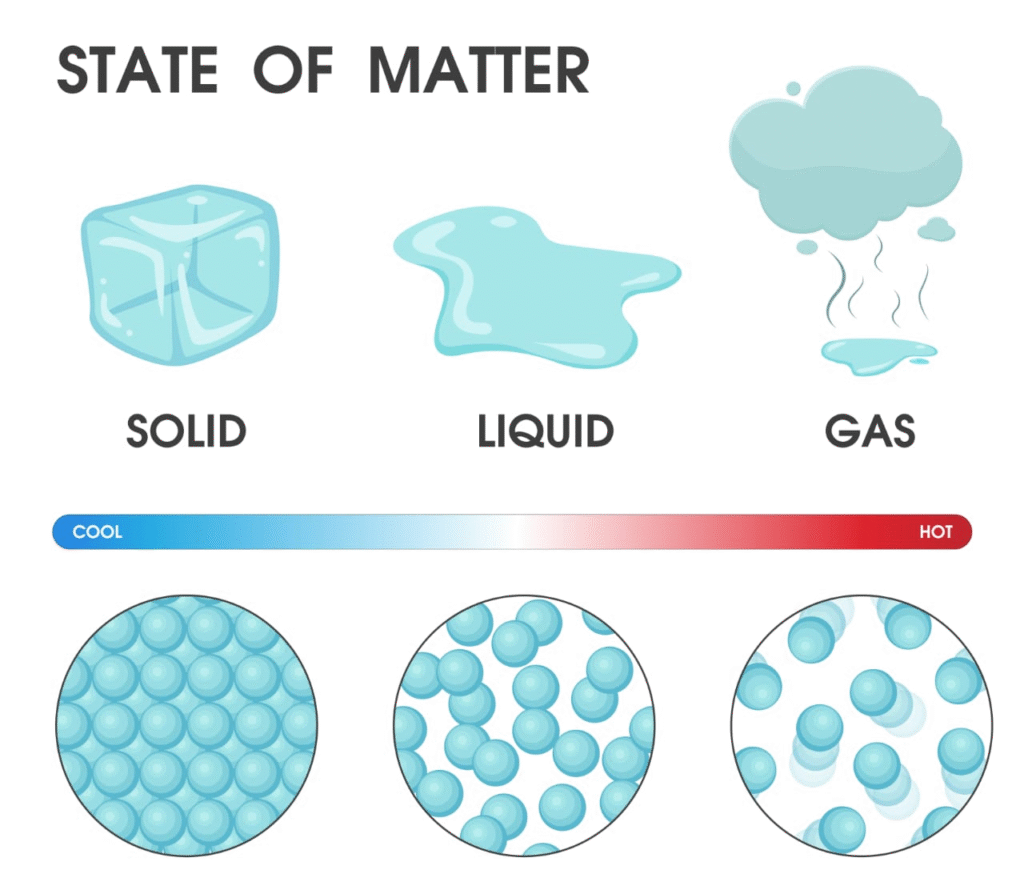
📌 ठोस (Solid)
📌 द्रव (Liquid)
📌 गैस (Gas)
💠 💡 पदार्थ की वर्गीकरण (Classification of Matter):
📌 पदार्थ को शुद्ध पदार्थ और मिश्रण में बाँटा जाता है।
📌 शुद्ध पदार्थ: तत्त्व (elements) और यौगिक (compounds)
📌 मिश्रण: समांगी (homogeneous) और विषमांगी (heterogeneous)
💠 💡 भौतिक और रासायनिक गुण (Physical and Chemical Properties):
📌 भौतिक गुण वे हैं जो पदार्थ की पहचान को बदले बिना मापे जा सकते हैं (जैसे रंग, घनत्व, गलनांक)।
📌 रासायनिक गुण वे हैं जो पदार्थ की संरचना में परिवर्तन लाते हैं (जैसे ज्वलनशीलता, अभिक्रियाशीलता)।
💠 💡 मापन की आवश्यकता (Need for Measurement):
📌 रसायन विज्ञान में सटीक मापन अत्यंत आवश्यक है।
📌 मात्रा मापन के लिए अंतरराष्ट्रीय मात्रक प्रणाली (SI) अपनाई गई है।
📌 SI मात्रक:
📌 द्रव्यमान – किलोग्राम (kg)
📌 लंबाई – मीटर (m)
📌 समय – सेकंड (s)
📌 तापमान – केल्विन (K)
📌 द्रव्य की मात्रा – मोल (mol)
💠 💡 महत्वपूर्ण SI उपसर्ग (SI Prefixes):
📌 किलो (k) = 10³
📌 मिली (m) = 10⁻³
📌 माइक्रो (μ) = 10⁻⁶
📌 नैनो (n) = 10⁻⁹
💠 💡 मापन में त्रुटियाँ (Errors in Measurement):
📌 त्रुटियाँ दो प्रकार की होती हैं:
📌 यादृच्छिक त्रुटि (Random Error)
📌 प्रणालीगत त्रुटि (Systematic Error)
📌 औसत विचलन और सापेक्ष विचलन का उपयोग करके माप की विश्वसनीयता ज्ञात की जाती है।
💠 💡 महत्वपूर्ण रासायनिक अवधारणाएँ (Basic Chemical Concepts):
📌 परमाणु (Atoms): पदार्थ के अत्यंत सूक्ष्म कण।
📌 अणु (Molecules): दो या अधिक परमाणुओं से बने कण।
📌 आयन्स (Ions): धनावेशित कण – कैटायन (+) और एनायन (–)
💠 💡 रासायनिक अभिक्रियाएँ (Chemical Reactions):
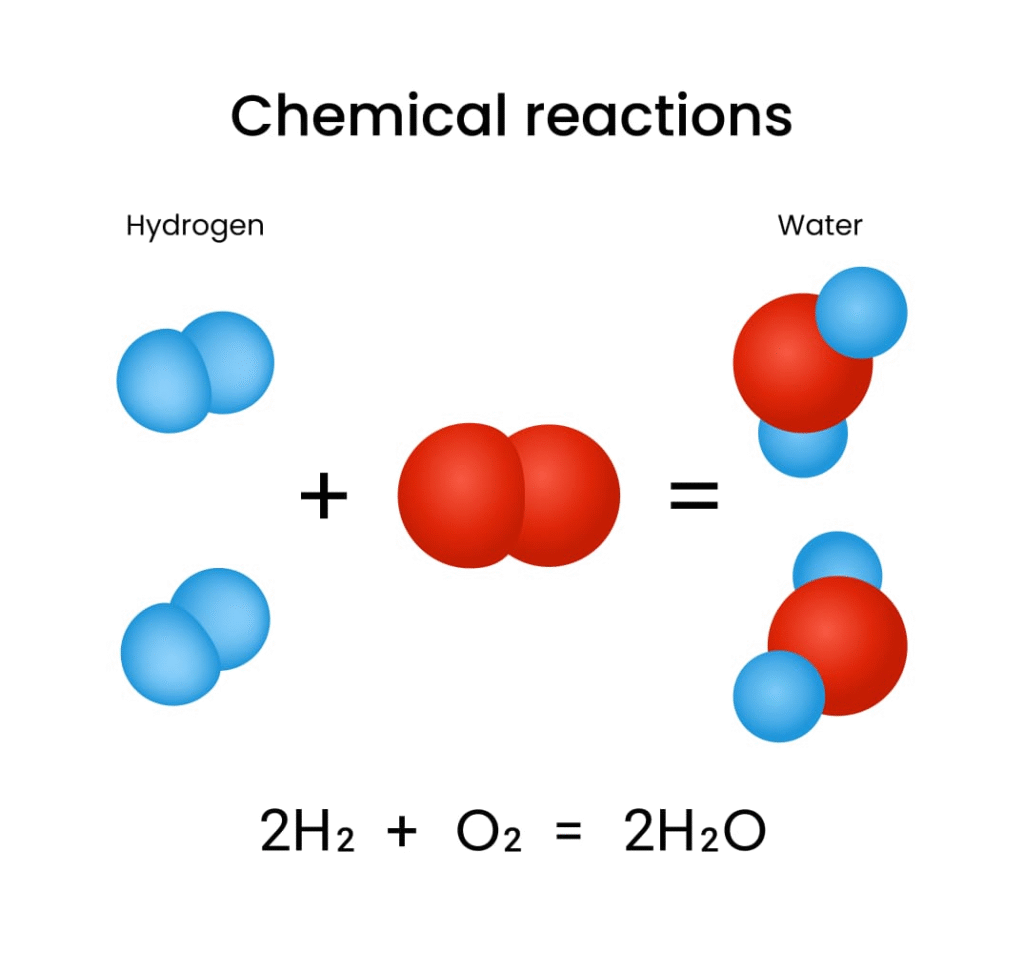
📌 अभिकारकों (Reactants) के मिलने से उत्पाद (Products) बनते हैं।
📌 रासायनिक समीकरण संतुलित होना चाहिए।
📌 द्रव्यमान संरक्षण का नियम लागू होता है – कुल द्रव्यमान पहले और बाद में समान।
💠 💡 रासायनिक सूत्र और नामकरण (Formulas and Nomenclature):
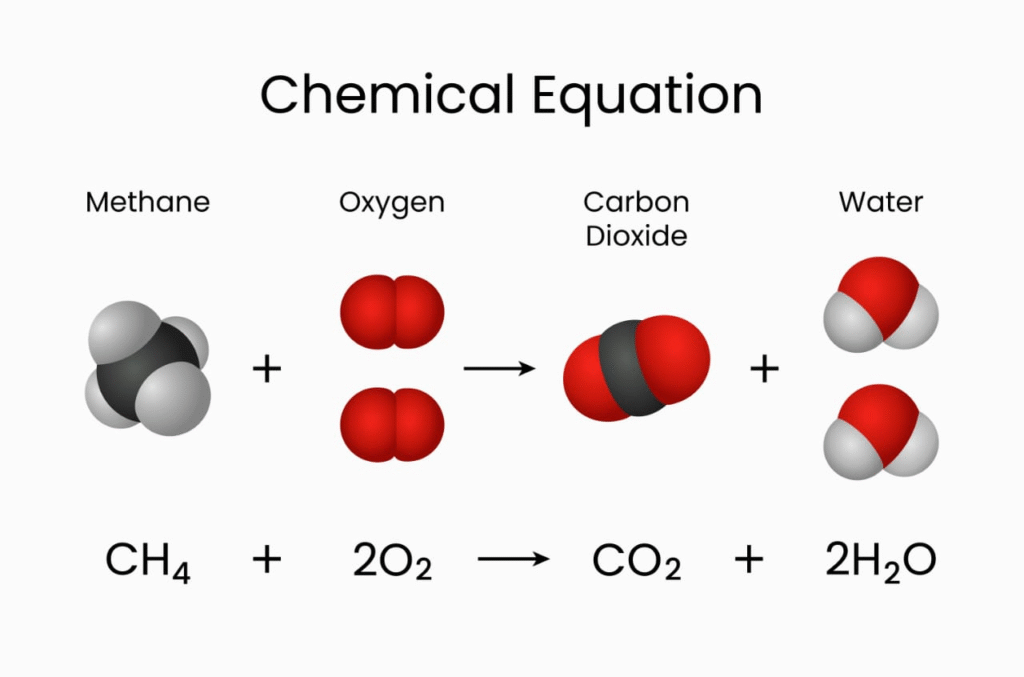
📌 अणु सूत्र एक अणु में उपस्थित तत्त्वों की संख्या को दर्शाते हैं।
📌 नामकरण IUPAC पद्धति से किया जाता है।
उदाहरण: H₂O – जल, CO₂ – कार्बन डाइऑक्साइड
💠 💡 मोल संकल्पना (The Mole Concept):
🟢 मोल (Mole):
📌 किसी पदार्थ की वह मात्रा जिसमें 6.022 × 10²³ कण (परमाणु/अणु/आयन) हों।
📌 इसे एवोगैड्रो संख्या कहते हैं।
📌 उदाहरण:
📌 1 मोल H₂O = 6.022 × 10²³ अणु
📌 1 मोल Na = 23 ग्राम
📌 द्रव्यमान (Mass) = मोल × मोलर द्रव्यमान
📌 कणों की संख्या = मोल × 6.022 × 10²³
💠 💡 द्रव्यमान और मात्रा में संबंध (Mass-Volume Relations):
📌 1 मोल गैस का आयतन सामान्य ताप और दाब (STP) पर 22.4 L होता है।
📌 द्रव्यमान, आयतन और मोल के बीच सूत्र बनाए जाते हैं:
📌 उदाहरण:
📌 Volume = Moles × 22.4 L (at STP)
💠 💡 सांद्रता मापन (Concentration Units):
📌 घोल में विलेय की मात्रा मापने के लिए:
📌 सामान्य एकक:
📌 Molarity (M) = मोल/लीटर
📌 Molality (m) = मोल/किलोग्राम विलायक
📌 Mole fraction = मोल अंश
💠 💡 स्टॉयकियोमेट्री (Stoichiometry):
📌 संतुलित समीकरण के आधार पर यह अनुमान लगाना कि कितनी मात्रा में अभिकारक या उत्पाद लगेगा/बनेगा।
📌 उदाहरण:
📌 H₂ + Cl₂ → 2HCl
📌 1 मोल H₂ और 1 मोल Cl₂ से 2 मोल HCl बनेंगे।
💠 💡 सीमित अभिकारक (Limiting Reagent):
📌 वह अभिकारक जो पहले समाप्त हो जाता है और अभिक्रिया को रोक देता है।
💠 💡 द्रव्यमान संरक्षण का नियम (Law of Conservation of Mass):
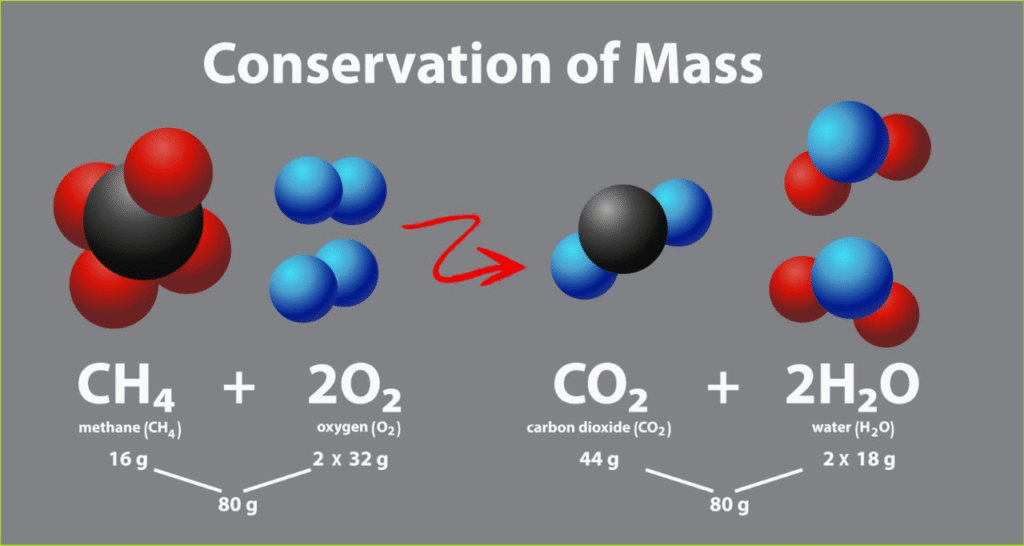
📌 रासायनिक अभिक्रियाओं में कुल द्रव्यमान अपरिवर्तित रहता है।
📌 Lavoisier द्वारा प्रतिपादित।
💠 💡 अणुसूत्र निर्धारण (Determination of Molecular Formula):
📌 प्रयोग से प्राप्त अनुपातिक सूत्र (Empirical Formula) को मोलर द्रव्यमान से गुणा करके अणुसूत्र (Molecular Formula) प्राप्त किया जाता है।
📌 सूत्र:
📌 n = मोलर द्रव्यमान / अनुपातिक सूत्र द्रव्यमान
📌 अणुसूत्र = (अनुपातिक सूत्र) × n
💠 💡 अति-महत्वपूर्ण सूत्र (Important Formulas Recap):
📌 n = m / M
📌 संख्या = मोल × 6.022 × 10²³
📌 घनत्व = द्रव्यमान / आयतन
📌 Molarity = मोल / लीटर
📌 Molality = मोल / किलोग्राम
📌 गैसीय आयतन = मोल × 22.4 L (STP)
🟢 📘 निष्कर्ष:
📌 यह अध्याय रसायन विज्ञान की बुनियाद रखता है।
📌 मोल अवधारणा, SI प्रणाली, मापन, रासायनिक समीकरण और सूत्रों की समझ के बिना रसायन विज्ञान की गहराई में नहीं जाया जा सकता।
————————————————————————————————————————————————————————————————————————————
पाठ्यपुस्तक के प्रश्न
💡 🔆 Q1:
रसायन विज्ञान किसे कहते हैं?
✅ 🟢 उत्तर:
📌 रसायन विज्ञान वह विज्ञान है जिसमें पदार्थ की संरचना, संघटन, गुणधर्म और उसमें होने वाले परिवर्तन तथा उनके नियमों का अध्ययन किया जाता है।
📌 यह जीवित और निर्जीव दोनों पदार्थों पर लागू होता है।
💡 🔆 Q2:
मात्रक प्रणाली क्या है?
✅ 🟢 उत्तर:
📌 मात्रक प्रणाली वह मानक प्रणाली है जिससे भौतिक राशियों को मापा जाता है।
📌 अंतरराष्ट्रीय मात्रक प्रणाली (SI) विश्व की सर्वाधिक स्वीकृत प्रणाली है।
📌 उदाहरण:
📌 लंबाई – मीटर (m)
📌 द्रव्यमान – किलोग्राम (kg)
📌 समय – सेकंड (s)
📌 तापमान – केल्विन (K)
📌 द्रव्य की मात्रा – मोल (mol)
💡 🔆 Q3:
एक मोल क्या होता है?
✅ 🟢 उत्तर:
📌 एक मोल किसी भी पदार्थ की वह मात्रा होती है जिसमें 6.022 × 10²³ कण (परमाणु, अणु या आयन) होते हैं।
📌 इसे एवोगैड्रो संख्या कहा जाता है।
📌 उदाहरण:
📌 1 मोल H₂O = 6.022 × 10²³ अणु
📌 1 मोल Na = 23 ग्राम
💡 🔆 Q4:
सांद्रता की मोलरता और मोललता में क्या अंतर है?
✅ 🟢 उत्तर:
📌 मोलरता (M):
📌 मोलरता = मोल / लीटर विलयन
📌 मोललता (m):
📌 मोललता = मोल / किलोग्राम विलायक
📌 अंतर: मोलरता आयतन पर निर्भर करती है, जबकि मोललता द्रव्यमान पर आधारित होती है।
💡 🔆 Q5:
1 मोल ऑक्सीजन अणु का द्रव्यमान ज्ञात कीजिए।
✅ 🟢 उत्तर:
📌 ऑक्सीजन अणु (O₂) का मोलर द्रव्यमान = 16 × 2 = 32 g/mol
📌 अतः 1 मोल O₂ का द्रव्यमान = 32 ग्राम
💡 🔆 Q6:
मोल की संख्या निकालने का सूत्र बताइए।
✅ 🟢 उत्तर:
📌 सूत्र:
📌 मोल = दिए गए द्रव्यमान / मोलर द्रव्यमान
📌 n = m / M
📌 उदाहरण:
📌 यदि 46 ग्राम NaCl हो और उसका मोलर द्रव्यमान 58.5 g/mol हो
📌 n = 46 / 58.5 = 0.786 मोल
💡 🔆 Q7:
1 मोल किसी भी गैस का STP पर आयतन कितना होता है?
✅ 🟢 उत्तर:
📌 सामान्य ताप और दाब (STP) पर 1 मोल किसी भी आदर्श गैस का आयतन होता है:
📌 22.4 लीटर
💡 🔆 Q8:
घनत्व कैसे निकालते हैं?
✅ 🟢 उत्तर:
📌 घनत्व (Density) = द्रव्यमान / आयतन
📌 SI मात्रक: kg/m³ या g/cm³
📌 उदाहरण:
📌 द्रव्यमान = 50 g, आयतन = 25 cm³
📌 घनत्व = 50 / 25 = 2 g/cm³
💡 🔆 Q9:
STP पर 2 मोल CO₂ गैस का आयतन कितना होगा?
✅ 🟢 उत्तर:
📌 1 मोल गैस का आयतन = 22.4 L
📌 अतः 2 मोल CO₂ का आयतन = 2 × 22.4 = 44.8 लीटर
💡 🔆 Q10:
कणों की संख्या निकालने का सूत्र बताइए।
✅ 🟢 उत्तर:
📌 कणों की संख्या = मोल × एवोगैड्रो संख्या
📌 N = n × 6.022 × 10²³
📌 उदाहरण:
📌 यदि n = 2 मोल,
📌 तो N = 2 × 6.022 × 10²³ = 1.2044 × 10²⁴ कण
💡 🔆 Q11:
60 ग्राम CH₄ में मोल की संख्या कितनी होगी?
(मोलर द्रव्यमान CH₄ = 16 g/mol)
🟢 उत्तर:
📌 मोल = दिए गए द्रव्यमान / मोलर द्रव्यमान
📌 = 60 / 16 = 3.75 मोल
💡 🔆 Q12:
1.2044 × 10²⁴ अणु CH₄ में कितने मोल होंगे?
🟢 उत्तर:
📌 मोल = कणों की संख्या / एवोगैड्रो संख्या
📌 = (1.2044 × 10²⁴) / (6.022 × 10²³) = 2 मोल
💡 🔆 Q13:
100 ग्राम CaCO₃ में कितने मोल होंगे?
(मोलर द्रव्यमान = 40 + 12 + (16×3) = 100 g/mol)
🟢 उत्तर:
📌 मोल = 100 / 100 = 1 मोल
💡 🔆 Q14:
46 ग्राम C₂H₆O में कणों की संख्या बताइए।
(मोलर द्रव्यमान = 46 g/mol)
🟢 उत्तर:
📌 मोल = 46 / 46 = 1 मोल
📌 कणों की संख्या = 1 × 6.022 × 10²³ = 6.022 × 10²³ अणु
💡 🔆 Q15:
1 मोल SO₂ में परमाणुओं की संख्या कितनी होगी?
🟢 उत्तर:
📌 1 SO₂ अणु = 1 S + 2 O = 3 परमाणु
📌 1 मोल SO₂ = 6.022 × 10²³ अणु
📌 परमाणुओं की कुल संख्या = 3 × 6.022 × 10²³ = 1.8066 × 10²⁴ परमाणु
💡 🔆 Q16:
विलयन की मोलरता क्या है यदि 5 मोल NaCl को 2 लीटर पानी में घोला जाए?
🟢 उत्तर:
📌 मोलरता = मोल / लीटर = 5 / 2 = 2.5 M
💡 🔆 Q17:
CO₂ के 0.5 मोल में अणुओं की संख्या कितनी होगी?
🟢 उत्तर:
📌 N = n × Nₐ = 0.5 × 6.022 × 10²³
📌 = 3.011 × 10²³ अणु
💡 🔆 Q18:
यदि 10 ग्राम H₂O हो, तो मोल की संख्या ज्ञात कीजिए।
(मोलर द्रव्यमान = 18 g/mol)
🟢 उत्तर:
📌 मोल = 10 / 18 = 0.555 मोल (लगभग)
💡 🔆 Q19:
0.2 मोल Na₂CO₃ में कितने Na⁺ आयन होंगे?
🟢 उत्तर:
📌 1 Na₂CO₃ में 2 Na⁺ आयन
📌 0.2 मोल × 2 × 6.022 × 10²³ = 2.409 × 10²³ Na⁺ आयन
💡 🔆 Q20:
यदि घनत्व 2 g/cm³ और द्रव्यमान 100 g हो, तो आयतन कितना होगा?
🟢 उत्तर:
📌 आयतन = द्रव्यमान / घनत्व = 100 / 2 = 50 cm³
💡 🔆 Q21:
CH₄ के 0.1 मोल में हाइड्रोजन परमाणुओं की संख्या बताइए।
🟢 उत्तर:
📌 1 CH₄ = 4 H
📌 H की संख्या = 4 × 0.1 × 6.022 × 10²³ = 2.409 × 10²³ परमाणु
💡 🔆 Q22:
यदि विलायक 1.5 kg और सोल्यूट के मोल 0.5 हो, तो मोललता ज्ञात कीजिए।
🟢 उत्तर:
📌 मोललता = मोल / विलायक का किग्रा = 0.5 / 1.5 = 0.333 mol/kg
💡 🔆 Q23:
10 ग्राम NaOH का मोलर द्रव्यमान 40 g/mol हो, तो उसमें मोल की संख्या क्या होगी?
🟢 उत्तर:
📌 मोल = 10 / 40 = 0.25 मोल
💡 🔆 Q24:
N₂ के 3 मोल में N परमाणुओं की संख्या बताइए।
🟢 उत्तर:
📌 1 N₂ = 2 N
📌 3 मोल × 2 × 6.022 × 10²³ = 3.613 × 10²⁴ परमाणु
💡 🔆 Q25:
6.022 × 10²³ कणों की संख्या वाले किसी पदार्थ का द्रव्यमान 98 g है, उसका मोलर द्रव्यमान क्या होगा?
🟢 उत्तर:
📌 6.022 × 10²³ कण = 1 मोल
📌 द्रव्यमान = 98 g
📌 अतः मोलर द्रव्यमान = 98 g/mol
————————————————————————————————————————————————————————————————————————————
अन्य महत्वपूर्ण प्रश्न
(CBSE MODEL प्रश्न पत्र)
सिर्फ इसी पाठ से निर्मित CBSE MODEL प्रश्न पत्र।
🔶 प्रश्न 1. एक मोल किसी पदार्थ की वह मात्रा है जिसमें अवोगाद्रो संख्या के बराबर कण होते हैं। अवोगाद्रो संख्या का मान है:
(A) 6.022 × 10²²
(B) 6.022 × 10²³
(C) 6.022 × 10²⁴
(D) 6.022 × 10²⁰
उत्तर: (B) 6.022 × 10²³
🔶 प्रश्न 2. 22.4 लीटर गैस का द्रव्यमान 44 ग्राम है, यह गैस कौन-सी हो सकती है?
(A) ऑक्सीजन
(B) कार्बन डाइऑक्साइड
(C) नाइट्रोजन
(D) हाइड्रोजन
उत्तर: (B) कार्बन डाइऑक्साइड
🔶 प्रश्न 3. निम्नलिखित में से कौन-सा मात्रक “मोलर संकेन्द्रण” के लिए प्रयुक्त होता है?
(A) mol
(B) mol/kg
(C) mol/L
(D) mol/m³
उत्तर: (C) mol/L
🔶 प्रश्न 4. 1 एमयू (amu) का मान होता है:
(A) 1.66 × 10⁻²⁷ kg
(B) 1.66 × 10⁻²⁴ g
(C) 1.66 × 10⁻²³ kg
(D) 1.66 × 10⁻²⁶ g
उत्तर: (A) 1.66 × 10⁻²⁷ kg
🔶 प्रश्न 5. एक अणु की द्रव्यमान संख्या होती है:
(A) प्रोटॉन + न्यूट्रॉन
(B) प्रोटॉन + इलेक्ट्रॉन
(C) न्यूट्रॉन + इलेक्ट्रॉन
(D) केवल न्यूट्रॉन
उत्तर: (A) प्रोटॉन + न्यूट्रॉन
🔶 प्रश्न 6. संतुलित रासायनिक समीकरण किसका पालन करता है?
(A) द्रव्यमान संरक्षण का नियम
(B) ऊर्जा संरक्षण का नियम
(C) गैस के नियम
(D) मात्रा संरक्षण का नियम
उत्तर: (A) द्रव्यमान संरक्षण का नियम
🔶 प्रश्न 7. 5.6 लीटर ऑक्सीजन गैस (STP पर) में उपस्थित अणुओं की संख्या क्या होगी?
(A) 3.011 × 10²³
(B) 1.505 × 10²³
(C) 6.022 × 10²³
(D) 2.011 × 10²³
उत्तर: (A) 3.011 × 10²³
🔶 प्रश्न 8. Assertion (A): 1 मोल किसी भी गैस का आयतन STP पर 22.4 L होता है।
Reason (R): सभी गैसें समान ताप और दाब पर समान आयतन रखती हैं।
(A) A और R दोनों सही हैं तथा R, A की सही व्याख्या है।
(B) A और R दोनों सही हैं, परंतु R, A की सही व्याख्या नहीं है।
(C) A सही है पर R गलत है।
(D) A गलत है पर R सही है।
उत्तर: (A)
🔶 प्रश्न 9. Assertion (A): द्रव्यमान संख्याएँ एक जैसे समस्थानिकों में समान होती हैं।
Reason (R): समस्थानिकों में प्रोटॉन की संख्या समान होती है।
(A) A और R दोनों सही हैं तथा R, A की सही व्याख्या है।
(B) A और R दोनों सही हैं, परंतु R, A की सही व्याख्या नहीं है।
(C) A सही है पर R गलत है।
(D) A गलत है पर R सही है।
उत्तर: (D)
🔶 प्रश्न 10. एक मोल पानी में उपस्थित अणुओं की संख्या क्या है?
(A) 3.011 × 10²³
(B) 6.022 × 10²³
(C) 1.204 × 10²⁴
(D) 1.806 × 10²⁴
उत्तर: (B) 6.022 × 10²³
🔶 प्रश्न 11. 1 मोल सल्फ्यूरिक अम्ल (H₂SO₄) में कितने ग्राम उपस्थित होंगे?
(A) 98 g
(B) 49 g
(C) 100 g
(D) 94.5 g
उत्तर: (A) 98 g
🔶 प्रश्न 12. 16 ग्राम ऑक्सीजन गैस में कितने मोल होंगे? (O = 16)
(A) 1
(B) 0.5
(C) 2
(D) 1.5
उत्तर: (B) 0.5
🔶 प्रश्न 13. गैसों का आयतन STP पर किस पर निर्भर करता है?
(A) द्रव्यमान
(B) घनत्व
(C) अणु संख्या
(D) कोई नहीं
उत्तर: (C) अणु संख्या
🔶 प्रश्न 14. एक रासायनिक प्रतिक्रिया में उत्पाद का द्रव्यमान अभिकर्मकों के द्रव्यमान से कम है, इसका अर्थ है:
(A) अभिक्रिया पूर्ण नहीं हुई
(B) ऊर्जा का क्षय हुआ
(C) द्रव्यमान संरक्षण नहीं हुआ
(D) उत्पाद गैस रूप में निकल गई
उत्तर: (D) उत्पाद गैस रूप में निकल गई
🔶 प्रश्न 15. एक मोल मिथेन (CH₄) में उपस्थित हाइड्रोजन परमाणुओं की संख्या है:
(A) 6.022 × 10²³
(B) 2.408 × 10²⁴
(C) 1.505 × 10²⁴
(D) 3.011 × 10²⁴
उत्तर: (B) 2.408 × 10²⁴
🔶 प्रश्न 16. निम्न में से कौन-सी राशि एक मौलिक राशि नहीं है?
(A) लंबाई
(B) तापमान
(C) घनत्व
(D) समय
उत्तर: (C) घनत्व
🔶 प्रश्न 17. 0.5 मोल NaCl में कितने Na⁺ आयन होंगे?
(A) 3.011 × 10²³
(B) 6.022 × 10²³
(C) 1.204 × 10²⁴
(D) 2.011 × 10²³
उत्तर: (A) 3.011 × 10²³
🔶 प्रश्न 18. निम्नलिखित में से किसका SI मात्रक गलत है?
(A) द्रव्यमान – किलोग्राम
(B) तापमान – केल्विन
(C) पदार्थ की मात्रा – मोल
(D) दाब – ग्राम प्रति लीटर
उत्तर: (D) दाब – ग्राम प्रति लीटर
🔷 प्रश्न 19. एक यौगिक का अणुभार 92 u है। यदि 23 ग्राम उस यौगिक के नमूने में उपस्थित हों, तो उसमें कितने मोल होंगे?
📌 उत्तर:
मोल = दिए गए द्रव्यमान / अणुभार
= 23 g / 92 g/mol
= 0.25 mol
🔷 प्रश्न 20. किसी पदार्थ का घनत्व 1.25 g/cm³ है। उसका SI मात्रक में मान क्या होगा?
📌 उत्तर:
1 g/cm³ = 1000 kg/m³
⇒ 1.25 g/cm³ = 1.25 × 1000 = 1250 kg/m³
🔷 प्रश्न 21. यदि 0.5 मोल नाइट्रोजन अणु (N₂) हो, तो उसमें कुल कितने परमाणु होंगे?
📌 उत्तर:
1 मोल N₂ = 6.022 × 10²³ अणु
0.5 मोल N₂ = 0.5 × 6.022 × 10²³ = 3.011 × 10²³ अणु
परंतु प्रत्येक अणु में 2 परमाणु होते हैं,
तो कुल परमाणु = 2 × 3.011 × 10²³ = 6.022 × 10²³ परमाणु
🔷 प्रश्न 22. यदि कोई पदार्थ 5 × 10²² अणुओं से बना है, तो उसमें कितने मोल होंगे?
📌 उत्तर:
मोल = अणुओं की संख्या / अवोगाद्रो संख्या
= (5 × 10²²) / (6.022 × 10²³)
≈ 0.083 mol
🔷 प्रश्न 23. 5.6 लीटर अमोनिया गैस (STP पर) में उपस्थित अणुओं की संख्या ज्ञात कीजिए।
📌 उत्तर:
STP पर 1 मोल गैस = 22.4 L
⇒ मोल = 5.6 / 22.4 = 0.25 mol
अब, अणु = 0.25 × 6.022 × 10²³
= 1.5055 × 10²³ अणु
📘 Section C: (प्रत्येक 3 अंक)
🔷 प्रश्न 24. 46 ग्राम Na का मोलसंख्या तथा कणों की संख्या ज्ञात कीजिए। (Na = 23)
📌 उत्तर:
मोल = 46 / 23 = 2 mol
कण = 2 × 6.022 × 10²³
= 1.2044 × 10²⁴ Na परमाणु
🔷 प्रश्न 25. CO₂ का द्रव्यमान 8.8 ग्राम है। इसमें उपस्थित C और O अणुओं की संख्या ज्ञात कीजिए। (C=12, O=16)
📌 उत्तर:
CO₂ का मोलर द्रव्यमान = 12 + (16×2) = 44 g/mol
मोल = 8.8 / 44 = 0.2 mol
⇒ CO₂ अणु = 0.2 × 6.022 × 10²³ = 1.204 × 10²³
1 CO₂ में 1 C और 2 O होते हैं
⇒ C = 1.204 × 10²³
O = 2 × 1.204 × 10²³ = 2.408 × 10²³
🔷 प्रश्न 26. एक मिश्रण में 10 ग्राम हाइड्रोजन और 80 ग्राम ऑक्सीजन है। प्रतिक्रिया के बाद बने जल की मात्रा (ग्राम में) ज्ञात करें। (H = 1, O = 16)
📌 उत्तर:
H₂ = 10 g ⇒ मोल = 10 / 2 = 5 mol
O₂ = 80 g ⇒ मोल = 80 / 32 = 2.5 mol
2 H₂ + O₂ → 2 H₂O
2 mol H₂ + 1 mol O₂ से 2 mol H₂O बनता है
तो 5 mol H₂ और 2.5 mol O₂ से
⇒ 5 mol H₂O बनेगा
⇒ 5 × 18 = 90 g H₂O
🔷 प्रश्न 27. 1.25 g Na₂CO₃ को 250 mL घोल में घोलने पर उसका मोलरता ज्ञात करें। (Na=23, C=12, O=16)
📌 उत्तर:
Na₂CO₃ का मोलर द्रव्यमान = (23×2) + 12 + (16×3) = 106 g/mol
मोल = 1.25 / 106 ≈ 0.01179 mol
वॉल्यूम = 250 mL = 0.250 L
मोलरता = मोल / लीटर
= 0.01179 / 0.250 = 0.0472 mol/L
🔷 प्रश्न 28. CH₄ में C और H का भार प्रतिशत ज्ञात करें। (C=12, H=1)
📌 उत्तर:
CH₄ का मोलर द्रव्यमान = 12 + (4×1) = 16 g/mol
→ C का प्रतिशत = (12/16) × 100 = 75%
→ H का प्रतिशत = (4/16) × 100 = 25%
🔶 Section D: केस आधारित प्रश्न (4 अंक प्रति प्रश्न)
🔷 प्रश्न 29.
निम्नलिखित जानकारी पर आधारित प्रश्नों के उत्तर दीजिए:
एक यौगिक में कार्बन = 40%, हाइड्रोजन = 6.67% और ऑक्सीजन = 53.33% है। यौगिक का अणु भार 180 है।
(क) अनुभव सूत्र ज्ञात कीजिए।
(ख) अनु सूत्र ज्ञात कीजिए।
📌 उत्तर:
(क)
मान लीजिए 100 g यौगिक है:
→ C = 40 g / 12 = 3.33 mol
→ H = 6.67 g / 1 = 6.67 mol
→ O = 53.33 g / 16 = 3.33 mol
सबसे कम मोल से भाग:
→ C = 3.33 / 3.33 = 1
→ H = 6.67 / 3.33 = 2
→ O = 3.33 / 3.33 = 1
अनुभव सूत्र = CH₂O
(ख)
CH₂O का मोलर द्रव्यमान = 12 + 2 + 16 = 30 g/mol
⇒ n = 180 / 30 = 6
⇒ अनु सूत्र = C₆H₁₂O₆
🔷 प्रश्न 30.
एक गैस के 4.4 g का आयतन STP पर 2.24 L पाया गया।
(क) गैस का मोलर द्रव्यमान ज्ञात करें।
(ख) गैस की पहचान करें।
📌 उत्तर:
(क)
मोल = आयतन / 22.4 = 2.24 / 22.4 = 0.1 mol
मोलर द्रव्यमान = 4.4 g / 0.1 mol = 44 g/mol
(ख)
44 g/mol = CO₂ (12 + 16×2)
⇒ गैस = कार्बन डाइऑक्साइड (CO₂)
🔷 प्रश्न 31.
नीचे दी गई अभिक्रिया पर आधारित प्रश्नों के उत्तर दीजिए:
Fe₂O₃ + 3CO → 2Fe + 3CO₂
(क) यदि 160 g Fe₂O₃ प्रयोग में लाया जाए, तो कितने ग्राम Fe प्राप्त होगा?
(Fe = 56, O = 16)
📌 उत्तर:
Fe₂O₃ का मोलर द्रव्यमान = (56×2) + (16×3) = 112 + 48 = 160 g/mol
⇒ 160 g = 1 mol Fe₂O₃
1 mol Fe₂O₃ → 2 mol Fe
⇒ Fe = 2 × 56 = 112 g Fe
🟦 Section E: दीर्घ उत्तरीय प्रश्न (5 अंक प्रति प्रश्न)
🔷 प्रश्न 32.
0.24 g Na₂CO₃ को 100 mL घोल में घोला गया। इस घोल की मोलरता ज्ञात करें।
(Na = 23, C = 12, O = 16)
📌 उत्तर:
Na₂CO₃ का मोलर द्रव्यमान = 106 g/mol
मोल = 0.24 / 106 = 0.00226 mol
वॉल्यूम = 100 mL = 0.100 L
मोलरता = मोल / वॉल्यूम
= 0.00226 / 0.100 = 0.0226 mol/L
🔷 प्रश्न 33.
एक मिश्रण में C = 40%, H = 6.7%, और O = 53.3% है। अणुभार 60 है। अनुभव सूत्र और अनु सूत्र ज्ञात करें।
📌 उत्तर:
→ C: 40 / 12 = 3.33 mol
→ H: 6.7 / 1 = 6.7 mol
→ O: 53.3 / 16 = 3.33 mol
Divide all by 3.33:
→ C = 1, H = 2, O = 1
अनुभव सूत्र = CH₂O
अनुभव सूत्र भार = 30
⇒ n = 60 / 30 = 2
⇒ अनु सूत्र = C₂H₄O₂
🔷 प्रश्न 34.
एक गैस का द्रव्यमान 1.4 g है और STP पर उसका आयतन 1.12 L है। गैस का मोलर द्रव्यमान तथा पहचान करें।
📌 उत्तर:
मोल = 1.12 / 22.4 = 0.05 mol
मोलर द्रव्यमान = 1.4 / 0.05 = 28 g/mol
⇒ गैस = नाइट्रोजन (N₂) (14 × 2 = 28)
🔷 प्रश्न 35.
2.3 g Na और 3.2 g सल्फर मिलाकर Na₂S तैयार किया जाता है। limiting reagent कौन-सी है और कितना उत्पाद बनेगा?
(Na = 23, S = 32)
📌 उत्तर:
Na के मोल = 2.3 / 23 = 0.1 mol
S के मोल = 3.2 / 32 = 0.1 mol
2Na + S → Na₂S
⇒ 2 mol Na के लिए 1 mol S
⇒ आवश्यक Na = 0.1 × 2 = 0.2 mol
मौजूद = 0.1 mol Na < आवश्यक
⇒ Limiting reagent = Na
0.1 mol Na = 0.05 mol Na₂S बनेगा
Na₂S का मोलर द्रव्यमान = (23×2) + 32 = 78 g/mol
⇒ उत्पाद = 0.05 × 78 = 3.9 g Na₂S
————————————————————————————————————————————————————————————————————————————
Neet पिछले सालों के प्रश्न
Q1. 1 ग्राम हाइड्रोजन अणु (H₂) में उपस्थित अणुओं की संख्या कितनी होगी?
(A) 6.022 × 10²²
(B) 3.011 × 10²³
(C) 6.022 × 10²³
(D) 1.204 × 10²⁴
Answer: (B)
Year: 2025 | Set: Z
Q2. 11.2 लीटर CH₄ गैस (STP पर) में उपस्थित अणुओं की संख्या कितनी है?
(A) 3.011 × 10²³
(B) 6.022 × 10²³
(C) 1.204 × 10²⁴
(D) 2.408 × 10²³
Answer: (A)
Year: 2025 | Set: X
Q3. निम्न में से कौन-सा मोल की परिभाषा को दर्शाता है?
(A) 1 ग्राम पदार्थ
(B) 6.022 × 10²³ कण
(C) 1 लीटर गैस
(D) 1 ग्राम-परमाणु
Answer: (B)
Year: 2024 | Set: 2
Q4. 2 ग्राम H₂ और 16 ग्राम O₂ से अधिकतम कितने ग्राम जल बन सकता है?
(A) 18
(B) 9
(C) 36
(D) 33
Answer: (B)
Year: 2024 | Set: Y
Q5. 4.4 ग्राम CO₂ में कितने मोल उपस्थित हैं? (C = 12, O = 16)
(A) 0.1
(B) 0.2
(C) 0.5
(D) 1
Answer: (B)
Year: 2023 | Set: 1
Q6. STP पर 5.6 लीटर O₂ गैस में उपस्थित अणुओं की संख्या क्या होगी?
(A) 1.505 × 10²³
(B) 3.011 × 10²³
(C) 6.022 × 10²³
(D) 4.408 × 10²³
Answer: (A)
Year: 2023 | Set: Z
Q7. एक मोल किसी भी गैस का STP पर आयतन होता है –
(A) 22.4 L
(B) 1 L
(C) 44.8 L
(D) 11.2 L
Answer: (A)
Year: 2022 | Set: Z
Q8. CH₄ अणु में उपस्थित C और H का भार प्रतिशत क्रमशः क्या है?
(A) 75%, 25%
(B) 25%, 75%
(C) 50%, 50%
(D) 12.5%, 87.5%
Answer: (A)
Year: 2022 | Set: X
Q9. 0.5 मोल NaCl में उपस्थित कुल आयन कितने होंगे?
(A) 6.022 × 10²³
(B) 3.011 × 10²³
(C) 1.204 × 10²⁴
(D) 2.408 × 10²³
Answer: (C)
Year: 2021 | Set: 2
Q10. निम्न में से कौन-सी राशि मौलिक भौतिक राशि नहीं है?
(A) तापमान
(B) द्रव्यमान
(C) घनत्व
(D) समय
Answer: (C)
Year: 2021 | Set: 1
Q11. एक गैस का मोलर द्रव्यमान 32 ग्राम है। STP पर 64 ग्राम गैस का आयतन कितना होगा?
(A) 22.4 L
(B) 44.8 L
(C) 11.2 L
(D) 33.6 L
Answer: (B)
Year: 2020 | Set: Y
Q12. Na₂CO₃ का मोलर द्रव्यमान क्या है?
(A) 106 g/mol
(B) 86 g/mol
(C) 96 g/mol
(D) 76 g/mol
Answer: (A)
Year: 2020 | Set: X
Q13. 0.1 मोल Fe₂O₃ में उपस्थित Fe परमाणुओं की संख्या कितनी होगी?
(A) 6.022 × 10²³
(B) 1.204 × 10²³
(C) 1.806 × 10²³
(D) 3.011 × 10²³
Answer: (C)
Year: 2019 | Set: 1
Q14. H₂O अणु का मोलर द्रव्यमान क्या है?
(A) 10 g/mol
(B) 12 g/mol
(C) 18 g/mol
(D) 16 g/mol
Answer: (C)
Year: 2019 | Set: Z
Q15. एक अणु का मोलर द्रव्यमान 60 g/mol है। 180 ग्राम में कितने मोल होंगे?
(A) 3
(B) 2
(C) 6
(D) 1
Answer: (A)
Year: 2018 | Set: X
Q16. 16 ग्राम O₂ गैस में कितने मोल होते हैं?
(A) 1
(B) 0.5
(C) 2
(D) 1.5
Answer: (B)
Year: 2018 | Set: Y
Q17. एक पदार्थ में 1.204 × 10²⁴ कण हैं, तो वह कितने मोल होंगे?
(A) 2
(B) 1
(C) 0.5
(D) 1.5
Answer: (A)
Year: 2017 | Set: 2
Q18. निम्नलिखित में से कौन-सा गैस नियम है जो मोल और आयतन का संबंध बताता है?
(A) बॉयल का नियम
(B) शार्ल का नियम
(C) अवोगाद्रो का नियम
(D) गे लूसाक का नियम
Answer: (C)
Year: 2017 | Set: 1
Q19. 0.25 मोल CH₄ में कितने हाइड्रोजन परमाणु होंगे?
(A) 6.022 × 10²³
(B) 3.011 × 10²³
(C) 1.505 × 10²⁴
(D) 2.408 × 10²³
Answer: (C)
Year: 2016 | Set: Y
Q20. 1 एमयू (amu) का मान क्या है?
(A) 1.66 × 10⁻²⁷ kg
(B) 1.66 × 10⁻²⁴ g
(C) 1.66 × 10⁻²³ kg
(D) 1.66 × 10⁻²⁶ g
Answer: (A)
Year: 2016 | Set: Z
Q21. 44 ग्राम CO₂ में कितने अणु होंगे?
(A) 6.022 × 10²³
(B) 3.011 × 10²³
(C) 1.204 × 10²⁴
(D) 2.408 × 10²³
Answer: (A)
Year: 2015 | Set: 2
Q22. एक आदर्श गैस की मोलर मात्रा STP पर होती है:
(A) 11.2 L
(B) 22.4 L
(C) 33.6 L
(D) 44.8 L
Answer: (B)
Year: 2015 | Set: 1
Q23. 2 ग्राम हाइड्रोजन और 16 ग्राम ऑक्सीजन को मिलाकर जल बनाया गया। शेष गैस कौन-सी और कितनी रहेगी?
(A) O₂, 8 g
(B) H₂, 1 g
(C) O₂, 4 g
(D) कोई शेष नहीं
Answer: (C)
Year: 2014 | Set: X
Q24. NaCl का अणुभार कितना होता है?
(A) 58.5 g/mol
(B) 60 g/mol
(C) 56.5 g/mol
(D) 59.5 g/mol
Answer: (A)
Year: 2014 | Set: Y
Q25. निम्न में से किसका द्रव्यमान न्यूनतम होता है?
(A) 1 मोल Fe
(B) 1 मोल H
(C) 1 मोल Cu
(D) 1 मोल Zn
Answer: (B)
Year: 2013 | Set: Z
Q26. 3 मोल NO₂ गैस में उपस्थित ऑक्सीजन परमाणुओं की संख्या कितनी होगी?
(A) 6.022 × 10²³
(B) 3.611 × 10²⁴
(C) 1.806 × 10²⁴
(D) 2.408 × 10²⁴
Answer: (C)
Year: 2013 | Set: X
Q27. एक गैस का मोलर द्रव्यमान 44 g/mol है। 2.2 ग्राम उस गैस का STP पर आयतन क्या होगा?
(A) 1.12 L
(B) 2.24 L
(C) 0.56 L
(D) 4.48 L
Answer: (A)
Year: 2012 | Set: Y
Q28. यदि किसी मिश्रण में C : H : O का भार अनुपात 40 : 6.7 : 53.3 हो, तो अनुभव सूत्र क्या होगा?
(A) CH₂O
(B) C₂H₄O₂
(C) C₆H₁₂O₆
(D) CH₄O
Answer: (A)
Year: 2012 | Set: Z
Q29. CO₂ का मोलर द्रव्यमान क्या है?
(A) 32 g/mol
(B) 44 g/mol
(C) 28 g/mol
(D) 60 g/mol
Answer: (B)
Year: 2011 | Set: 2
Q30. 2.5 मोल N₂O गैस में उपस्थित अणुओं की संख्या कितनी होगी?
(A) 1.505 × 10²⁴
(B) 6.022 × 10²³
(C) 3.011 × 10²³
(D) 2.408 × 10²³
Answer: (A)
Year: 2011 | Set: 1
Q31. 22.4 L गैस STP पर कितने मोल के बराबर होती है?
(A) 0.5 mol
(B) 1 mol
(C) 2 mol
(D) 1.5 mol
Answer: (B)
Year: 2010 | Set: X
Q32. निम्न में से किसका द्रव्यमान सर्वाधिक है?
(A) 1 मोल H₂
(B) 1 मोल O₂
(C) 1 मोल CO₂
(D) 1 मोल CH₄
Answer: (C)
Year: 2010 | Set: Z
Q33. अवोगाद्रो संख्या के बराबर कणों की संख्या किसमें होगी?
(A) 12 g C
(B) 1 g H
(C) 18 g H₂O
(D) सभी
Answer: (D)
Year: 2009 | Set: Y
Q34. 0.5 मोल CH₄ में उपस्थित कुल परमाणुओं की संख्या कितनी होगी?
(A) 3.011 × 10²³
(B) 1.204 × 10²⁴
(C) 6.022 × 10²³
(D) 2.408 × 10²³
Answer: (B)
Year: 2009 | Set: Z
Q35. एक पदार्थ का अणुभार 90 g/mol है। 270 ग्राम में कितने मोल होंगे?
(A) 3
(B) 2
(C) 1
(D) 4
Answer: (A)
Year: 2008 | Set: 1
Q36. O₂ गैस का मोलर द्रव्यमान क्या है?
(A) 16 g/mol
(B) 32 g/mol
(C) 28 g/mol
(D) 44 g/mol
Answer: (B)
Year: 2008 | Set: 2
Q37. 1 मोल H₂O में कुल कितने परमाणु होते हैं?
(A) 6.022 × 10²³
(B) 1.204 × 10²⁴
(C) 1.806 × 10²⁴
(D) 3.011 × 10²³
Answer: (C)
Year: 2007 | Set: X
Q38. निम्न में से किस यौगिक का मोलर द्रव्यमान सर्वाधिक है?
(A) H₂O
(B) CH₄
(C) CO₂
(D) NH₃
Answer: (C)
Year: 2007 | Set: Z
Q39. STP पर 44.8 लीटर ऑक्सीजन गैस में कितने मोल होंगे?
(A) 2 mol
(B) 1 mol
(C) 3 mol
(D) 0.5 mol
Answer: (A)
Year: 2006 | Set: Y
Q40. 18 ग्राम H₂O में कितने मोल हैं?
(A) 1 mol
(B) 0.5 mol
(C) 2 mol
(D) 3 mol
Answer: (A)
Year: 2006 | Set: Z
Q41. 5.6 लीटर गैस STP पर कितने मोल के बराबर होगी?
(A) 0.25
(B) 0.5
(C) 1
(D) 2
Answer: (B)
Year: 2005 | Set: 2
Q42. एक गैस का मोलर द्रव्यमान 28 g/mol है। 56 ग्राम गैस STP पर कितने लीटर होगी?
(A) 22.4
(B) 11.2
(C) 44.8
(D) 33.6
Answer: (C)
Year: 2005 | Set: 1
Q43. निम्न में से कौन-सी इकाई SI प्रणाली की नहीं है?
(A) मोल
(B) लीटर
(C) किलोग्राम
(D) मीटर
Answer: (B)
Year: 2004 | Set: X
Q44. 1 मोल CO₂ में कुल कितने परमाणु होते हैं?
(A) 3.011 × 10²³
(B) 6.022 × 10²³
(C) 1.806 × 10²⁴
(D) 9.033 × 10²³
Answer: (C)
Year: 2004 | Set: Y
Q45. एक गैस का STP पर द्रव्यमान 88 g है और उसका आयतन 44.8 L है। मोलर द्रव्यमान है:
(A) 44 g/mol
(B) 88 g/mol
(C) 22 g/mol
(D) 66 g/mol
Answer: (A)
Year: 2003 | Set: Z
Q46. H₂O₂ का मोलर द्रव्यमान क्या है?
(A) 32 g/mol
(B) 34 g/mol
(C) 36 g/mol
(D) 18 g/mol
Answer: (B)
Year: 2003 | Set: X
Q47. 6.022 × 10²³ कण किसमें मिलेंगे?
(A) 1 mol H₂O
(B) 18 g H₂O
(C) 1 mol Na
(D) उपरोक्त सभी
Answer: (D)
Year: 2002 | Set: 1
Q48. CH₃OH में C और H का कुल भार प्रतिशत क्या है?
(A) 12:4
(B) 48:12
(C) 60:13
(D) 37.5:12.5
Answer: (D)
Year: 2002 | Set: 2
Q49. 1 मोल N₂ में कितने N परमाणु होते हैं?
(A) 6.022 × 10²³
(B) 1.204 × 10²⁴
(C) 3.011 × 10²³
(D) 2.408 × 10²³
Answer: (B)
Year: 2001 | Set: Y
Q50. एक रासायनिक समीकरण संतुलित होता है क्योंकि:
(A) यह ऊर्जा का संरक्षण करता है
(B) यह भार का संरक्षण करता है
(C) यह गति का संरक्षण करता है
(D) यह दाब का संरक्षण करता है
Answer: (B)
Year: 2001 | Set: Z
————————————————————————————————————————————————————————————————————————————
JEE MAINS पिछले सालों के प्रश्न
Q1. एक यौगिक की अनुभव सूत्र CH₂O है तथा उसका अणुभार 180 ग्राम प्रति मोल है। उसका अनु सूत्र क्या होगा?
(A) CH₂O
(B) C₂H₄O₂
(C) C₆H₁₂O₆
(D) C₃H₆O₃
उत्तर: (C)
Year: 2024 | Shift: 2 | Set: B
Q2. 88 ग्राम CO₂ में उपस्थित अणुओं की संख्या कितनी होगी?
(A) 1.204 × 10²⁴
(B) 6.022 × 10²³
(C) 2.408 × 10²³
(D) 3.011 × 10²³
उत्तर: (A)
Year: 2024 | Shift: 1 | Set: A
Q3. एक गैस के 2.24 लीटर STP पर कितने मोल होते हैं?
(A) 0.1
(B) 0.01
(C) 0.2
(D) 0.5
उत्तर: (A)
Year: 2023 | Shift: 1 | Set: C
Q4. यदि C : H : O का भार अनुपात किसी यौगिक में 40 : 6.7 : 53.3 है, तो अनुभव सूत्र क्या होगा?
(A) C₂H₄O₂
(B) CH₂O
(C) C₆H₁₂O₆
(D) CH₄O
उत्तर: (B)
Year: 2023 | Shift: 2 | Set: D
Q5. एक यौगिक में कार्बन = 27.3%, ऑक्सीजन = 72.7%, अणुभार = 88 है। अनुभव सूत्र ज्ञात करें।
(A) C₂H₄O₂
(B) C₃H₄O₃
(C) CH₂O₂
(D) C₂H₂O₄
उत्तर: (C)
Year: 2022 | Shift: 1 | Set: A
Q6. 18 ग्राम जल में कितने अणु होते हैं?
(A) 6.022 × 10²³
(B) 3.011 × 10²³
(C) 1.204 × 10²⁴
(D) 9.033 × 10²³
उत्तर: (A)
Year: 2022 | Shift: 2 | Set: C
Q7. एक अणु का द्रव्यमान 60 g/mol है। 0.5 मोल में उपस्थित अणुओं की संख्या क्या होगी?
(A) 3.011 × 10²³
(B) 1.204 × 10²⁴
(C) 6.022 × 10²³
(D) 2.408 × 10²³
उत्तर: (A)
Year: 2021 | Shift: 1 | Set: B
Q8. किसी गैस का मोलर द्रव्यमान 28 g/mol है। 5.6 लीटर STP पर उस गैस का द्रव्यमान कितना होगा?
(A) 5.6 g
(B) 7.0 g
(C) 6.0 g
(D) 8.0 g
उत्तर: (B)
Year: 2021 | Shift: 2 | Set: A
Q9. निम्न में से कौन-सी राशि भौतिक मौलिक राशि नहीं है?
(A) तापमान
(B) द्रव्यमान
(C) ऊर्जा
(D) लम्बाई
उत्तर: (C)
Year: 2020 | Shift: 1 | Set: C
Q10. 0.5 मोल Na₂SO₄ में उपस्थित कुल आयनों की संख्या क्या होगी?
(A) 6.022 × 10²³
(B) 1.806 × 10²⁴
(C) 3.011 × 10²³
(D) 9.033 × 10²³
उत्तर: (B)
Year: 2020 | Shift: 2 | Set: D
Q11. निम्न में से किस रासायनिक अभिक्रिया में द्रव्यमान संरक्षण का नियम लागू नहीं होता?
(A) Na + Cl₂ → NaCl
(B) CH₄ + 2O₂ → CO₂ + 2H₂O
(C) CaCO₃ → CaO + CO₂
(D) कोई नहीं
उत्तर: (D)
Year: 2019 | Shift: 1 | Set: A
Q12. 1 मोल CH₄ में उपस्थित कुल परमाणुओं की संख्या क्या है?
(A) 6.022 × 10²³
(B) 3.011 × 10²³
(C) 1.204 × 10²⁴
(D) 2.408 × 10²⁴
उत्तर: (D)
Year: 2019 | Shift: 2 | Set: B
Q13. एक मोल किसी गैस का STP पर आयतन क्या होता है?
(A) 11.2 लीटर
(B) 22.4 लीटर
(C) 44.8 लीटर
(D) 33.6 लीटर
उत्तर: (B)
Year: 2018 | Shift: 1 | Set: D
Q14. यदि 6.022 × 10²³ अणु किसी गैस में हैं, तो उसका आयतन STP पर क्या होगा?
(A) 22.4 लीटर
(B) 11.2 लीटर
(C) 1.12 लीटर
(D) 2.24 लीटर
उत्तर: (A)
Year: 2018 | Shift: 2 | Set: A
Q15. एक यौगिक का अणुभार 180 है तथा C : H : O अनुपात 40 : 6.7 : 53.3 है। अनु सूत्र क्या होगा?
(A) CH₂O
(B) C₂H₄O₂
(C) C₆H₁₂O₆
(D) CH₄O
उत्तर: (C)
Year: 2017 | Shift: 1 | Set: B
Q16. निम्न में से किस यौगिक का मोलर द्रव्यमान 98 ग्राम प्रति मोल है?
(A) H₂SO₄
(B) HNO₃
(C) NaOH
(D) KOH
उत्तर: (A)
Year: 2017 | Shift: 2 | Set: D
Q17. 4.4 ग्राम CO₂ में कितने मोल होते हैं?
(A) 0.1
(B) 0.2
(C) 0.5
(D) 1.0
उत्तर: (B)
Year: 2016 | Shift: 1 | Set: A
Q18. निम्नलिखित में से कौन-सा SI मात्रक नहीं है?
(A) मोल
(B) केल्विन
(C) लीटर
(D) किलोग्राम
उत्तर: (C)
Year: 2016 | Shift: 2 | Set: C
Q19. 5.6 लीटर ऑक्सीजन गैस में उपस्थित अणुओं की संख्या कितनी है?
(A) 3.011 × 10²³
(B) 6.022 × 10²³
(C) 1.505 × 10²³
(D) 2.408 × 10²³
उत्तर: (A)
Year: 2015 | Shift: 1 | Set: B
Q20. एक यौगिक का अणुभार 60 g/mol है। 180 ग्राम में कितने मोल होंगे?
(A) 3
(B) 2
(C) 1
(D) 6
उत्तर: (A)
Year: 2015 | Shift: 2 | Set: D
Q21. निम्नलिखित में से किसका द्रव्यमान सबसे कम होता है?
(A) 1 मोल Na
(B) 1 मोल Fe
(C) 1 मोल Cl
(D) 1 मोल H
उत्तर: (D)
Year: 2014 | Shift: 1 | Set: A
Q22. 22.4 लीटर CO₂ का द्रव्यमान कितना होगा?
(A) 22 g
(B) 32 g
(C) 44 g
(D) 16 g
उत्तर: (C)
Year: 2014 | Shift: 2 | Set: C
Q23. यदि किसी यौगिक में 0.2 मोल H₂ हैं, तो उसमें उपस्थित अणुओं की संख्या क्या होगी?
(A) 1.204 × 10²³
(B) 6.022 × 10²³
(C) 3.011 × 10²³
(D) 2.408 × 10²³
उत्तर: (A)
Year: 2013 | Shift: 1 | Set: B
Q24. 1 मोल CaCO₃ में उपस्थित कुल परमाणुओं की संख्या कितनी होगी?
(A) 3.011 × 10²³
(B) 1.204 × 10²⁴
(C) 6.022 × 10²³
(D) 1.806 × 10²⁴
उत्तर: (D)
Year: 2013 | Shift: 2 | Set: A
Q25. Na₂CO₃ का अणुभार क्या है?
(A) 106
(B) 76
(C) 58
(D) 84
उत्तर: (A)
Year: 2012 | Shift: 1 | Set: C
Q26. CH₄ में C और H का भार प्रतिशत क्रमशः क्या होगा?
(A) 25% और 75%
(B) 75% और 25%
(C) 40% और 60%
(D) 50% और 50%
उत्तर: (B)
Year: 2012 | Shift: 2 | Set: D
Q27. 1 मोल SO₂ में कितने अणु होते हैं?
(A) 6.022 × 10²³
(B) 3.011 × 10²³
(C) 1.204 × 10²⁴
(D) 2.408 × 10²³
उत्तर: (A)
Year: 2011 | Shift: 1 | Set: A
Q28. 0.5 मोल NaCl में उपस्थित Na⁺ आयनों की संख्या क्या होगी?
(A) 6.022 × 10²³
(B) 3.011 × 10²³
(C) 1.204 × 10²⁴
(D) 2.408 × 10²³
उत्तर: (B)
Year: 2011 | Shift: 2 | Set: C
Q29. यदि 1 ग्राम हाइड्रोजन अणु (H₂) हो, तो कितने मोल होंगे?
(A) 1 mol
(B) 0.5 mol
(C) 0.25 mol
(D) 2 mol
उत्तर: (B)
Year: 2010 | Shift: 1 | Set: A
Q30. निम्नलिखित में से किस गैस का मोलर द्रव्यमान सर्वाधिक है?
(A) CH₄
(B) O₂
(C) CO₂
(D) NH₃
उत्तर: (C)
Year: 2010 | Shift: 2 | Set: D
Q31. किसी यौगिक में तत्वों का भार प्रतिशत इस प्रकार है: Na = 43.4%, C = 11.3%, और O = 45.3%। अनुभव सूत्र क्या होगा?
(A) NaCO₂
(B) Na₂CO₃
(C) Na₂C₂O₄
(D) NaHCO₃
उत्तर: (B)
Year: 2009 | Shift: 1 | Set: B
Q32. 1 मोल किसी भी आदर्श गैस का STP पर आयतन होता है:
(A) 11.2 L
(B) 22.4 L
(C) 33.6 L
(D) 44.8 L
उत्तर: (B)
Year: 2009 | Shift: 2 | Set: C
Q33. 2 मोल NO₂ में कितने O परमाणु होंगे?
(A) 3.011 × 10²³
(B) 6.022 × 10²³
(C) 2.408 × 10²⁴
(D) 1.204 × 10²⁴
उत्तर: (C)
Year: 2008 | Shift: 1 | Set: A
Q34. यदि 1 मोल NaOH में उपस्थित Na⁺ आयन पूछे जाएँ, तो उनका उत्तर होगा:
(A) 6.022 × 10²³
(B) 3.011 × 10²³
(C) 1.204 × 10²⁴
(D) 1.806 × 10²⁴
उत्तर: (A)
Year: 2008 | Shift: 2 | Set: D
Q35. किसी अज्ञात गैस का द्रव्यमान 88 g है और आयतन STP पर 44.8 लीटर है। मोलर द्रव्यमान है:
(A) 44 g/mol
(B) 22 g/mol
(C) 88 g/mol
(D) 66 g/mol
उत्तर: (A)
Year: 2007 | Shift: 1 | Set: B
Q36. निम्न में से किस यौगिक का अनुभव सूत्र CH₂O है?
(A) ग्लूकोज़
(B) फॉर्मल्डिहाइड
(C) एसिटिक अम्ल
(D) एथेनॉल
उत्तर: (A)
Year: 2007 | Shift: 2 | Set: A
Q37. निम्नलिखित में से किस यौगिक में तीन प्रकार के परमाणु होते हैं?
(A) CO₂
(B) O₂
(C) CH₄
(D) H₂
उत्तर: (A)
Year: 2006 | Shift: 1 | Set: C
Q38. 2 मोल H₂O में कुल कितने परमाणु होंगे?
(A) 1.204 × 10²⁴
(B) 3.011 × 10²⁴
(C) 2.408 × 10²⁴
(D) 1.806 × 10²⁴
उत्तर: (D)
Year: 2006 | Shift: 2 | Set: D
Q39. 22.4 लीटर गैस का द्रव्यमान 44 ग्राम है, तो गैस कौन-सी हो सकती है?
(A) N₂
(B) O₂
(C) CO₂
(D) SO₂
उत्तर: (C)
Year: 2005 | Shift: 1 | Set: A
Q40. एक यौगिक में C : H का मोल अनुपात 1 : 2 है तथा मोलर द्रव्यमान 30 g/mol है। अनु सूत्र क्या होगा?
(A) CH₄
(B) C₂H₄
(C) C₂H₆
(D) C₃H₈
उत्तर: (C)
Year: 2005 | Shift: 2 | Set: B
Q41. निम्न में से कौन-सी राशि व्युत्पन्न राशि है?
(A) तापमान
(B) मोल
(C) घनत्व
(D) द्रव्यमान
उत्तर: (C)
Year: 2004 | Shift: 1 | Set: C
Q42. H₂O₂ का मोलर द्रव्यमान क्या है?
(A) 34 g/mol
(B) 32 g/mol
(C) 36 g/mol
(D) 18 g/mol
उत्तर: (A)
Year: 2004 | Shift: 2 | Set: D
Q43. निम्न में से किस यौगिक में केवल 2 प्रकार के तत्व उपस्थित हैं?
(A) CH₄
(B) CO₂
(C) NH₃
(D) NaCl
उत्तर: (B)
Year: 2003 | Shift: 1 | Set: B
Q44. 1 मोल NO₂ में कितने NO बंध उपस्थित हैं?
(A) 6.022 × 10²³
(B) 3.011 × 10²³
(C) 1.204 × 10²⁴
(D) 1.806 × 10²⁴
उत्तर: (A)
Year: 2003 | Shift: 2 | Set: C
Q45. निम्न में से कौन-सा संयुग्मन (combination) उचित है?
(A) 1 मोल = 6.022 × 10²³ कण
(B) 1 मोल = 22.4 ग्राम
(C) 1 मोल = 1 ग्राम
(D) 1 मोल = 100 कण
उत्तर: (A)
Year: 2002 | Shift: 1 | Set: A
Q46. H₂O₂ में उपस्थित तत्वों की संख्या है:
(A) 2
(B) 3
(C) 4
(D) 1
उत्तर: (A)
Year: 2002 | Shift: 2 | Set: B
Q47. एक गैस का STP पर द्रव्यमान 2.8 g है और आयतन 2.24 L है। मोलर द्रव्यमान होगा:
(A) 28 g/mol
(B) 44 g/mol
(C) 22 g/mol
(D) 11 g/mol
उत्तर: (A)
Year: 2001 | Shift: 1 | Set: C
Q48. किसी पदार्थ में 1.505 × 10²³ अणु हैं, तो उसमें कितने मोल होंगे?
(A) 0.25 mol
(B) 0.5 mol
(C) 1 mol
(D) 2 mol
उत्तर: (A)
Year: 2001 | Shift: 2 | Set: D
Q49. NaCl का अणुभार कितना है?
(A) 58.5 g/mol
(B) 60 g/mol
(C) 56.5 g/mol
(D) 59.5 g/mol
उत्तर: (A)
Year: 2001 | Shift: 3 | Set: A
Q50. 1 मोल H₂O₂ में कुल कितने परमाणु होते हैं?
(A) 3.011 × 10²³
(B) 6.022 × 10²³
(C) 1.806 × 10²⁴
(D) 2.408 × 10²⁴
उत्तर: (C)
Year: 2001 | Shift: 3 | Set: B
————————————————————————————————————————————————————————————————————————————
JEE ADVANCED पिछले सालों के प्रश्न
Q1. 1 मोल किसी आदर्श गैस का आयतन STP पर होता है:
(A) 22.4 लीटर
(B) 11.2 लीटर
(C) 44.8 लीटर
(D) 33.6 लीटर
उत्तर: (A)
Year: 2025 | Paper: 1 | Set: 1
Q2. एक यौगिक का अणुभार 60 g/mol है। यदि 30 ग्राम यौगिक हो, तो उसमें मोल की संख्या होगी:
(A) 0.5
(B) 2
(C) 1
(D) 3
उत्तर: (A)
Year: 2025 | Paper: 1 | Set: 2
Q3. निम्न में से कौन-सा नियम मोल संख्या और आयतन के बीच संबंध बताता है?
(A) बॉयल का नियम
(B) शार्ल का नियम
(C) अवोगाद्रो का नियम
(D) गे-लूसाक का नियम
उत्तर: (C)
Year: 2024 | Paper: 1 | Set: 1
Q4. 0.5 मोल CO₂ गैस में उपस्थित ऑक्सीजन परमाणुओं की संख्या होगी:
(A) 3.011 × 10²³
(B) 6.022 × 10²³
(C) 1.505 × 10²³
(D) 1.204 × 10²⁴
उत्तर: (A)
Year: 2024 | Paper: 1 | Set: 2
Q5. 88 ग्राम CO₂ में उपस्थित अणुओं की संख्या कितनी होगी?
(A) 1.204 × 10²⁴
(B) 6.022 × 10²³
(C) 2.408 × 10²³
(D) 3.011 × 10²³
उत्तर: (A)
Year: 2023 | Paper: 1 | Set: 2
Q6. निम्न में से किस यौगिक का मोलर द्रव्यमान सर्वाधिक है?
(A) CH₄
(B) CO₂
(C) H₂O
(D) NH₃
उत्तर: (B)
Year: 2023 | Paper: 1 | Set: 1
Q7. यदि किसी यौगिक में C : H : O का भार प्रतिशत 40 : 6.7 : 53.3 है और अणुभार 180 g/mol है, तो उसका अनुभव सूत्र होगा:
(A) CH₂O
(B) C₂H₄O₂
(C) C₆H₁₂O₆
(D) C₃H₆O₃
उत्तर: (C)
Year: 2022 | Paper: 1 | Set: 2
Q8. STP पर 5.6 लीटर O₂ गैस में कितने अणु होते हैं?
(A) 3.011 × 10²³
(B) 1.505 × 10²³
(C) 6.022 × 10²³
(D) 2.408 × 10²³
उत्तर: (A)
Year: 2022 | Paper: 1 | Set: 1
Q9. 0.25 मोल CH₄ में कुल हाइड्रोजन परमाणुओं की संख्या क्या होगी?
(A) 6.022 × 10²³
(B) 1.204 × 10²⁴
(C) 2.408 × 10²³
(D) 1.505 × 10²⁴
उत्तर: (D)
Year: 2021 | Paper: 1 | Set: 2
Q10. निम्न में से कौन-सा एक SI मात्रक नहीं है?
(A) मोल
(B) केल्विन
(C) लीटर
(D) किलोग्राम
उत्तर: (C)
Year: 2021 | Paper: 1 | Set: 1
Q11. 1 मोल H₂O₂ में उपस्थित कुल परमाणुओं की संख्या होगी:
(A) 6.022 × 10²³
(B) 1.204 × 10²⁴
(C) 1.806 × 10²⁴
(D) 2.408 × 10²⁴
उत्तर: (C)
Year: 2020 | Paper: 1 | Set: 2
Q12. 4.4 ग्राम CO₂ में उपस्थित मोल की संख्या क्या होगी?
(A) 0.1
(B) 0.2
(C) 0.5
(D) 1
उत्तर: (B)
Year: 2020 | Paper: 1 | Set: 1
Q13. 0.1 मोल SO₂ गैस में उपस्थित अणुओं की संख्या होगी:
(A) 6.022 × 10²²
(B) 1.204 × 10²³
(C) 3.011 × 10²²
(D) 2.408 × 10²²
उत्तर: (A)
Year: 2019 | Paper: 1 | Set: 2
Q14. CH₄ अणु में C और H का भार प्रतिशत क्रमशः है:
(A) 75% और 25%
(B) 25% और 75%
(C) 50% और 50%
(D) 60% और 40%
उत्तर: (A)
Year: 2019 | Paper: 1 | Set: 1
Q15. 1 मोल CaCO₃ में उपस्थित कुल परमाणुओं की संख्या क्या होगी?
(A) 1.204 × 10²⁴
(B) 6.022 × 10²³
(C) 3.011 × 10²³
(D) 1.806 × 10²⁴
उत्तर: (D)
Year: 2018 | Paper: 1 | Set: 2
Q16. 1.0 ग्राम H₂ में कितने अणु होंगे?
(A) 3.011 × 10²³
(B) 6.022 × 10²³
(C) 1.204 × 10²⁴
(D) 2.408 × 10²³
उत्तर: (A)
Year: 2018 | Paper: 1 | Set: 1
Q17. Na₂SO₄ के 0.5 मोल में कुल आयनों की संख्या कितनी होगी?
(A) 1.204 × 10²⁴
(B) 3.011 × 10²³
(C) 6.022 × 10²³
(D) 9.033 × 10²³
उत्तर: (A)
Year: 2017 | Paper: 1 | Set: 2
Q18. 1 मोल CH₄ में कुल परमाणुओं की संख्या कितनी होगी?
(A) 6.022 × 10²³
(B) 3.011 × 10²³
(C) 1.204 × 10²⁴
(D) 2.408 × 10²⁴
उत्तर: (D)
Year: 2025 | Paper: 2 | Set: 1
Q19. किसी यौगिक का अनुभव सूत्र CH₂O है तथा उसका अणुभार 180 g/mol है। उसका अनु सूत्र होगा:
(A) CH₂O
(B) C₂H₄O₂
(C) C₆H₁₂O₆
(D) C₃H₆O₃
उत्तर: (C)
Year: 2024 | Paper: 2 | Set: 2
Q20. एक मिश्रण में C : H : O का भार अनुपात 40 : 6.7 : 53.3 है। अनुभव सूत्र क्या होगा?
(A) CH₄
(B) CH₂O
(C) C₂H₄O
(D) C₂H₆O
उत्तर: (B)
Year: 2024 | Paper: 2 | Set: 1
Q21. 5.6 लीटर गैस STP पर कितने मोल के बराबर होती है?
(A) 0.25
(B) 0.5
(C) 1
(D) 2
उत्तर: (B)
Year: 2023 | Paper: 2 | Set: 2
Q22. 1 मोल NaCl में Na⁺ आयनों की संख्या होगी:
(A) 6.022 × 10²³
(B) 3.011 × 10²³
(C) 1.204 × 10²⁴
(D) 9.033 × 10²³
उत्तर: (A)
Year: 2023 | Paper: 2 | Set: 1
Q23. H₂O₂ अणु का मोलर द्रव्यमान है:
(A) 34 g/mol
(B) 36 g/mol
(C) 18 g/mol
(D) 32 g/mol
उत्तर: (A)
Year: 2022 | Paper: 2 | Set: 2
Q24. 44.8 लीटर O₂ गैस STP पर कितने मोल के बराबर होगी?
(A) 1
(B) 2
(C) 3
(D) 0.5
उत्तर: (B)
Year: 2022 | Paper: 2 | Set: 1
Q25. एक गैस का द्रव्यमान 1.4 g है और उसका STP पर आयतन 1.12 L है। मोलर द्रव्यमान क्या होगा?
(A) 28 g/mol
(B) 44 g/mol
(C) 22 g/mol
(D) 32 g/mol
उत्तर: (A)
Year: 2021 | Paper: 2 | Set: 2
Q26. 1 मोल CO₂ गैस में कितने परमाणु होते हैं?
(A) 6.022 × 10²³
(B) 1.204 × 10²⁴
(C) 1.806 × 10²⁴
(D) 2.408 × 10²⁴
उत्तर: (C)
Year: 2021 | Paper: 2 | Set: 1
Q27. CH₄ गैस में C और H के मोल अनुपात क्रमशः क्या होंगे?
(A) 1 : 2
(B) 1 : 4
(C) 1 : 1
(D) 2 : 1
उत्तर: (B)
Year: 2020 | Paper: 2 | Set: 2
Q28. 0.5 मोल O₂ गैस में कितने O परमाणु होते हैं?
(A) 3.011 × 10²³
(B) 6.022 × 10²³
(C) 1.204 × 10²⁴
(D) 2.408 × 10²³
उत्तर: (B)
Year: 2020 | Paper: 2 | Set: 1
Q29. निम्न में से कौन-सा यौगिक केवल दो प्रकार के तत्वों से बना है?
(A) CH₄
(B) CO₂
(C) NH₃
(D) NaCl
उत्तर: (B)
Year: 2019 | Paper: 2 | Set: 2
Q30. 18 ग्राम जल में कितने अणु होते हैं?
(A) 6.022 × 10²³
(B) 3.011 × 10²³
(C) 1.204 × 10²⁴
(D) 2.408 × 10²³
उत्तर: (A)
Year: 2019 | Paper: 2 | Set: 1
Q31. 1 मोल किसी गैस का STP पर आयतन होता है:
(A) 11.2 L
(B) 22.4 L
(C) 33.6 L
(D) 44.8 L
उत्तर: (B)
Year: 2018 | Paper: 2 | Set: 2
Q32. 2 मोल CH₄ में उपस्थित कुल परमाणुओं की संख्या कितनी होगी?
(A) 1.204 × 10²⁴
(B) 3.011 × 10²⁴
(C) 2.408 × 10²⁴
(D) 1.806 × 10²⁴
उत्तर: (B)
Year: 2018 | Paper: 2 | Set: 1
Q33. CO₂ अणु का मोलर द्रव्यमान क्या है?
(A) 44 g/mol
(B) 32 g/mol
(C) 28 g/mol
(D) 46 g/mol
उत्तर: (A)
Year: 2017 | Paper: 2 | Set: 2
Q34. किसी रासायनिक अभिक्रिया में द्रव्यमान संरक्षण का नियम संतुलन बनाए रखने में क्यों सहायक होता है?
(A) परमाणु संरक्षित रहते हैं
(B) अणु बदलते नहीं
(C) मोल संरक्षित रहते हैं
(D) द्रव्यमान नष्ट नहीं होता
उत्तर: (D)
Year: 2017 | Paper: 2 | Set: 1
————————————————————————————————————————————————————————————————————————————
मॉडल प्रश्न पत्र, अभ्यास
Q1. किसी यौगिक में कार्बन = 40%, हाइड्रोजन = 6.7% और ऑक्सीजन = 53.3% है। अनुभव सूत्र क्या होगा?
(A) CH₄O
(B) CH₂O
(C) C₂H₄O₂
(D) CH₃O
Answer: (B)
Q2. 1 मोल पानी में उपस्थित अणुओं की संख्या कितनी होगी?
(A) 6.022 × 10²²
(B) 6.022 × 10²³
(C) 3.011 × 10²³
(D) 1.204 × 10²⁴
Answer: (B)
Q3. किसी आदर्श गैस के लिए STP पर मोलर आयतन होता है:
(A) 11.2 L
(B) 22.4 L
(C) 33.6 L
(D) 44.8 L
Answer: (B)
Q4. NaCl का अणुभार होता है:
(A) 56.5 g/mol
(B) 58.5 g/mol
(C) 60.5 g/mol
(D) 52.5 g/mol
Answer: (B)
Q5. CH₄ अणु में C और H का भार प्रतिशत क्रमशः होगा:
(A) 40% और 60%
(B) 25% और 75%
(C) 75% और 25%
(D) 50% और 50%
Answer: (C)
Q6. 0.5 मोल CO₂ में उपस्थित अणुओं की संख्या है:
(A) 3.011 × 10²³
(B) 1.505 × 10²³
(C) 6.022 × 10²³
(D) 2.408 × 10²³
Answer: (A)
Q7. निम्न में से कौन-सी भौतिक राशि मौलिक नहीं है?
(A) द्रव्यमान
(B) घनत्व
(C) तापमान
(D) समय
Answer: (B)
Q8. 44 ग्राम CO₂ में कितने मोल होते हैं?
(A) 1
(B) 2
(C) 0.5
(D) 1.5
Answer: (A)
Q9. 1 मोल NaOH में उपस्थित OH⁻ आयनों की संख्या कितनी होगी?
(A) 1.204 × 10²⁴
(B) 6.022 × 10²³
(C) 3.011 × 10²³
(D) 9.033 × 10²³
Answer: (B)
Q10. किसी अणु का द्रव्यमान 90 g/mol है। यदि 180 ग्राम पदार्थ हो, तो मोल संख्या होगी:
(A) 2
(B) 0.5
(C) 1
(D) 3
Answer: (A)
Q11. निम्न में से किस गैस का मोलर द्रव्यमान 28 g/mol है?
(A) CO
(B) CO₂
(C) CH₄
(D) N₂O
Answer: (A)
Q12. एक अणु में कुल 3 प्रकार के परमाणु हैं – यह किस पर लागू होता है?
(A) H₂
(B) CO₂
(C) H₂O
(D) NaCl
Answer: (C)
Q13. निम्न में से कौन-सा गैस नियम मोल संख्या से संबंधित है?
(A) बॉयल का नियम
(B) शार्ल का नियम
(C) अवोगाद्रो का नियम
(D) गे-लूसाक का नियम
Answer: (C)
Q14. 1.5 मोल H₂O में उपस्थित कुल परमाणुओं की संख्या कितनी होगी?
(A) 2.408 × 10²⁴
(B) 1.806 × 10²⁴
(C) 1.204 × 10²⁴
(D) 9.033 × 10²³
Answer: (B)
Q15. 5.6 लीटर गैस STP पर कितने मोल के बराबर होती है?
(A) 0.25
(B) 0.5
(C) 1
(D) 2
Answer: (B)
Q16. CH₄ का मोलर द्रव्यमान कितना है?
(A) 14 g/mol
(B) 16 g/mol
(C) 18 g/mol
(D) 20 g/mol
Answer: (B)
Q17. H₂O₂ में उपस्थित कुल परमाणु होते हैं:
(A) 2
(B) 3
(C) 4
(D) 5
Answer: (C)
Q18. CO₂ अणु में कुल कितने परमाणु होते हैं?
(A) 3
(B) 2
(C) 4
(D) 1
Answer: (A)
Q19. 2.5 मोल CH₄ में उपस्थित कुल हाइड्रोजन परमाणुओं की संख्या है:
(A) 5.0 × 10²⁴
(B) 6.022 × 10²³
(C) 1.204 × 10²⁴
(D) 2.408 × 10²⁴
Answer: (A)
Q20. 1 मोल CO₂ में उपस्थित ऑक्सीजन परमाणुओं की संख्या है:
(A) 3.011 × 10²³
(B) 6.022 × 10²³
(C) 1.204 × 10²⁴
(D) 2.408 × 10²³
Answer: (C)
Q21. निम्न में से किसका द्रव्यमान सबसे कम होता है?
(A) 1 मोल H₂
(B) 1 मोल CO₂
(C) 1 मोल O₂
(D) 1 मोल CH₄
Answer: (A)
Q22. NaOH का अणुभार होता है:
(A) 36 g/mol
(B) 40 g/mol
(C) 44 g/mol
(D) 46 g/mol
Answer: (B)
Q23. निम्न में से कौन-सी इकाई SI प्रणाली की नहीं है?
(A) मोल
(B) लीटर
(C) किलोग्राम
(D) केल्विन
Answer: (B)
Q24. यदि किसी गैस का मोलर द्रव्यमान 32 g/mol है, तो 64 ग्राम का STP पर आयतन होगा:
(A) 22.4 L
(B) 33.6 L
(C) 44.8 L
(D) 11.2 L
Answer: (C)
Q25. 0.25 मोल NaCl में कुल आयनों की संख्या क्या होगी?
(A) 6.022 × 10²³
(B) 3.011 × 10²³
(C) 1.204 × 10²⁴
(D) 9.033 × 10²³
Answer: (B)
Q26. एक यौगिक में C = 54.5%, H = 9.1%, और O = 36.4% है। यदि उसका अणुभार 88 g/mol है, तो अनु सूत्र क्या होगा?
(A) C₃H₈O₃
(B) C₄H₈O₂
(C) C₂H₄O
(D) C₃H₆O₂
Answer: (A)
Q27. 0.1 मोल CaCO₃ में उपस्थित Ca²⁺ आयनों की संख्या होगी:
(A) 6.022 × 10²²
(B) 3.011 × 10²³
(C) 1.204 × 10²³
(D) 6.022 × 10²³
Answer: (A)
Q28. 90 ग्राम H₂O में उपस्थित कुल अणुओं की संख्या होगी:
(A) 3.011 × 10²⁴
(B) 1.806 × 10²⁴
(C) 1.204 × 10²⁴
(D) 2.408 × 10²⁴
Answer: (A)
Q29. 44.8 लीटर CH₄ गैस STP पर द्रव्यमान होगा:
(A) 16 g
(B) 32 g
(C) 64 g
(D) 88 g
Answer: (C)
Q30. निम्न में से कौन-सी मात्रक संयोजित नहीं है?
(A) घनत्व = kg/m³
(B) दाब = N/m²
(C) मोलर संकेन्द्रण = mol/L
(D) ताप = kg/K
Answer: (D)
Q31. किसी अज्ञात यौगिक में 6.022 × 10²³ C परमाणु तथा 1.204 × 10²⁴ H परमाणु हैं। अनुभव सूत्र होगा:
(A) CH₄
(B) CH₆
(C) CH₂
(D) C₂H₄
Answer: (C)
Q32. 2 मोल CO₂ में कितने कुल परमाणु होंगे?
(A) 6.022 × 10²³
(B) 1.806 × 10²⁴
(C) 3.011 × 10²³
(D) 1.204 × 10²⁴
Answer: (B)
Q33. 4 ग्राम H₂ और 32 ग्राम O₂ को मिलाकर जल बनाने पर कितना जल बनेगा?
(A) 18 g
(B) 36 g
(C) 54 g
(D) 72 g
Answer: (B)
Q34. 1 मोल CH₃OH में उपस्थित कुल बंधों की संख्या कितनी होगी?
(A) 4
(B) 5
(C) 6
(D) 7
Answer: (D)
Q35. निम्नलिखित में से कौन-सा युग्म SI प्रणाली में नहीं है?
(A) द्रव्यमान – किलोग्राम
(B) तापमान – फेरेनहाइट
(C) समय – सेकंड
(D) पदार्थ की मात्रा – मोल
Answer: (B)
Q36. 1 मोल CO₂ का STP पर आयतन और द्रव्यमान क्रमशः हैं:
(A) 22.4 L, 32 g
(B) 22.4 L, 44 g
(C) 44.8 L, 88 g
(D) 11.2 L, 22 g
Answer: (B)
Q37. 2.5 मोल NaOH में उपस्थित Na⁺ आयनों की संख्या होगी:
(A) 1.505 × 10²⁴
(B) 2.408 × 10²⁴
(C) 6.022 × 10²³
(D) 3.011 × 10²³
Answer: (A)
Q38. एक मिश्रण में CH₄ और O₂ का अनुपात 1:2 है। पूर्ण दहन के बाद प्राप्त जल की मोल संख्या होगी:
(A) 1
(B) 2
(C) 4
(D) 3
Answer: (B)
Q39. 0.75 मोल N₂ गैस में उपस्थित परमाणुओं की संख्या क्या होगी?
(A) 1.204 × 10²⁴
(B) 9.033 × 10²³
(C) 6.022 × 10²³
(D) 3.011 × 10²³
Answer: (A)
Q40. यदि 1 मोल पदार्थ का अणुभार 98 g/mol हो, तो 49 ग्राम में उपस्थित अणुओं की संख्या कितनी होगी?
(A) 6.022 × 10²³
(B) 3.011 × 10²³
(C) 1.204 × 10²⁴
(D) 9.033 × 10²³
Answer: (B)
Q41–Q50: JEE Advanced उपयुक्त कठिन प्रश्न
Q41. CH₃COOH में उपस्थित सभी बंधों की कुल संख्या कितनी होगी?
(A) 5
(B) 6
(C) 7
(D) 8
Answer: (D)
Q42. किसी अणु में 6.022 × 10²³ अणु और 1.806 × 10²⁴ परमाणु हैं। औसतन प्रति अणु कितने परमाणु हैं?
(A) 2
(B) 3
(C) 4
(D) 5
Answer: (C)
Q43. C₂H₆O के दो समावयवों में से एक में हाइड्रोजन बंध सम्भव है, वह है:
(A) एथेनॉल
(B) डाइमेथाइल ईथर
(C) एसीटोन
(D) फॉर्मल्डिहाइड
Answer: (A)
Q44. 0.1 मोल H₂SO₄ को जल में घोलने पर प्राप्त कुल आयनों की संख्या कितनी होगी?
(A) 6.022 × 10²²
(B) 1.204 × 10²³
(C) 1.806 × 10²³
(D) 2.408 × 10²³
Answer: (C)
Q45. यदि CO₂ का मोलर द्रव्यमान 44 g/mol है, तो 88 ग्राम CO₂ में STP पर कितने लीटर गैस होगी?
(A) 22.4
(B) 44.8
(C) 11.2
(D) 33.6
Answer: (B)
Q46. एक अज्ञात यौगिक में C = 27.27%, O = 72.73% है और अणुभार 88 है। अनु सूत्र होगा:
(A) CO
(B) CO₂
(C) C₂O₃
(D) CH₂O₂
Answer: (B)
Q47. 4.4 ग्राम CO₂ में कितने अणु होंगे?
(A) 6.022 × 10²²
(B) 3.011 × 10²³
(C) 1.505 × 10²³
(D) 2.408 × 10²²
Answer: (C)
Q48. H₂O₂ का मोलर द्रव्यमान 34 g/mol है। 68 ग्राम में उपस्थित मोल की संख्या होगी:
(A) 1
(B) 2
(C) 3
(D) 0.5
Answer: (B)
Q49. 1 मोल O₃ में उपस्थित कुल बंधों की संख्या होगी:
(A) 1.204 × 10²⁴
(B) 6.022 × 10²³
(C) 1.806 × 10²⁴
(D) 2.408 × 10²⁴
Answer: (B)
Q50. यदि 2 मोल CH₄ जलाते हैं, तो अधिकतम कितने मोल जल उत्पादित होंगे?
(A) 2
(B) 4
(C) 1
(D) 3
Answer: (B)
————————————————————————————————————————————————————————————————————————————
