Class 8 : Science – ( Hindi ) : Lesson 9. विलेयों, विलायकों और विलयनों का अदभुत संसार
व्याख्या और विवेचन
🔹 विलयन की मूल अवधारणा
हम अपने दैनिक जीवन में अनेक ऐसे पदार्थ देखते हैं जो देखने में एक जैसे लगते हैं, परंतु वास्तव में वे दो या अधिक पदार्थों के मिश्रण होते हैं 🧠। जब एक पदार्थ दूसरे पदार्थ में पूरी तरह घुल जाता है और एकसमान मिश्रण बनाता है, तो उसे विलयन कहा जाता है ⚖️। उदाहरण के रूप में जल में घुली चीनी या नमक को लिया जा सकता है 💧।
विलयन हमें यह समझने में सहायता करता है कि पदार्थ केवल ठोस, द्रव या गैस के रूप में ही नहीं, बल्कि मिश्रित रूप में भी पाए जाते हैं 🔄। विज्ञान में विलयनों का अध्ययन अत्यंत महत्वपूर्ण है, क्योंकि अनेक प्राकृतिक और औद्योगिक प्रक्रियाएँ इन्हीं पर आधारित होती हैं 🏭🌍।
🔹 विलायक और विलेय
विलयन के दो मुख्य घटक होते हैं — विलायक और विलेय 🧪। जिस पदार्थ में दूसरा पदार्थ घुलता है, उसे विलायक कहते हैं, जबकि जो पदार्थ घुलता है, उसे विलेय कहा जाता है ⚖️।
उदाहरण के लिए, नमक और जल के विलयन में जल विलायक है और नमक विलेय 🧠। सामान्यतः विलायक की मात्रा विलेय से अधिक होती है, जिससे विलेय पूरी तरह घुल सके 📌।
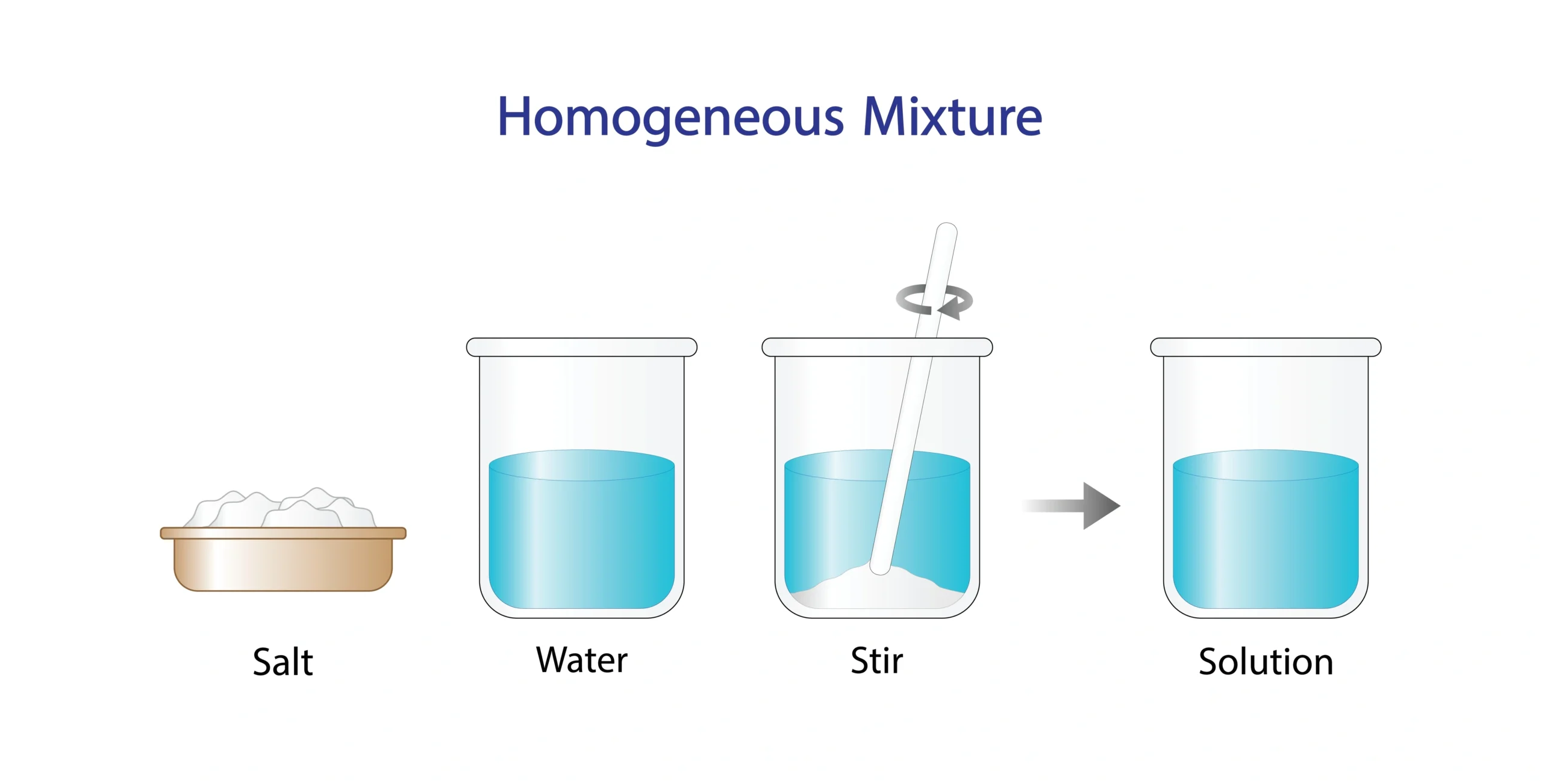
🔹 विलयन बनने की प्रक्रिया
जब विलेय को विलायक में मिलाया जाता है, तो विलेय के कण विलायक के कणों के बीच प्रवेश कर जाते हैं 🔄। इस प्रक्रिया में विलेय दिखाई नहीं देता, परंतु वह विलयन में उपस्थित रहता है 🧠।
विलयन बनने के बाद मिश्रण का प्रत्येक भाग समान गुण दर्शाता है ⚖️। इसी कारण विलयन को एकसमान मिश्रण कहा जाता है 📐।
🔹 विलयन के गुण
विलयन पारदर्शी होता है और उसमें विलेय के कण नग्न आँखों से दिखाई नहीं देते 👀❌। विलयन को छानने से विलेय अलग नहीं किया जा सकता ⚠️।
विलयन स्थिर होता है और समय के साथ परतों में नहीं बँटता 🧠। ये सभी गुण विलयन को अन्य मिश्रणों से अलग करते हैं 📌।
🔹 सांद्रता की अवधारणा
विलयन में विलेय की मात्रा को सांद्रता कहा जाता है 📐। यदि विलेय की मात्रा अधिक हो, तो विलयन सान्द्र कहलाता है, और यदि मात्रा कम हो, तो विलयन विरल होता है ⚖️।
सांद्रता विलयन के गुणों को प्रभावित करती है 🧠। स्वाद, रंग और क्रिया-शीलता सभी सांद्रता पर निर्भर करते हैं 🍹।
🔹 संतृप्त और असंतृप्त विलयन
जिस विलयन में और अधिक विलेय घुल सकता है, उसे असंतृप्त विलयन कहते हैं 🧪। इसके विपरीत, जिस विलयन में निर्धारित तापमान पर और विलेय न घुल सके, वह संतृप्त विलयन कहलाता है ⚖️।
यदि संतृप्त विलयन को गरम किया जाए, तो उसमें और विलेय घुल सकता है 🔥। इससे स्पष्ट होता है कि तापमान विलयन को प्रभावित करता है 🧠।
🔹 तापमान का प्रभाव
तापमान बढ़ाने से अधिकांश ठोस विलेयों की घुलनशीलता बढ़ जाती है 🌡️। यही कारण है कि गरम जल में चीनी जल्दी घुल जाती है 💧➡️🍬।
कुछ गैसों के लिए स्थिति विपरीत होती है 🧠। अधिक तापमान पर गैसों की घुलनशीलता कम हो जाती है, जैसे गरम पानी में कम गैस घुलती है ⚖️।
🔹 विलयनों के प्रकार
विलयन ठोस, द्रव और गैस — तीनों अवस्थाओं में पाए जा सकते हैं 🧪। ठोस विलयन का उदाहरण मिश्र धातु है, जैसे पीतल ⚙️।
द्रव विलयन में नमक जल या चीनी जल आते हैं 💧। गैसीय विलयन का उदाहरण वायु है, जिसमें विभिन्न गैसें घुली होती हैं 🌬️।
🔹 दैनिक जीवन में विलयन
हमारे दैनिक जीवन में विलयन का व्यापक उपयोग होता है 🏠। शीतल पेय, औषधियाँ और भोजन सभी विलयन के उदाहरण हैं 🧃💊।
कृषि में उर्वरकों के विलयन और चिकित्सा में इंजेक्शन के विलयन का उपयोग किया जाता है 🌾⚕️। इससे स्पष्ट होता है कि विलयन जीवन का अभिन्न अंग हैं 🧠।
🔹 विलयन और पर्यावरण
प्राकृतिक जल स्रोतों में अनेक पदार्थ विलयन के रूप में उपस्थित रहते हैं 🌊। यदि हानिकारक पदार्थ जल में घुल जाएँ, तो प्रदूषण फैलता है ⚠️।
विलयनों की समझ पर्यावरण संरक्षण में सहायता करती है 🌍। इससे जल शुद्धिकरण और प्रदूषण नियंत्रण संभव होता है 🧠।
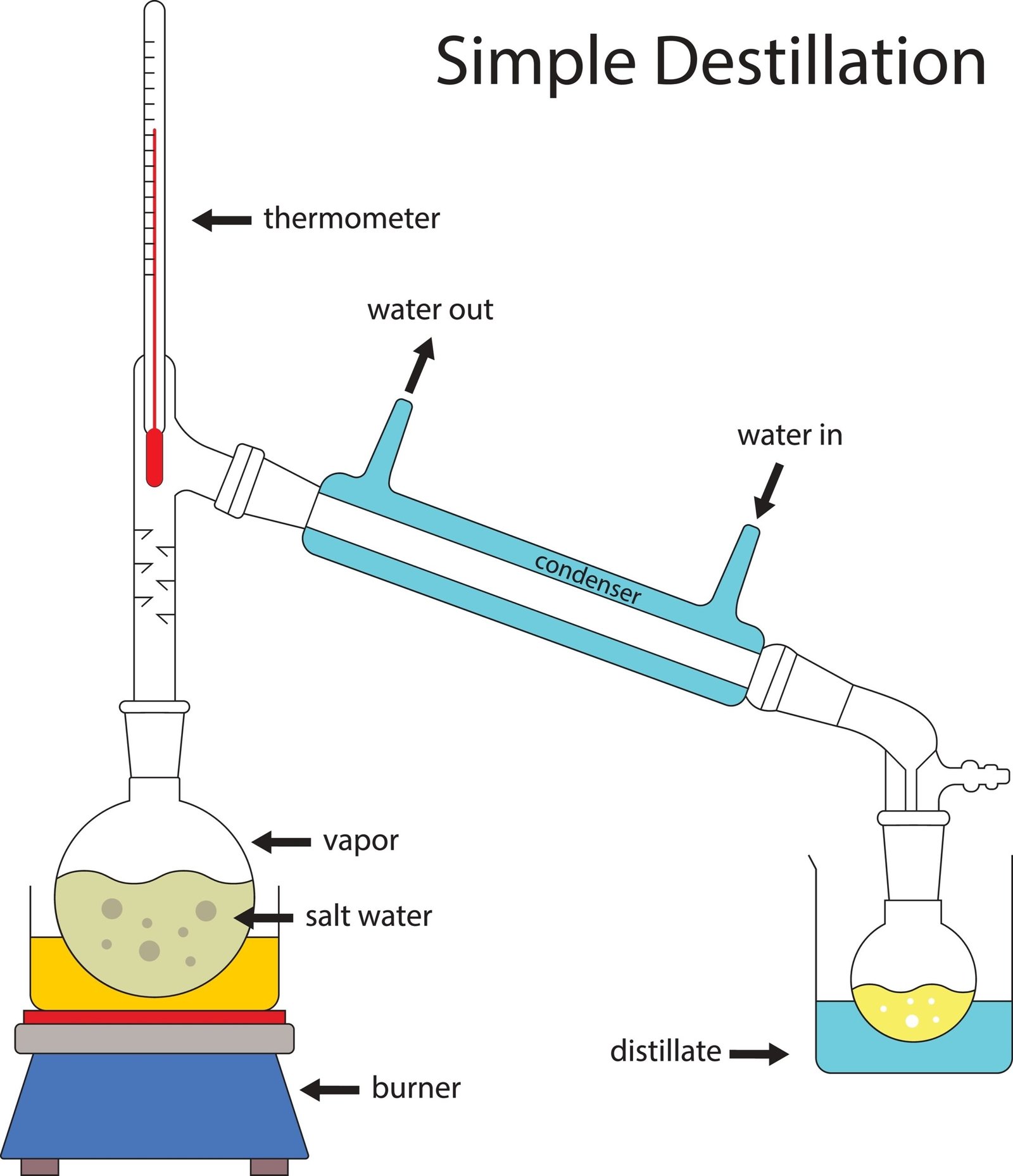
🔹 विज्ञान और विलयन
विलयन का अध्ययन रसायन विज्ञान की आधारशिला है 🧪। औद्योगिक उत्पादन, औषधि निर्माण और अनुसंधान में विलयन की भूमिका महत्वपूर्ण है 🏭🔬।
इस अध्याय से विद्यार्थियों को पदार्थों के व्यवहार की गहरी समझ मिलती है ⚖️।
🔹 सारांश
विलयन दो या अधिक पदार्थों का एकसमान मिश्रण होता है। विलयन के मुख्य घटक विलायक और विलेय होते हैं। विलयन पारदर्शी, स्थिर और एकसमान होता है। सांद्रता, तापमान और घुलनशीलता विलयन के गुणों को प्रभावित करते हैं। विलयन ठोस, द्रव और गैस — तीनों अवस्थाओं में पाए जाते हैं। दैनिक जीवन, उद्योग और पर्यावरण में विलयन की महत्वपूर्ण भूमिका है।
🔹 त्वरित पुनरावृत्ति ⭐
⭐ विलयन एकसमान मिश्रण होता है
⭐ विलायक में विलेय घुलता है
⭐ विलयन छानने से अलग नहीं होता
⭐ सांद्रता विलेय की मात्रा दर्शाती है
⭐ संतृप्त विलयन में और विलेय नहीं घुलता
⭐ तापमान घुलनशीलता को प्रभावित करता है
⭐ ठोस, द्रव और गैसीय विलयन होते हैं
⭐ विलयन दैनिक जीवन में उपयोगी हैं
⭐ विलयन पर्यावरण से जुड़े हैं
⭐ विलयन रसायन विज्ञान का आधार है
——————————————————————————————————————————————————————————————————————————–
पाठ्यपुस्तक के प्रश्न
🔒 ❓ प्रश्न 1.
सत्य-असत्य कथनों को पहचानिए और सही करें।
📌 ✅ उत्तर:
🔹 (क) ✔️ सत्य — ऑक्सीजन गैस की विलयशीलता ठंडे जल में गर्म जल की अपेक्षा अधिक होती है।
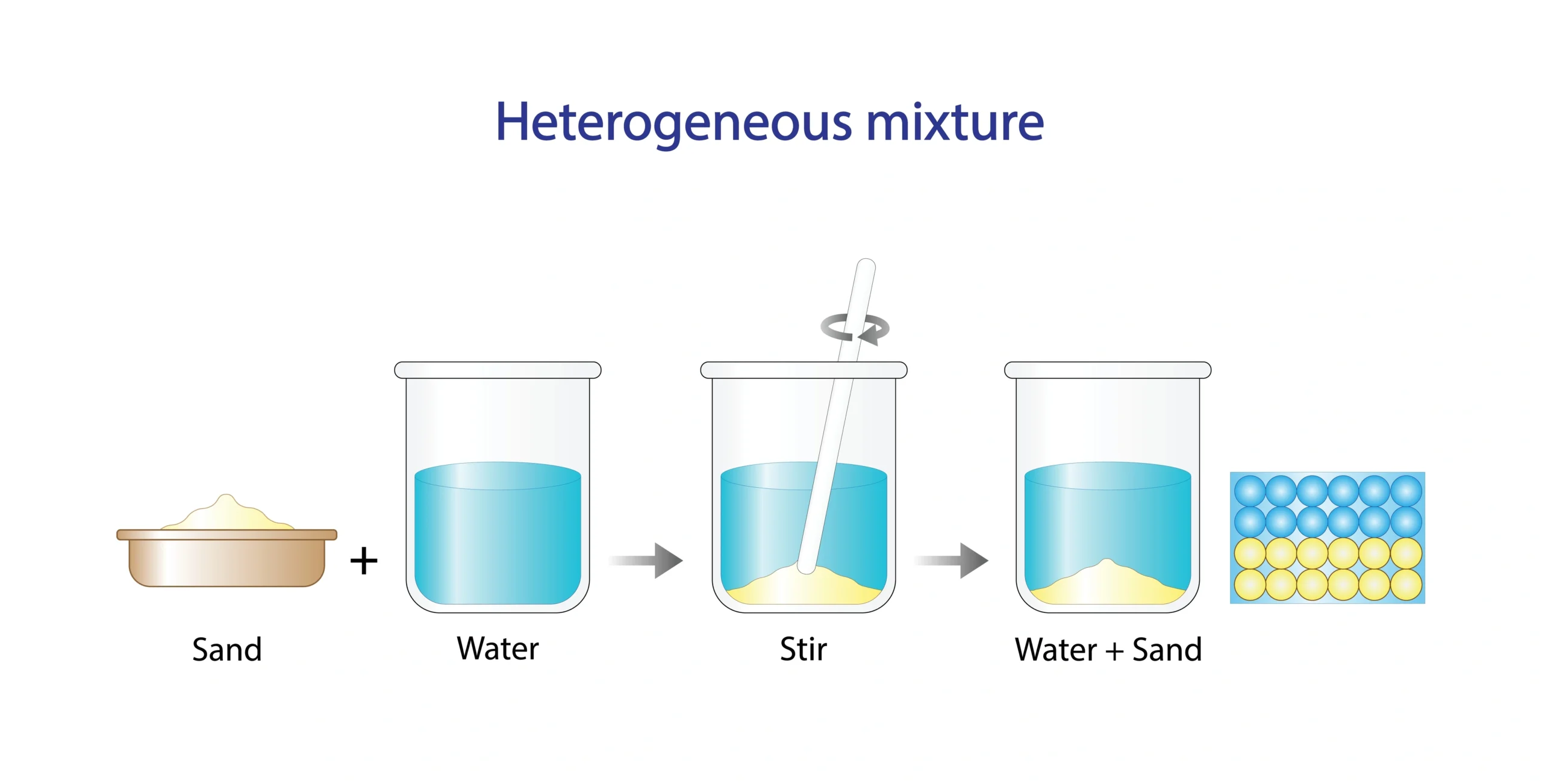
🔹 (ख) ✔️ सत्य — तेल और पानी का मिश्रण एक विलयन नहीं बल्कि अविलयन (emulsion) होता है।
🔹 (ग) ✔️ सत्य — किसी वस्तु द्वारा विस्थापित पानी को उसका आयतन माना जाता है।
🔹 (घ) ❌ असत्य — संतृप्त विलयन में और अधिक विलेय घुल नहीं सकता; अधिक विलेयता असंतृप्त विलयन की विशेषता है।
🔹 (ङ) ✔️ सत्य — वायुमंडलीय वायु एक समरूप मिश्रण (homogeneous mixture) है।
🔒 ❓ प्रश्न 2.
रिक्त स्थानों की पूर्ति कीजिए।
📌 ✅ उत्तर:
(क) किसी ठोस का आयतन विस्थापन विधि द्वारा मापा जा सकता है, जहाँ ठोस जल में पूरी तरह डूब जाता है और जल स्तर का अंतर मापा जाता है।
(ख) किसी विशिष्ट तापमान पर विलेय की अधिकतम मात्रा जो घुल सकती है, उसे उस तापमान पर उस पदार्थ की विलेयता कहते हैं।
(ग) तापमान बढ़ने पर प्रायः विलेयता में वृद्धि होती है।
(घ) ऐसा विलयन जिसमें विलेय पूरी तरह घुल चुका हो और और अधिक नहीं घुल सकता, वह संतृप्त विलयन कहलाता है।
🔒 ❓ प्रश्न 3.
जब आप तेल को जल में डालते हैं तो वह ऊपर तैरता है। कारण स्पष्ट करें।
📌 ✅ उत्तर:
➡️ इसका कारण तेल का जल से कम घनत्व होना है।
➡️ तेल और जल आपस में अविलेय होते हैं और घनत्व के कारण हल्का होने से तेल ऊपर तैरता है।
✔️ सही विकल्प: (क) — तेल जल से कम सघन होता है।
🔒 ❓ प्रश्न 4.
द्रव का द्रव्यमान = 225 g, आयतन = 90 cm³ → घनत्व ज्ञात कीजिए।
📌 ✅ उत्तर:
घनत्व = द्रव्यमान / आयतन
= 225 g / 90 cm³
= 2.5 g/cm³
✔️ यदि यह द्रव जल की तुलना में अधिक घनत्व वाला है, तो यह जल में डूबेगा।
🔒 ❓ प्रश्न 5.
कौन-सा कथन विलेयता के नियमों के विरुद्ध है?
📌 ✅ उत्तर:
✔️ सही विकल्प: (घ) — एक संतृप्त विलयन उच्च तापमान पर बनता है ❌
➡️ यह कथन गलत है क्योंकि संतृप्त विलयन किसी भी तापमान पर बन सकता है।
🔒 ❓ प्रश्न 6.
आपके पास 2 लीटर क्षमता की बोतल है। उसमें 500 mL जल भरा है।
📌 ✅ उत्तर:
➡️ बोतल की कुल क्षमता = 2000 mL
➡️ भरे गए जल की मात्रा = 500 mL
➡️ शेष स्थान = 2000 – 500 = 1500 mL जल और भरा जा सकता है।
🔒 ❓ प्रश्न 7.
एक संतरे का द्रव्यमान = 400 g, आयतन = 40 cm³
➡️ घनत्व = ?
📌 ✅ उत्तर:
घनत्व = द्रव्यमान / आयतन
= 400 / 40 = 10 g/cm³
🔒 ❓ प्रश्न 8.
चित्र 9.25 — छिलके वाला संत्रा तैरता है, बिना छिलके का डूबता है। क्यों?
📌 ✅ उत्तर:
➡️ छिलका संत्रे को अधिक आयतन देता है, जिससे उसका घनत्व कम होता है और वह तैरता है।
➡️ छिलका हटाने से आयतन कम हो जाता है, और संत्रे का घनत्व बढ़ जाता है → वह डूब जाता है।
🔒 ❓ प्रश्न 9.
संत्रा ‘क’ का द्रव्यमान = 200 g, आयतन = 40 cm³
संत्रा ‘ख’ का द्रव्यमान = 240 g, आयतन = 60 cm³
📌 ✅ उत्तर:
➡️ घनत्व ‘क’ = 200 / 40 = 5 g/cm³
➡️ घनत्व ‘ख’ = 240 / 60 = 4 g/cm³
✔️ संत्रा ‘ख’ का घनत्व कम है → वह अधिक तैरने योग्य होगा।
🔒 ❓ प्रश्न 10.
एक वस्तु का द्रव्यमान = 120 g, आयतन = 60 cm³
📌 ✅ उत्तर:
घनत्व = 120 / 60 = 2 g/cm³
➡️ यदि इस घनत्व से अधिक घनत्व वाला द्रव है, तो वस्तु डूबेगी।
➡️ यदि कम घनत्व वाला द्रव है, तो वस्तु तैरेगी।
🔒 ❓ प्रश्न 11.
लोहे की ब्लॉक → द्रव्यमान = 600 g, घनत्व = 7.9 g/cm³
➡️ आयतन = ?
📌 ✅ उत्तर:
➡️ आयतन = द्रव्यमान / घनत्व
= 600 / 7.9 ≈ 75.95 cm³
🔒 ❓ प्रश्न 12.
चित्र 9.26 — नली में जल जम गया, दबाव से नली फट सकती है — क्यों?
📌 ✅ उत्तर:
➡️ जब जल को -70°C पर ठंडा किया गया, तो वह बर्फ में बदल गया, और उसका आयतन बढ़ गया।
➡️ यह बढ़ा हुआ आयतन सीमित स्थान में अधिक दाब बनाता है, जिससे नली फट जाती है।
✔️ यह जल के विलक्षण गुणों में से एक है — जमते समय इसका आयतन बढ़ता है।
——————————————————————————————————————————————————————————————————————————–
अन्य महत्वपूर्ण प्रश्न
SECTION 1 — बहुविकल्पीय प्रश्न (5 Questions)
🔒 ❓ Q1. जिस पदार्थ में कोई अन्य पदार्थ घुलता है, उसे क्या कहते हैं?
🟢 1️⃣ विलेय
🔵 2️⃣ विलायक
🟡 3️⃣ विलयन
🟣 4️⃣ अविलेय
✔️ Answer: 🔵 2️⃣ विलायक
🔒 ❓ Q2. जो पदार्थ विलायक में घुलता है, वह क्या कहलाता है?
🟢 1️⃣ विलायक
🔵 2️⃣ विलेय
🟡 3️⃣ मिश्रण
🟣 4️⃣ अवसाद
✔️ Answer: 🔵 2️⃣ विलेय
🔒 ❓ Q3. नमक का जल में घुलना किसका उदाहरण है?
🟢 1️⃣ निलंबन
🔵 2️⃣ विलयन
🟡 3️⃣ अविलेय मिश्रण
🟣 4️⃣ पायस
✔️ Answer: 🔵 2️⃣ विलयन
🔒 ❓ Q4. निम्न में से कौन सही विलायक है?
🟢 1️⃣ चीनी
🔵 2️⃣ नमक
🟡 3️⃣ जल
🟣 4️⃣ चाक
✔️ Answer: 🟡 3️⃣ जल
🔒 ❓ Q5. किसी विलयन में अधिकतम विलेय घुल जाने की अवस्था क्या कहलाती है?
🟢 1️⃣ विरल अवस्था
🔵 2️⃣ संतृप्त अवस्था
🟡 3️⃣ असंतृप्त अवस्था
🟣 4️⃣ ठोस अवस्था
✔️ Answer: 🔵 2️⃣ संतृप्त अवस्था
SECTION 2 — अति लघु उत्तरीय प्रश्न (5 Questions)
🔒 ❓ Q6. विलयन किसे कहते हैं?
📌 ✅ Answer: विलेय और विलायक का समांग मिश्रण
🔒 ❓ Q7. विलेय का एक उदाहरण लिखिए।
📌 ✅ Answer: नमक
🔒 ❓ Q8. विलायक का एक उदाहरण लिखिए।
📌 ✅ Answer: जल
🔒 ❓ Q9. संतृप्त विलयन क्या होता है?
📌 ✅ Answer: जिसमें और विलेय न घुल सके
🔒 ❓ Q10. क्या सभी पदार्थ जल में घुलते हैं?
📌 ✅ Answer: नहीं
SECTION 3 — लघु उत्तरीय प्रश्न (3 Questions)
🔒 ❓ Q11. विलयन कैसे बनता है?
📌 ✅ Answer:
🔹 विलेय को विलायक में मिलाया जाता है।
🔸 कण समान रूप से फैल जाते हैं।
🔹 समांग मिश्रण बन जाता है।
🔒 ❓ Q12. संतृप्त और असंतृप्त विलयन में अंतर लिखिए।
📌 ✅ Answer:
🔹 संतृप्त विलयन में अधिक विलेय नहीं घुलता।
🔸 असंतृप्त विलयन में और विलेय घुल सकता है।
🔹 ताप बढ़ाने से घुलनशीलता बदल सकती है।
🔒 ❓ Q13. विलयनों का दैनिक जीवन में क्या महत्व है?
📌 ✅ Answer:
🔹 पेय पदार्थ विलयन होते हैं।
🔸 औषधियाँ प्रायः विलयन रूप में होती हैं।
🔹 भोजन और उद्योग में व्यापक उपयोग है।
SECTION 4 — दीर्घ उत्तरीय प्रश्न (2 Questions)
🔒 ❓ Q14. विलायक, विलेय और विलयन को उदाहरण सहित समझाइए।
📌 ✅ Answer:
🔹 विलायक वह पदार्थ है जिसमें अन्य पदार्थ घुलते हैं।
🔸 विलेय वह पदार्थ है जो विलायक में घुलता है।
🔹 दोनों के मिलने से विलयन बनता है।
🔸 नमक और जल का विलयन इसका सामान्य उदाहरण है।
🔒 ❓ Q15. ताप का विलयनों की घुलनशीलता पर क्या प्रभाव पड़ता है?
📌 ✅ Answer:
🔹 अधिकांश ठोस पदार्थों की घुलनशीलता ताप बढ़ाने पर बढ़ती है।
🔸 ताप घटाने पर विलेय अलग हो सकता है।
🔹 इस सिद्धांत का उपयोग दैनिक जीवन और उद्योग में होता है।
——————————————————————————————————————————————————————————————————————————–
उच्चतर ज्ञान
🧭 विलयन: दिखाई देने से अधिक गहरा विज्ञान
हमारे दैनिक जीवन में अनेक ऐसे द्रव्य मिलते हैं जो एक समान दिखाई देते हैं,
पर वास्तव में वे कई पदार्थों के संयोजन से बने होते हैं 🧪।
चीनी का जल में घुलना,
नमक का सूप में मिल जाना,
या वायु का एकसमान होना—
ये सभी विलयन के उदाहरण हैं 🌊।
विलयन केवल पदार्थों का मेल नहीं है,
बल्कि यह कणों के स्तर पर होने वाली
एक सुव्यवस्थित प्रक्रिया है।
इस प्रक्रिया को समझे बिना
द्रव्य के व्यवहार को पूरी तरह नहीं जाना जा सकता।
⭐ एक-पंक्ति विचार
जो एकसमान दिखता है, वह अक्सर विलयन होता है।
🧠 विलयन क्या है
विलयन वह मिश्रण है
जिसमें एक पदार्थ दूसरे पदार्थ में
पूरी तरह और समान रूप से घुल जाता है 🧠।
इसमें घुला हुआ पदार्थ
अलग दिखाई नहीं देता।
विलयन की विशेषता यह है कि
इसके सभी भागों में
संघटन एक जैसा होता है।
इसी कारण विलयन
दिखने में एकसमान प्रतीत होता है।
🧪 विलायक: घुलाने वाला माध्यम
विलायक वह पदार्थ है
जिसमें कोई अन्य पदार्थ घुलता है 🧪।
अधिकांश विलयनों में
विलायक की मात्रा अधिक होती है।
जल सबसे सामान्य विलायक है,
इसलिए इसे
सार्वभौमिक विलायक कहा जाता है 🌊।
अनेक ठोस, द्रव और गैसीय पदार्थ
जल में आसानी से घुल जाते हैं।
विलायक की प्रकृति
यह निर्धारित करती है कि
कौन-सा पदार्थ उसमें घुलेगा।
⭐ एक-पंक्ति बल
विलायक विलयन की आधारभूमि है।
🌱 विलेय: घुलने वाला पदार्थ
विलेय वह पदार्थ है
जो विलायक में घुलता है 🌱।
विलेय की मात्रा
आमतौर पर विलायक से कम होती है।
नमक, चीनी या गैसें
विलेय के सामान्य उदाहरण हैं।
विलेय के कण
विलायक के कणों के बीच
रिक्त स्थानों में समा जाते हैं।
इसी कारण
विलयन बनने पर
आयतन में बहुत अधिक परिवर्तन नहीं होता।
🌀 विलयन की कणीय व्याख्या
विलयन बनने की प्रक्रिया
कणों के स्तर पर घटित होती है 🌀।
विलेय के कण
विलायक के कणों के बीच फैल जाते हैं
और समान रूप से वितरित हो जाते हैं।
यह दर्शाता है कि
द्रव्य के कणों के बीच
रिक्त स्थान होता है
और कण निरंतर गतिशील रहते हैं।
विलयन
द्रव्य की कणीय प्रकृति का
प्रत्यक्ष प्रमाण है।
🌡️ ताप का विलयन पर प्रभाव
ताप विलयन की प्रक्रिया को
महत्वपूर्ण रूप से प्रभावित करता है 🌡️।
अधिक ताप पर
कणों की गति बढ़ जाती है,
जिससे विलेय
तेज़ी से घुलता है।
इसी कारण
गर्म जल में चीनी
ठंडे जल की अपेक्षा
जल्दी घुल जाती है।
यह उदाहरण
कणों की गति और
ताप के संबंध को स्पष्ट करता है।
⚖️ विलयन की सांद्रता का विचार
विलयन में
विलेय की मात्रा
उसकी सांद्रता को निर्धारित करती है ⚖️।
कम विलेय वाला विलयन
पतला कहलाता है,
जबकि अधिक विलेय वाला
गाढ़ा माना जाता है।
सांद्रता का ज्ञान
औषधि निर्माण,
खाद्य पदार्थों
और रासायनिक प्रक्रियाओं में
अत्यंत आवश्यक है।
🌱 दैनिक जीवन में विलयन
विलयन का संसार
केवल प्रयोगशाला तक सीमित नहीं है 🌱।
हमारा दैनिक जीवन
विलयनों से भरा हुआ है।
🍵 चाय और कॉफी
🩺 औषधीय घोल
🌬️ वायु
🌊 समुद्री जल
ये सभी
विलयन के विविध रूप हैं।
इनकी समझ
हमें पदार्थों के उपयोग में
सजग बनाती है।
⚠️ भ्रांति और वैज्ञानिक सत्य
⚠️ भ्रांति
घुला हुआ पदार्थ नष्ट हो जाता है।
✅ वैज्ञानिक सत्य
विलेय नष्ट नहीं होता,
बल्कि विलायक में
समान रूप से फैल जाता है।
⚠️ भ्रांति
सभी पदार्थ जल में घुलते हैं।
✅ वैज्ञानिक सत्य
केवल कुछ पदार्थ ही
जल में घुलनशील होते हैं।
सही समझ
विज्ञान की गहराई को उजागर करती है।
🧠 मुख्य अवधारणा
विलयन
🧪 विलायक
🌱 विलेय
🌀 कणों का समान वितरण
🌡️ ताप का प्रभाव
⚖️ सांद्रता
के माध्यम से
द्रव्य की कणीय प्रकृति को स्पष्ट करता है।
विलयनों का अध्ययन
पदार्थों के व्यवहार को
समझने की दिशा में
एक महत्वपूर्ण कदम है।
⭐ अंतिम विचार
जब हम विलयनों को समझते हैं,
तब द्रव्य का सूक्ष्म संसार
हमारे लिए स्पष्ट हो जाता है।
——————————————————————————————————————————————————————————————————————————–
