Class 10: Science (In Hindi) – Lesson 4. कार्बन एवं उसके यौगिक
पाठ का विश्लेषण एवं विवेचन
🔵 व्याख्या (Explanation)
💡 परिचय:
कार्बन एक अत्यंत बहुमुखी तत्व है। इसकी चार संयोजकता (4 valency) और श्रृंखला निर्माण (Catenation) की क्षमता के कारण यह असंख्य यौगिक बनाता है। पृथ्वी पर पाए जाने वाले लगभग सभी जैविक पदार्थों में कार्बन उपस्थित होता है — जैसे प्रोटीन, कार्बोहाइड्रेट, तेल, वसा आदि।
🟢 1️⃣ कार्बन की संयोजकता (Valency of Carbon)
कार्बन का परमाणु क्रमांक 6 है और इसकी इलेक्ट्रॉनिक संरचना 2,4 होती है। इसमें चार संयोजक इलेक्ट्रॉन होते हैं। यह न तो चार इलेक्ट्रॉन त्याग सकता है और न ही ग्रहण कर सकता है, क्योंकि ऐसा करने में बहुत अधिक ऊर्जा लगती है। इसलिए कार्बन परमाणु इलेक्ट्रॉन साझा करके सहसंयोजक बंध (Covalent Bond) बनाता है।
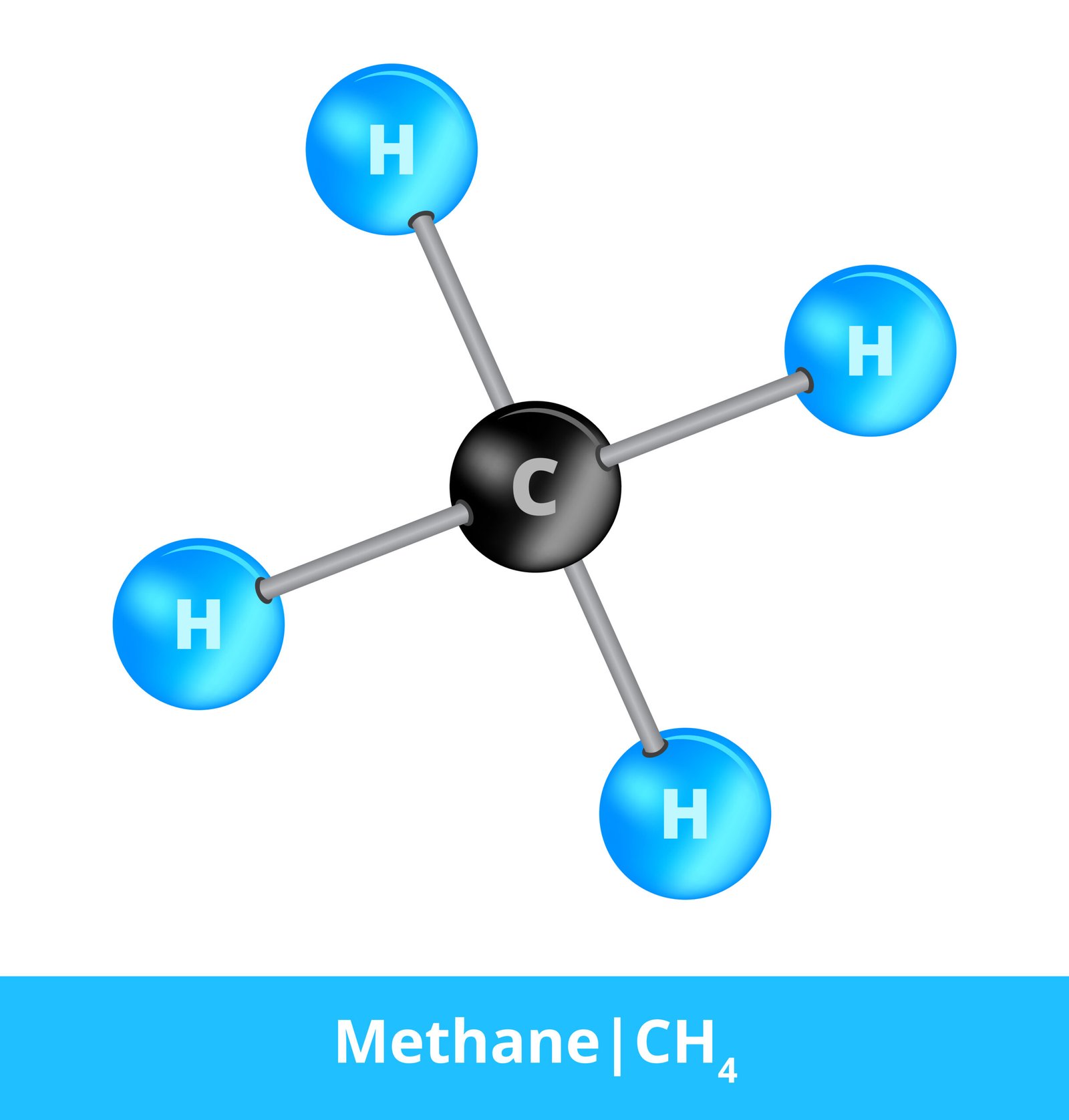
✏️ उदाहरण: मिथेन (CH₄)
यहाँ एक कार्बन परमाणु चार हाइड्रोजन परमाणुओं के साथ इलेक्ट्रॉन साझा करता है।
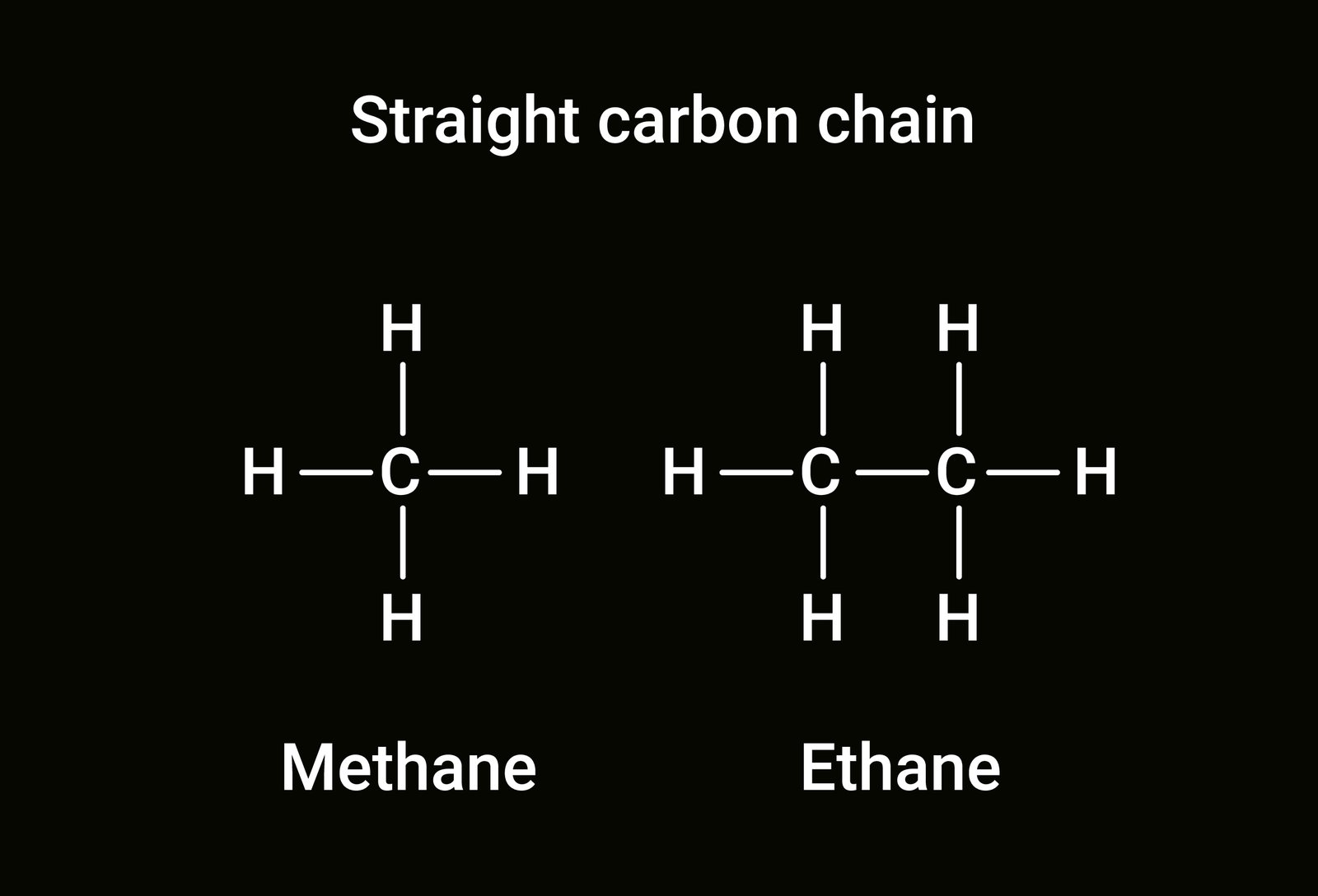
🟡 2️⃣ श्रृंखला निर्माण (Catenation)
कार्बन परमाणु आपस में जुड़कर लंबी श्रृंखलाएँ और चक्रीय संरचनाएँ बनाते हैं। यह गुण कार्बन को अनगिनत यौगिक बनाने में सक्षम बनाता है।
उदाहरण:
C–C–C–C (सीधी श्रृंखला)
या
C
│
C–C–C (शाखित श्रृंखला)
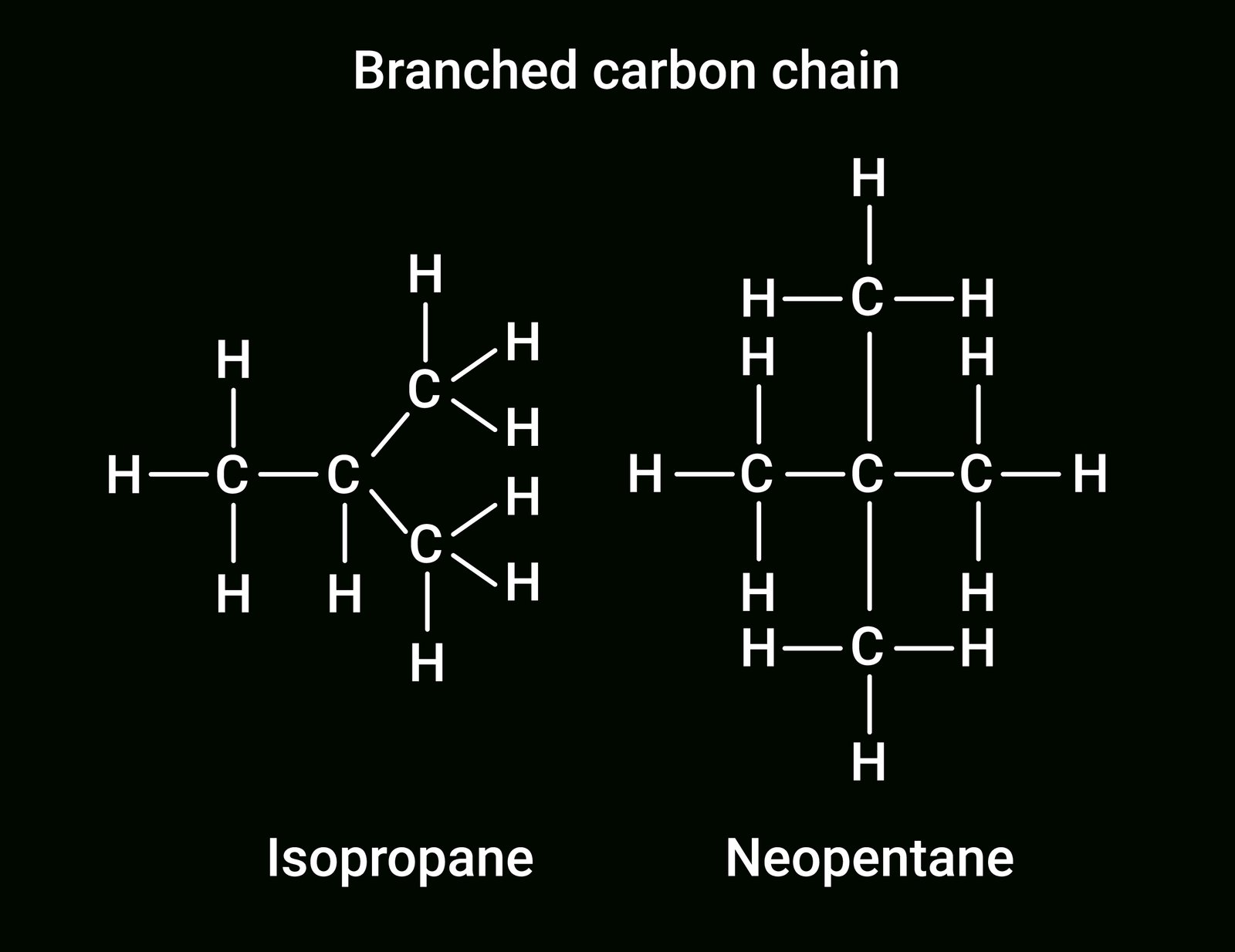
🔴 3️⃣ कार्बनिक यौगिक (Organic Compounds)
वे यौगिक जिनमें मुख्यतः कार्बन और हाइड्रोजन होते हैं, उन्हें कार्बनिक यौगिक कहा जाता है। इनमें ऑक्सीजन, नाइट्रोजन, सल्फर, क्लोरीन जैसे तत्व भी उपस्थित हो सकते हैं।
उदाहरण: CH₄ (मिथेन), C₂H₆ (एथेन), C₂H₄ (एथीन), C₂H₂ (एथाइन)
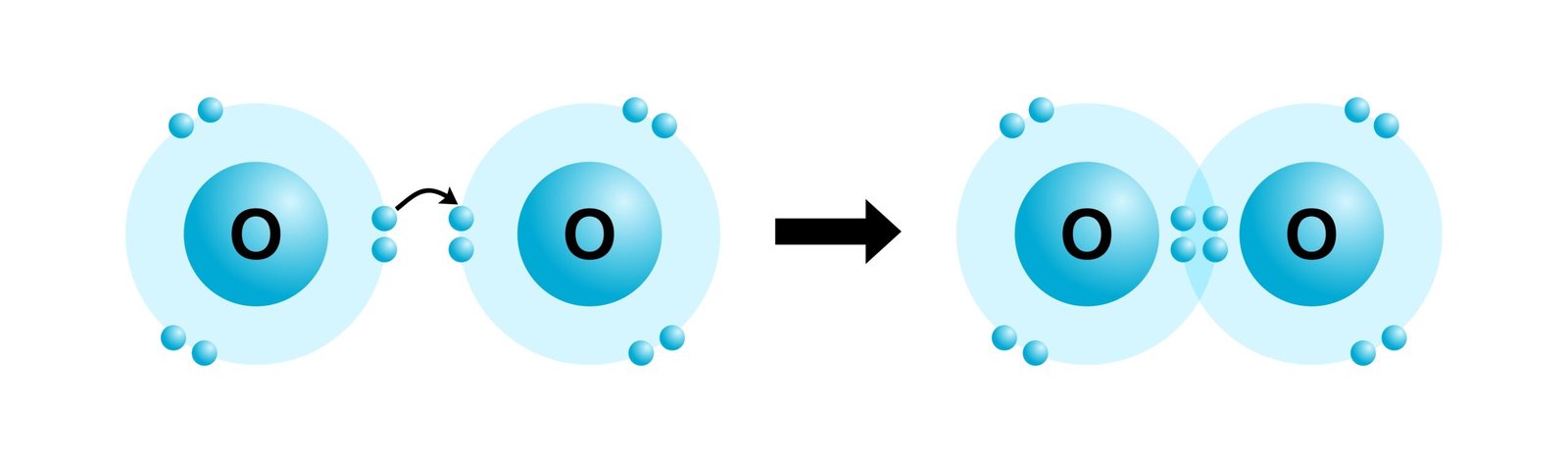
🟢 4️⃣ कार्बन के बंधों के प्रकार
✏️ एकल बंध: C–C (एथेन)
✏️ द्वि-बंध: C=C (एथीन)
✏️ त्रि-बंध: C≡C (एथाइन)

🟡 5️⃣ हाइड्रोकार्बन (Hydrocarbons)
ये केवल कार्बन और हाइड्रोजन से बने होते हैं।
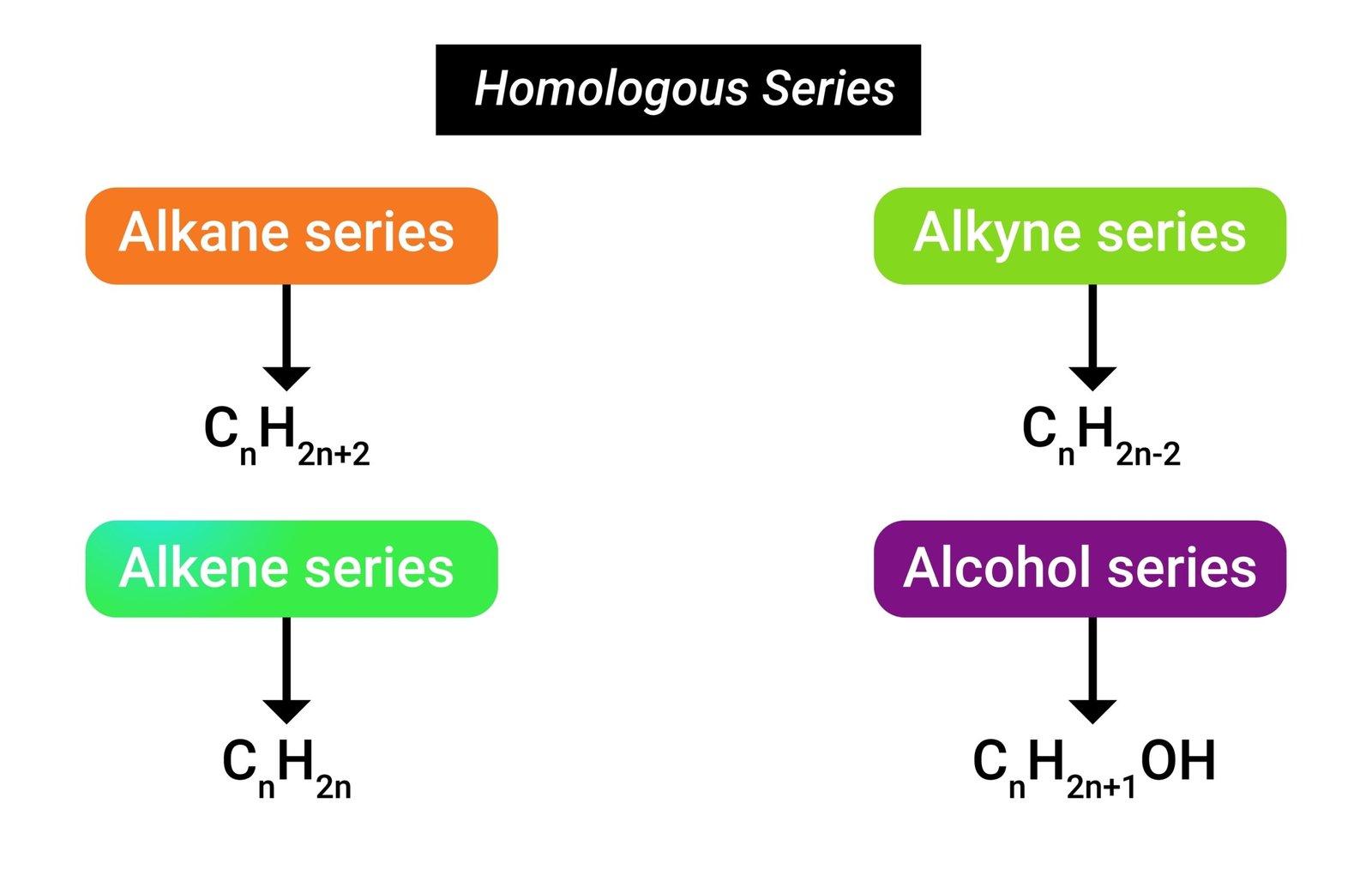
प्रकार:
1️⃣ संतृप्त हाइड्रोकार्बन (Alkanes): केवल एकल बंध होते हैं।
सामान्य सूत्र CₙH₂ₙ₊₂
उदाहरण: CH₄, C₂H₆
2️⃣ असंतृप्त हाइड्रोकार्बन (Alkenes, Alkynes): द्वि या त्रि-बंध वाले यौगिक।
उदाहरण: C₂H₄ (एथीन), C₂H₂ (एथाइन)
🔵 6️⃣ समावयवता (Isomerism)
ऐसे यौगिक जिनका आणविक सूत्र समान लेकिन संरचना भिन्न होती है, उन्हें समावयवी कहते हैं।
उदाहरण: C₄H₁₀ → n-ब्यूटेन और आइसो-ब्यूटेन
🟢 7️⃣ कार्यात्मक समूह (Functional Groups)
यह परमाणु या समूह यौगिक के गुणों को निर्धारित करते हैं।
उदाहरण:
–OH (हाइड्रॉक्सिल) → एथेनॉल
–CHO (एल्डिहाइड) → एथेनल
–CO– (कीटोन) → प्रोपेनोन
–COOH (कार्बोक्सिल) → एथेनोइक अम्ल
🟡 8️⃣ एथेनॉल (C₂H₅OH)
यह रंगहीन, वाष्पशील और ज्वलनशील द्रव है। यह जल में घुलनशील और ईंधन के रूप में प्रयोग किया जाता है।
रासायनिक अभिक्रिया: 2C₂H₅OH + 2Na → 2C₂H₅ONa + H₂↑
🔵 9️⃣ एथेनोइक अम्ल (CH₃COOH)
इसे सिरका अम्ल या एसीटिक अम्ल कहते हैं। यह तीव्र गंध वाला और जल में घुलनशील द्रव है। जब तापमान 16°C से कम होता है, यह ठोस रूप में परिवर्तित हो जाता है, जिसे बर्फीला सिरका कहा जाता है।
अभिक्रिया: CH₃COOH + NaOH → CH₃COONa + H₂O
🟢 10️⃣ साबुन और डिटर्जेंट
साबुन: वसीय अम्लों के सोडियम या पोटैशियम लवण होते हैं।
वसा + NaOH → साबुन + ग्लिसरीन
साबुन के अणु का एक भाग जल-अविलेय और दूसरा जल-विलेय होता है। यह गंदगी को घेरे रखकर माइसिल बनाता है।
डिटर्जेंट: कृत्रिम यौगिक जो कठोर जल में भी कार्य करते हैं।
🟡 11️⃣ कार्बन चक्र (Carbon Cycle)

यह एक प्राकृतिक चक्र है जिसमें वातावरण, जीव-जंतु और पौधों में कार्बन का सतत आदान-प्रदान होता है।
मुख्य चरण:
पौधे प्रकाश संश्लेषण द्वारा CO₂ को ग्लूकोज़ में बदलते हैं।
जानवर श्वसन से CO₂ पुनः वातावरण में छोड़ते हैं।
जीवाश्म ईंधनों के दहन से CO₂ बढ़ती है।
🔴 12️⃣ कार्बन के उपयोग
ऊर्जा स्रोत — कोयला, पेट्रोलियम, गैस
औद्योगिक पदार्थ — प्लास्टिक, रबर, दवाएँ
हीरा (सबसे कठोर), ग्रेफाइट (विद्युत सुचालक)
🟢 सारांश (Summary)
कार्बन की संयोजकता 4 होती है, यह सहसंयोजक बंध बनाता है।
श्रृंखला निर्माण के कारण असंख्य कार्बनिक यौगिक बनते हैं।
हाइड्रोकार्बन दो प्रकार के — संतृप्त और असंतृप्त।
कार्यात्मक समूह –OH, –CHO, –COOH, –CO– विशेष गुण देते हैं।
एथेनॉल और एथेनोइक अम्ल कार्बन के प्रमुख यौगिक हैं।
साबुन और डिटर्जेंट सफाई के लिए उपयोगी हैं।
कार्बन चक्र से पर्यावरण में संतुलन बना रहता है।
📝 Quick Recap
1️⃣ कार्बन की संयोजकता 4 होती है।
2️⃣ श्रृंखला निर्माण से लाखों यौगिक संभव हैं।
3️⃣ एथेनॉल व एथेनोइक अम्ल के व्यावहारिक उपयोग हैं।
4️⃣ साबुन व डिटर्जेंट गंदगी को हटाने के लिए माइसिल बनाते हैं।
5️⃣ कार्बन चक्र जीवन के संतुलन को बनाए रखता है।
6️⃣ हीरा और ग्रेफाइट कार्बन के दो महत्वपूर्ण रूप हैं।
✔️ Final Note:
कार्बन की बहुसंयोजकता और श्रृंखला निर्माण की क्षमता इसे “जीवन का मूल तत्व” बनाती है।
———————————————————————————————————————————————————————————————————————————————–
पाठ्यपुस्तक के प्रश्न
🔵 Question 1:
एथेन का आणविक सूत्र C₂H₆ है। इसमें —
(a) 6 सहसंयोजक आवेश हैं।
(b) 7 सहसंयोजक आवेश हैं।
(c) 8 सहसंयोजक आवेश हैं।
(d) 9 सहसंयोजक आवेश हैं।
🟢 Answer:
✔️ एथेन (C₂H₆) में 6 सहसंयोजक बंध होते हैं।
🔹 प्रत्येक कार्बन परमाणु 4 बंध बनाता है, जिनमें 3 हाइड्रोजन और 1 दूसरे कार्बन से होता है।
➡️ सही उत्तर: (a) 6 सहसंयोजक आवेश हैं।
🔵 Question 2:
ब्यूटेनोइक अम्ल–कार्बन यौगिक है, जिसका प्रमुख कार्यात्मक समूह —
(a) कार्बोक्सिलिक अम्ल (b) ऐल्डिहाइड (c) कीटोन (d) ऐल्कोहल
🟢 Answer:
✔️ ब्यूटेनोइक अम्ल में प्रमुख कार्यात्मक समूह –COOH (कार्बोक्सिलिक अम्ल) होता है।
➡️ सही उत्तर: (a) कार्बोक्सिलिक अम्ल।
🔵 Question 3:
खाना बनाते समय यदि बर्तन की तली बाहर से काली हो रही है तो इसका अर्थ है कि—
(a) ईंधन पूरी तरह नहीं जल रहा है।
(b) ईंधन पूरी तरह जल रहा है।
(c) ईंधन आई है।
(d) ईंधन पूरी तरह से जल रहा है।
🟢 Answer:
✔️ यदि बर्तन की तली काली हो रही है, तो ईंधन में अपूर्ण दहन हो रहा है।
✔️ अपूर्ण दहन से कार्बन के कण (कालिख) उत्पन्न होते हैं जो बर्तन की तली पर जमते हैं।
➡️ सही उत्तर: (a) ईंधन पूरी तरह नहीं जल रहा है।
🔵 Question 4:
CH₃Cl में आबद्ध निर्माण का उपयोग कर सहसंयोजक आवेश की प्रकृति समझाइए।
🟢 Answer:
1️⃣ CH₃Cl में कार्बन एकल बंध द्वारा तीन हाइड्रोजन और एक क्लोरीन परमाणु से जुड़ा है।
2️⃣ सभी बंध सहसंयोजक हैं, क्योंकि इनमें इलेक्ट्रॉन साझा किए गए हैं।
3️⃣ कार्बन और क्लोरीन के बीच बंध ध्रुवीय (polar) होता है क्योंकि क्लोरीन अधिक विद्युतऋणात्मक है।
🔵 Question 5:
इलेक्ट्रॉन बिंदु संरचना बनाइए —
(a) एथेनोइक अम्ल (b) H₂S (c) प्रोपेन (d) F₂
🟢 Answer:
💡 (a) एथेनोइक अम्ल (CH₃COOH):
C परमाणु चार बंध बनाता है – तीन H के साथ और एक O के साथ।
दूसरा O परमाणु –OH समूह में जुड़ा होता है।
💡 (b) H₂S:
S परमाणु दो हाइड्रोजन से जुड़ा, कुल 2 साझा इलेक्ट्रॉन युग्म।
💡 (c) प्रोपेन (C₃H₈):
C–C–C श्रृंखला, प्रत्येक कार्बन चार बंध बनाता है।
💡 (d) F₂:
दोनों F परमाणु एकल इलेक्ट्रॉन युग्म साझा करते हैं।
✔️ सभी बंध सहसंयोजक होते हैं।
🔵 Question 6:
समजातीय श्रेणी क्या है? उदाहरण सहित समझाइए।
🟢 Answer:
1️⃣ समजातीय श्रेणी वह समूह है जिसमें यौगिकों के गुण क्रमिक रूप से बदलते हैं।
2️⃣ प्रत्येक सदस्य में एक –CH₂– इकाई का अंतर होता है।
✏️ उदाहरण:
मीथेन (CH₄), एथेन (C₂H₆), प्रोपेन (C₃H₈) – ये सभी एक समजातीय श्रेणी बनाते हैं।
🔵 Question 7:
भौतिक और रासायनिक गुणों के आधार पर एथेनॉल और एथेनोइक अम्ल में अंतर कीजिए।
🟢 Answer:
1️⃣ एथेनॉल रंगहीन, ज्वलनशील और तटस्थ द्रव है।
2️⃣ एथेनोइक अम्ल तीव्र गंध वाला, अम्लीय स्वभाव का होता है।
3️⃣ एथेनॉल ईंधन और औषधि में, जबकि एथेनोइक अम्ल सिरके में प्रयुक्त होता है।
🔵 Question 8:
जब एथेनॉल में सोडियम डाला जाता है तो गैस उत्पन्न होती है। यह गैस कौन-सी है?
🟢 Answer:
अभिक्रिया: 2C₂H₅OH + 2Na → 2C₂H₅ONa + H₂↑
✔️ यहाँ हाइड्रोजन गैस उत्पन्न होती है।
🔵 Question 9:
कार्बन एवं उसके यौगिकों का उपयोग औद्योगिक कार्यों में क्यों किया जाता है?
🟢 Answer:
1️⃣ कार्बन के यौगिक जैसे ईंधन (कोयला, पेट्रोलियम, गैस) ऊर्जा स्रोत हैं।
2️⃣ कार्बन प्लास्टिक, रबर, डिटर्जेंट, औषधि आदि में प्रयुक्त होता है।
✔️ इसलिए यह औद्योगिक रूप से अत्यंत महत्वपूर्ण तत्व है।
🔵 Question 10:
साबुन और डिटर्जेंट के निर्माण की विधि समझाइए।
🟢 Answer:
1️⃣ साबुन: वसीय अम्ल + NaOH → साबुन + ग्लिसरीन।
2️⃣ डिटर्जेंट: पेट्रोलियम से बने कृत्रिम पदार्थ जो कठोर जल में भी कार्य करते हैं।
✔️ दोनों ही माइसिल सिद्धांत के अनुसार सफाई करते हैं।
🔵 Question 11:
कठोर जल में साबुन झाग क्यों नहीं बनाता?
🟢 Answer:
1️⃣ कठोर जल में Ca²⁺ और Mg²⁺ आयन होते हैं।
2️⃣ ये आयन साबुन के साथ अस्थुल लवण बनाते हैं।
3️⃣ परिणामस्वरूप झाग नहीं बनता और सफाई कम हो जाती है।
🔵 Question 12:
समावयवता क्या है? उदाहरण दीजिए।
🟢 Answer:
1️⃣ जिन यौगिकों का आणविक सूत्र समान लेकिन संरचना भिन्न होती है, उन्हें समावयवी कहते हैं।
2️⃣ ✏️ उदाहरण: C₄H₁₀ → n-ब्यूटेन और आइसो-ब्यूटेन।
🔵 Question 13:
दिए गए हाइड्रोकार्बन CH₃CH₂CH₂CH₃ और CH₃CH(CH₃)CH₃ में किसमें समावयवता होती है?
🟢 Answer:
✔️ दोनों का आणविक सूत्र C₄H₁₀ समान है पर संरचना भिन्न।
✔️ इस कारण ये एक-दूसरे के समावयवी हैं।
🔵 Question 14:
एथेन और एथीन की रासायनिक क्रियाओं में क्या अंतर है?
🟢 Answer:
1️⃣ एथेन में सभी एकल बंध होते हैं, अतः यह स्थिर होता है।
2️⃣ एथीन में द्वि-बंध होने से यह अधिक अभिक्रियाशील होता है।
✔️ इसलिए एथीन हाइड्रोजन के साथ योग-अभिक्रिया करता है जबकि एथेन नहीं।
🔵 Question 15:
साबुन की क्रिया प्रक्रिया की क्रियाविधि समझाइए।
🟢 Answer:
1️⃣ साबुन के अणु का एक भाग जल-अविलेय और दूसरा जल-विलेय होता है।
2️⃣ यह तेल या चिकनाई के चारों ओर माइसिल बनाता है।
3️⃣ माइसिल गंदगी को पानी के साथ बाहर निकाल देता है।
✔️ यही सफाई की वैज्ञानिक प्रक्रिया है।
————————————————————————————————————————————————————————————————————————————
अन्य महत्वपूर्ण प्रश्न
(CBSE MODEL प्रश्न पत्र)
सिर्फ इसी पाठ से निर्मित CBSE MODEL प्रश्न पत्र
🔵 Section A (Q1–6): बहुत लघु उत्तर / वस्तुनिष्ठ प्रश्न (1 अंक प्रत्येक)
🔵 Question 1: कार्बन की संयोजकता कितनी होती है?
🟢 Answer: कार्बन की संयोजकता 4 होती है क्योंकि इसमें 4 संयोजक इलेक्ट्रॉन होते हैं।
🔵 Question 2: कार्बन किस प्रकार का बंध बनाता है?
🟢 Answer: कार्बन सहसंयोजक बंध (Covalent bond) बनाता है।
🔵 Question 3: मिथेन का आणविक सूत्र लिखिए।
🟢 Answer: मिथेन का सूत्र CH₄ है।
🔵 Question 4: एथेनोइक अम्ल को और क्या कहा जाता है?
🟢 Answer: इसे सिरका अम्ल या एसीटिक अम्ल कहा जाता है।
🔵 Question 5: साबुन किससे बनता है?
🟢 Answer: साबुन वसीय अम्लों के सोडियम या पोटैशियम लवण से बनता है।
🔵 Question 6: हीरा और ग्रेफाइट किस तत्व के रूप हैं?
🟢 Answer: दोनों कार्बन के रूप हैं।
🟢 Section B (Q7–12): लघु उत्तर प्रकार-I (2 अंक प्रत्येक)
🟢 Question 7: मिथेन गैस के अणु में बनने वाले बंधों का प्रकार बताइए।
🔵 Answer: मिथेन (CH₄) में एक कार्बन परमाणु चार हाइड्रोजन परमाणुओं से चार एकल सहसंयोजक बंध बनाता है।
🟢 Question 8: कार्बन तत्व को जीवन का आधार क्यों कहा जाता है?
🔵 Answer:
1️⃣ कार्बन 4 संयोजकता वाला तत्व है, जिससे यह अनेक यौगिक बना सकता है।
2️⃣ यह श्रृंखला निर्माण की क्षमता रखता है और लाखों प्रकार के जैविक यौगिक बनाता है।
🟢 Question 9: एथेनॉल के दो उपयोग लिखिए।
🔵 Answer:
1️⃣ यह ईंधन के रूप में प्रयुक्त होता है।
2️⃣ यह औषधियों और इत्रों के निर्माण में काम आता है।
🟢 Question 10: एथेनोइक अम्ल की एक अभिक्रिया लिखिए।
🔵 Answer: CH₃COOH + NaOH → CH₃COONa + H₂O
🟢 Question 11: समावयवता क्या है?
🔵 Answer: समान आणविक सूत्र लेकिन भिन्न संरचना वाले यौगिकों को समावयवी कहते हैं।
✏️ उदाहरण: C₄H₁₀ — n-ब्यूटेन और आइसो-ब्यूटेन।
🟢 Question 12: कार्बन चक्र से हमें क्या लाभ होता है?
🔵 Answer: यह वातावरण में CO₂ का संतुलन बनाए रखता है जिससे जीवन की निरंतरता बनी रहती है।
🟡 Section C (Q13–22): लघु उत्तर प्रकार-II (3 अंक प्रत्येक)
🔵 Question 13: मिथेन (CH₄) में बंधों की प्रकृति का वर्णन कीजिए।
🟢 Answer:
1️⃣ मिथेन में एक कार्बन परमाणु चार हाइड्रोजन परमाणुओं से जुड़ा होता है।
2️⃣ हर C–H बंध एकल सहसंयोजक बंध होता है जो इलेक्ट्रॉनों के साझा करने से बनता है।
3️⃣ इस प्रकार CH₄ अणु एक संतृप्त हाइड्रोकार्बन है जिसमें सभी बंध एकल हैं।
🔵 Question 14: संतृप्त और असंतृप्त हाइड्रोकार्बनों में क्या अंतर है?
🟢 Answer:
1️⃣ संतृप्त हाइड्रोकार्बन: इनमें केवल एकल बंध (C–C) होते हैं।
✏️ उदाहरण: एथेन (C₂H₆)
2️⃣ असंतृप्त हाइड्रोकार्बन: इनमें द्वि या त्रि बंध (C=C, C≡C) होते हैं।
✏️ उदाहरण: एथीन (C₂H₄), एथाइन (C₂H₂)
3️⃣ संतृप्त हाइड्रोकार्बन स्थिर होते हैं जबकि असंतृप्त अपेक्षाकृत अधिक अभिक्रियाशील होते हैं।
🔵 Question 15: कार्यात्मक समूह क्या होता है? उदाहरण सहित समझाइए।
🟢 Answer:
1️⃣ कोई भी ऐसा परमाणु या परमाणुओं का समूह जो यौगिक के रासायनिक गुणों को निर्धारित करता है, कार्यात्मक समूह कहलाता है।
2️⃣ ✏️ उदाहरण:
–OH (हाइड्रॉक्सिल समूह) → एथेनॉल (C₂H₅OH)
–COOH (कार्बोक्सिल समूह) → एथेनोइक अम्ल (CH₃COOH)
3️⃣ ये समूह यौगिक की अभिक्रियाशीलता और प्रकृति तय करते हैं।
🔵 Question 16: एथेनॉल की किसी एक रासायनिक अभिक्रिया को समीकरण सहित समझाइए।
🟢 Answer:
एथेनॉल सोडियम के साथ अभिक्रिया करता है —
🔹 अभिक्रिया: 2C₂H₅OH + 2Na → 2C₂H₅ONa + H₂↑
🔹 यहाँ हाइड्रोजन गैस उत्सर्जित होती है और सोडियम एथॉक्साइड बनता है।
✔️ यह अभिक्रिया धातुओं के साथ एथेनॉल की क्रियाशीलता दर्शाती है।
🔵 Question 17: साबुन और डिटर्जेंट में क्या अंतर है?
🟢 Answer:
1️⃣ साबुन: यह वसीय अम्लों के सोडियम या पोटैशियम लवण होते हैं और नरम जल में काम करते हैं।
2️⃣ डिटर्जेंट: यह कृत्रिम रासायनिक पदार्थ हैं जो कठोर जल में भी सफाई कर सकते हैं।
3️⃣ साबुन जैव-अवक्रमणीय होते हैं जबकि डिटर्जेंट नहीं।
🔵 Question 18: कार्बन चक्र का वर्णन कीजिए।
🟢 Answer:
1️⃣ कार्बन चक्र एक प्राकृतिक प्रक्रिया है जिसमें कार्बन का स्थानांतरण वातावरण, पौधों, जानवरों और मिट्टी के बीच होता है।
2️⃣ पौधे CO₂ को प्रकाश संश्लेषण से ग्लूकोज़ में बदलते हैं।
3️⃣ जीवाश्म ईंधन के दहन और श्वसन से CO₂ पुनः वातावरण में जाती है।
✔️ यह चक्र वायुमंडलीय CO₂ का संतुलन बनाए रखता है।
🔵 Question 19: एथेनोइक अम्ल की दो विशेषताएँ लिखिए।
🟢 Answer:
1️⃣ यह तीव्र गंध वाला पारदर्शी द्रव है जो जल में घुलनशील है।
2️⃣ यह अम्लीय प्रकृति का होता है और धातुओं के साथ अभिक्रिया करके हाइड्रोजन गैस उत्सर्जित करता है।
🔵 Question 20: एथेनोइक अम्ल और सोडियम कार्बोनेट की अभिक्रिया का समीकरण लिखिए।
🟢 Answer:
2CH₃COOH + Na₂CO₃ → 2CH₃COONa + H₂O + CO₂↑
✔️ इस अभिक्रिया में कार्बन डाइऑक्साइड गैस उत्पन्न होती है।
🔵 Question 21: कार्बन के दो अपरूपों (Allotropes) का नाम लिखिए और उनके गुण बताइए।
🟢 Answer:
1️⃣ हीरा: कठोर, पारदर्शी और ऊष्मा सुचालक।
2️⃣ ग्रेफाइट: काला, विद्युत सुचालक और मुलायम।
💡 दोनों ही कार्बन के शुद्ध रूप हैं लेकिन परमाणु संरचना भिन्न होती है।
🔵 Question 22: यदि किसी जल में साबुन झाग नहीं बनाता तो इसका क्या कारण है?
🟢 Answer:
1️⃣ कठोर जल में Ca²⁺ और Mg²⁺ आयन होते हैं जो साबुन के साथ अस्थुल लवण बनाते हैं।
2️⃣ इससे झाग नहीं बन पाता और सफाई घट जाती है।
3️⃣ इस कारण कठोर जल में साबुन की प्रभावशीलता कम हो जाती है।
🔴 Section D (Q23–30): दीर्घ उत्तर प्रकार प्रश्न (4 अंक प्रत्येक)
🔵 Question 23: कार्बन की सहसंयोजकता की व्याख्या कीजिए और मिथेन के निर्माण को चित्र सहित समझाइए।
🟢 Answer:
1️⃣ कार्बन का परमाणु क्रमांक 6 है तथा उसकी इलेक्ट्रॉनिक संरचना 2,4 होती है।
2️⃣ इसमें 4 संयोजक इलेक्ट्रॉन होते हैं, इसलिए यह चार सहसंयोजक बंध बना सकता है।
3️⃣ यह न तो इलेक्ट्रॉन ग्रहण करता है और न त्यागता है, बल्कि साझेदारी करता है।
4️⃣ मिथेन (CH₄) के निर्माण में एक कार्बन परमाणु चार हाइड्रोजन परमाणुओं के साथ चार एकल सहसंयोजक बंध बनाता है।
💡 चित्र वर्णन:
C परमाणु बीच में स्थित होता है और चारों ओर 4 H परमाणु होते हैं, प्रत्येक C–H एकल सहसंयोजक बंध बनाता है।
✔️ निष्कर्ष: मिथेन एक स्थिर, संतृप्त, सहसंयोजक यौगिक है।
🔵 Question 24: एथेनॉल और एथेनोइक अम्ल के गुणों तथा उपयोगों की तुलना कीजिए।
🟢 Answer:
1️⃣ एथेनॉल (C₂H₅OH):
• यह रंगहीन, वाष्पशील, ज्वलनशील द्रव है।
• जल में घुलनशील है और ईंधन के रूप में प्रयुक्त होता है।
• औषधि, इत्र व जीवाणुनाशक के रूप में उपयोगी।
2️⃣ एथेनोइक अम्ल (CH₃COOH):
• यह तीव्र गंध वाला पारदर्शी द्रव है।
• यह जल में घुलनशील और अम्लीय स्वभाव का होता है।
• सिरके में 5–8% एथेनोइक अम्ल पाया जाता है।
3️⃣ समानता:
दोनों में कार्बन, हाइड्रोजन और ऑक्सीजन तत्व होते हैं।
4️⃣ अंतर:
एथेनॉल तटस्थ जबकि एथेनोइक अम्ल अम्लीय स्वभाव का होता है।
🔵 Question 25: कार्बन के अपरूपों (Allotropes) की तुलना कीजिए।
🟢 Answer:
1️⃣ हीरा (Diamond):
• पारदर्शी, बहुत कठोर और ऊष्मा सुचालक।
• प्रत्येक कार्बन परमाणु 4 अन्य से जुड़ा होता है।
• प्रयोग: काटने के औज़ार, आभूषण।
2️⃣ ग्रेफाइट (Graphite):
• काला, मुलायम और विद्युत सुचालक।
• प्रत्येक कार्बन परमाणु 3 अन्य से जुड़ा होता है और परतों के रूप में व्यवस्थित होता है।
• प्रयोग: पेंसिल की निब, विद्युत-ध्रुव।
3️⃣ फुलरीन (Fullerene):
• अणु गोलाकार पिंजरे जैसा होता है (C₆₀)।
• प्रयोग: औषधीय अनुसंधान व नैनोटेक्नोलॉजी।
✔️ निष्कर्ष: कार्बन के अलग-अलग अपरूप उसकी संयोजकता और परमाण्विक व्यवस्था के कारण विभिन्न गुण प्रदर्शित करते हैं।
🔵 Question 26: कार्बन चक्र को समझाइए और इसका महत्व बताइए।
🟢 Answer:
1️⃣ कार्बन चक्र एक प्राकृतिक प्रक्रिया है जिसमें कार्बन का सतत स्थानांतरण वातावरण, पौधों, प्राणियों और मिट्टी में होता है।
2️⃣ पौधे प्रकाश संश्लेषण से CO₂ को ग्लूकोज़ में बदलते हैं।
3️⃣ जानवर श्वसन के माध्यम से CO₂ पुनः वातावरण में छोड़ते हैं।
4️⃣ जीवाश्म ईंधन के दहन से भी CO₂ बढ़ती है।
✔️ महत्व:
• यह वातावरण में CO₂ का संतुलन बनाए रखता है।
• पौधों द्वारा ऑक्सीजन उत्सर्जन सुनिश्चित करता है।
• पारिस्थितिक संतुलन के लिए आवश्यक है।
🔵 Question 27: साबुन की क्रिया-विधि को माइसिल सिद्धांत के आधार पर समझाइए।
🟢 Answer:
1️⃣ साबुन के अणु का एक भाग जल-विलेय (Hydrophilic) और दूसरा जल-अविलेय (Hydrophobic) होता है।
2️⃣ जब साबुन को जल में घोला जाता है, तो यह गंदगी के चारों ओर माइसिल (Micelle) बनाता है।
3️⃣ माइसिल का जल-अविलेय भाग तेल के कणों से जुड़ता है जबकि जल-विलेय भाग पानी में रहता है।
4️⃣ धोते समय यह गंदगी को पानी के साथ बाहर निकाल देता है।
✔️ निष्कर्ष: माइसिल निर्माण की यही क्रिया सफाई का वैज्ञानिक कारण है।
🔵 Question 28: कार्बन के सहसंयोजक बंधों के गुण और उदाहरण बताइए।
🟢 Answer:
1️⃣ गुण:
• ये बंध मजबूत होते हैं।
• इनमें विद्युत आवेश का स्थानांतरण नहीं होता।
• ये विद्युत के सुचालक नहीं होते।
2️⃣ उदाहरण: मिथेन (CH₄), एथेन (C₂H₆), एथेनॉल (C₂H₅OH)।
3️⃣ निष्कर्ष: सहसंयोजक बंध कार्बन यौगिकों को स्थायित्व प्रदान करते हैं और उन्हें जीवनोपयोगी बनाते हैं।
🔵 Question 29: एथेनॉल के उपयोगों और दुष्प्रभावों को समझाइए।
🟢 Answer:
1️⃣ उपयोग:
• औषधि, इत्र और ईंधन के रूप में।
• हाथ सैनिटाइज़र और क्लीनिंग एजेंट में।
2️⃣ दुष्प्रभाव:
• अत्यधिक सेवन से यकृत (लीवर) को हानि होती है।
• यह मस्तिष्क की कार्यक्षमता को घटाता है।
✔️ निष्कर्ष: एथेनॉल का नियंत्रित उपयोग उपयोगी है परंतु अधिकता हानिकारक।
🔵 Question 30: कार्बन यौगिकों की विविधता के कारणों की व्याख्या कीजिए।
🟢 Answer:
1️⃣ कार्बन की चार संयोजकता (C valency = 4) इसे अनेक तत्वों से जुड़ने में सक्षम बनाती है।
2️⃣ इसमें श्रृंखला निर्माण (Catenation) की क्षमता है।
3️⃣ यह एकल, द्वि और त्रि बंध बना सकता है।
4️⃣ विभिन्न कार्यात्मक समूहों (–OH, –COOH, –CHO) से यह लाखों भिन्न यौगिक बना सकता है।
✔️ निष्कर्ष: इन्हीं कारणों से कार्बन को बहुमुखी तत्व कहा जाता है और यह जैविक रसायन का आधार है।
————————————————————————————————————————————————————————————————————————————
मस्तिष्क मानचित्र
————————————————————————————————————————————————————————————————————————————
