Class 12 : Chemistry (Hindi) – Lesson 5.उपसहसंयोजन यौगिक
पाठ का विश्लेषण एवं विवेचन
🔵 प्रस्तावना:
उपसहसंयोजन यौगिक (समन्वय यौगिक) वे यौगिक हैं जिनमें एक केन्द्रीय परमाणु या आयन (प्रायः संक्रमण धातु) कुछ अणुओं या आयनों से जुड़ा होता है जिन्हें लिगैण्ड कहा जाता है। ये यौगिक जटिल संरचना वाले होते हैं और इनका व्यवहार साधारण आयनिक यौगिकों से भिन्न होता है।
📍 उदाहरण – [Cu(NH₃)₄]SO₄, [Fe(CN)₆]³⁻, [Co(NH₃)₆]Cl₃, [Ag(NH₃)₂]Cl।
🟢 उपसहसंयोजन यौगिकों के घटक भाग:
1️⃣ केन्द्रीय धात्विक आयन या परमाणु:
यह वह अणु होता है जो लिगैण्डों को अपनी रिक्त कक्षिकाओं के माध्यम से ग्रहण करता है।
📘 उदाहरण – Co³⁺, Fe²⁺, Ni²⁺।
2️⃣ लिगैण्ड (Ligand):
वे अणु या आयन जो केन्द्रीय धातु को इलेक्ट्रॉन युग्म प्रदान करते हैं।
📐 इन्हें लुईस क्षारक (Lewis base) कहा जाता है।
✔ प्रकार:
एकदन्ती (Monodentate): जो केवल एक बन्ध बनाते हैं।
📌 उदाहरण – H₂O, NH₃, Cl⁻, CN⁻।
द्विदन्ती (Bidentate): जो दो बन्ध बनाते हैं।
📌 उदाहरण – C₂O₄²⁻ (ऑक्सालेट), en (एथिलीन डायमीन)।
बहुदन्ती (Polydentate): एक से अधिक बन्ध।
📘 उदाहरण – EDTA⁴⁻ (हेक्सादन्ती)।
द्विसंयोजी लिगैण्ड: जब एक ही अणु के दो भाग अलग-अलग धातु से जुड़ें।
3️⃣ समन्वय संख्या (Coordination Number):
यह वह संख्या है जो बताती है कि केन्द्रीय धातु से कितने लिगैण्ड-परमाणु सीधे जुड़े हैं।
📘 उदाहरण –
[Co(NH₃)₆]³⁺ में समन्वय संख्या = 6
[Ag(NH₃)₂]⁺ में = 2
4️⃣ समन्वय गोला (Coordination Sphere):
केन्द्रीय धातु और उससे जुड़े लिगैण्डों का समूह कोष्ठक ([ ]) में रखा जाता है — यही समन्वय गोला कहलाता है।
इसके बाहर स्थित आयन सहयौगिक या आयनिक गोला बनाते हैं।
📌 उदाहरण – [Cu(NH₃)₄]SO₄ में [Cu(NH₃)₄]²⁺ समन्वय गोला है और SO₄²⁻ आयनिक गोला।
5️⃣ लिगैण्ड का द्विदिश स्वभाव:
लिगैण्ड इलेक्ट्रॉन दाता (Lewis base) होते हैं, जबकि धातु इलेक्ट्रॉन ग्राही (Lewis acid)।
🟡 उदाहरण द्वारा व्याख्या:
📘 [Co(NH₃)₆]Cl₃ → Co³⁺ + 6NH₃
समन्वय संख्या = 6
यह आयनिक यौगिक विद्युत अपघटन में 3Cl⁻ आयन देता है।
🟣 नामकरण (Nomenclature) के नियम:
1️⃣ धनायनिक भाग पहले, फिर ऋणायनिक भाग लिखा जाए।
2️⃣ समन्वय गोले के अन्दर लिगैण्डों के नाम वर्णानुक्रम में।
3️⃣ एक ही प्रकार के एक से अधिक लिगैण्ड के लिए उपसर्ग – di, tri, tetra, penta, hexa।
4️⃣ यदि लिगैण्ड का नाम पहले से ही di, tri आदि रखता हो, तो bis, tris, tetrakis उपसर्ग।
5️⃣ ऋणायनिक यौगिक के धातु नाम के अंत में –ate जोड़ा जाता है।
6️⃣ धातु की ऑक्सीकरण अवस्था रोमन अंकों में (III, II, IV)।
📘 उदाहरण:
[Co(NH₃)₆]Cl₃ → Hexaamminecobalt(III) chloride
[Cu(NH₃)₄]SO₄ → Tetraamminecopper(II) sulfate
K₄[Fe(CN)₆] → Potassium hexacyanoferrate(II)
🟢 संरचना एवं बन्धन के सिद्धान्त:
🔹 वर्नर का सिद्धान्त (Werner’s Theory):
📍 (1893) में प्रस्तुत किया गया।
✔ मुख्य बिन्दु:
धातु की दो संयोजकताएँ होती हैं –
(a) प्राथमिक (ionizable)
(b) द्वितीयक (non-ionizable)
प्राथमिक संयोजकता आयनिक रूप से बाहर होती है और द्वितीयक समन्वय गोले के अन्दर।
समन्वय संख्या निश्चित होती है।
लिगैण्ड द्वितीयक संयोजकता से जुड़े होते हैं।
📘 उदाहरण:
[Co(NH₃)₆]Cl₃
→ 3Cl⁻ आयन प्राथमिक संयोजकता (आयनित)
→ 6NH₃ द्वितीयक संयोजकता (समन्वय गोले के भीतर)।
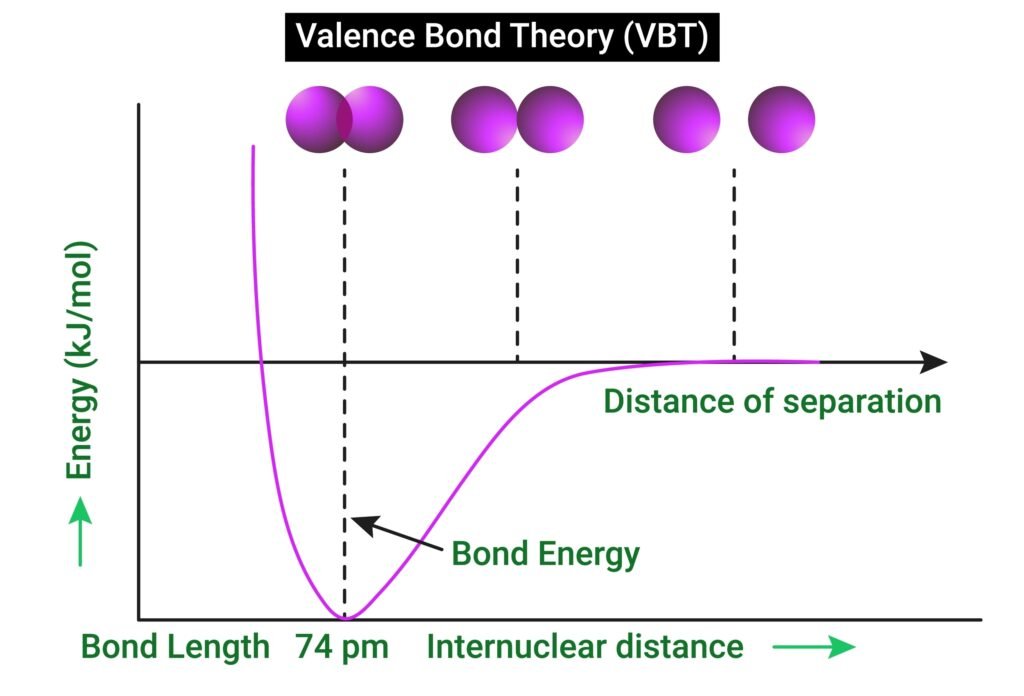
🔹 संयोजन (Valence Bond Theory – VBT):
📘 यह बताती है कि धातु अपने रिक्त कक्षिकाओं का संकरण (hybridization) करके लिगैण्डों से σ-बन्ध बनाती है।
समन्वय संख्या संकरण आकृति
2 sp रेखीय
4 dsp² या sp³ चतुर्भुज या चतुष्फलकीय
6 d²sp³ या sp³d² अष्टफलक
📍 उदाहरण:
[Ni(CN)₄]²⁻ → dsp² → वर्गाकार
[NiCl₄]²⁻ → sp³ → चतुष्फलकीय
📌 यह सिद्धान्त चुंबकत्व भी समझाता है –
यदि संकरण में सभी इलेक्ट्रॉन युग्मित हों → डायामैग्नेटिक
यदि कुछ अविवाहित हों → पराचुम्बकीय
🔹 क्रिस्टल क्षेत्र सिद्धान्त (Crystal Field Theory – CFT):
📘 लिगैण्ड के ऋणावेश व धातु के धनावेश के बीच विद्युत-स्थैतिक आकर्षण से बने क्षेत्र (Field) को क्रिस्टल क्षेत्र कहते हैं।
💡 CFT के अनुसार, जब लिगैण्ड धातु के पास आते हैं तो d-कक्षिकाएँ दो समूहों में विभाजित हो जाती हैं —
📐 अष्टफलीय (Octahedral):
t₂g (निम्न ऊर्जा) – dxy, dyz, dxz
eg (उच्च ऊर्जा) – dx²−y², dz²
📘 विभाजन की ऊर्जा → Δ₀ (क्रिस्टल क्षेत्र विभाजन ऊर्जा)।
✔ यदि Δ₀ बड़ा → युग्मन → नीचला स्पिन
यदि Δ₀ छोटा → अविवाहित इलेक्ट्रॉन → उच्च स्पिन
📌 उदाहरण:
[Fe(CN)₆]³⁻ → Δ₀ बड़ा → सभी युग्मित (नीचला स्पिन)
[Fe(H₂O)₆]³⁺ → Δ₀ छोटा → अविवाहित (उच्च स्पिन)
🔹 क्रिस्टल क्षेत्र स्थिरीकरण ऊर्जा (CFSE):
📐 CFSE = (nₜ₂g × 0.4Δ₀) − (nₑg × 0.6Δ₀)
यह ऊर्जा यौगिक की स्थिरता को मापती है।
🔹 लिगैण्ड क्षेत्र की शक्ति (Spectrochemical Series):
लिगैण्डों का Δ₀ बढ़ाने की क्षमता के अनुसार क्रम —
I⁻ < Br⁻ < Cl⁻ < F⁻ < H₂O < NH₃ < en < CN⁻ < CO
📘 बाएँ → कमजोर क्षेत्र
📘 दाएँ → प्रबल क्षेत्र
🟡 समावयवता (Isomerism):
समन्वय यौगिकों में संरचना या संयोजन भिन्न होने पर विभिन्न समावयव बनते हैं।
📍 प्रकार:
1️⃣ संरचनात्मक समावयव (Structural):
आयनीकरण समावयवता (Ionization): [Co(NH₃)₅Br]SO₄ ↔ [Co(NH₃)₅SO₄]Br
समन्वय समावयवता (Coordination): [Co(NH₃)₆][Cr(CN)₆] ↔ [Cr(NH₃)₆][Co(CN)₆]
लिगैण्ड समावयवता (Linkage): [Co(NO₂)(NH₃)₅]Cl₂ ↔ [Co(ONO)(NH₃)₅]Cl₂
सॉल्वेशन (Hydrate): [Cr(H₂O)₆]Cl₃ ↔ [Cr(H₂O)₅Cl]Cl₂·H₂O
2️⃣ स्थानिक समावयव (Stereoisomerism):
ज्यामितीय: cis / trans
📘 उदाहरण – [Pt(NH₃)₂Cl₂] → cis (एक ही ओर) / trans (विपरीत ओर)
प्रकाशीय (Optical):
जब यौगिक दर्पण-प्रतिबिंब असममिति दिखाता है।
📘 उदाहरण – [Co(en)₃]³⁺ → d और l रूप।
🟢 रंगीन यौगिकों का कारण:
CFT के अनुसार, d–d इलेक्ट्रॉन संक्रमण से रंग उत्पन्न होता है।
Δ₀ के अनुसार अवशोषित प्रकाश की तरंगदैर्घ्य बदलती है।
📘 उदाहरण:
[Ti(H₂O)₆]³⁺ – बैंगनी (Δ₀ मध्यम)
[Cu(H₂O)₆]²⁺ – नीला
पूर्ण d¹⁰ या d⁰ आयन रंगहीन होते हैं (Zn²⁺, Sc³⁺)।
🟣 उत्प्रेरक क्रिया में समन्वय यौगिकों की भूमिका:
कई संक्रमण धातु यौगिक उत्प्रेरक के रूप में कार्य करते हैं क्योंकि वे इलेक्ट्रॉन विनिमय कर सकते हैं।
📘 उदाहरण:
PtCl₂(NH₃)₂ – कैंसर-रोधी औषधि।
Ni(CO)₄ – निकेल शोधन में।
Fe(CN)₆³⁻ / Fe(CN)₆⁴⁻ – रेडॉक्स अभिक्रियाओं में।
🟢 महत्त्वपूर्ण प्रयोग:
1️⃣ चिकित्सा में:
Cisplatin (Pt(NH₃)₂Cl₂) कैंसर-रोधी औषधि।
2️⃣ विश्लेषणात्मक रसायन में:
[Fe(CN)₆]³⁻ और [Fe(CN)₆]⁴⁻ के रंग परिवर्तन से आयनों की पहचान।
3️⃣ उद्योग में:
Ni(CO)₄ द्वारा धातु शोधन (Mond प्रक्रिया)।
4️⃣ कृषि में:
सूक्ष्म पोषक तत्वों की आपूर्ति हेतु Fe, Cu यौगिक।
🔵 संक्षिप्त तथ्य सारणी:
गुणधर्म उदाहरण कारण
रंग [Cu(H₂O)₆]²⁺ नीला d–d संक्रमण
चुम्बकत्व [Fe(H₂O)₆]²⁺ पराचुम्बकीय अविवाहित इलेक्ट्रॉन
समावयवता [Pt(NH₃)₂Cl₂] cis/trans
प्रकाशीयता [Co(en)₃]³⁺ असममिति
उत्प्रेरक [PtCl₂(NH₃)₂] इलेक्ट्रॉन दान/ग्रहण
🔹 II. पाठ का सारांश
🔵 उपसहसंयोजन यौगिकों में केन्द्रीय धातु आयन कुछ लिगैण्डों से जुड़ा होता है जो इलेक्ट्रॉन युग्म प्रदान करते हैं। ये यौगिक संक्रमण धातुओं के कारण रंगीन और जटिल होते हैं।
🟢 लिगैण्ड एकदन्ती (NH₃, H₂O), द्विदन्ती (en, C₂O₄²⁻) या बहुदन्ती (EDTA⁴⁻) हो सकते हैं। समन्वय संख्या वह संख्या है जो धातु से जुड़े लिगैण्ड परमाणुओं की होती है।
🟡 नामकरण में लिगैण्डों के नाम वर्णानुक्रम में और धातु की ऑक्सीकरण अवस्था रोमन अंकों में दी जाती है।
🔴 वर्नर के सिद्धान्त ने प्राथमिक और द्वितीयक संयोजकता का विचार दिया।
VBT ने संकरण (sp³, dsp², d²sp³) और चुंबकत्व समझाया।
CFT ने रंग, स्थिरता व इलेक्ट्रॉन वितरण की व्याख्या दी।
🟢 लिगैण्ड क्षेत्र शक्ति के अनुसार Δ₀ बदलता है और उसी से रंग भिन्न होते हैं।
समावयवता के प्रकार – आयनीकरण, समन्वय, लिगैण्ड, ज्यामितीय और प्रकाशीय।
🟡 ये यौगिक औद्योगिक, जैविक और औषधीय दृष्टि से अत्यन्त उपयोगी हैं।
Ni(CO)₄, Cisplatin, [Fe(CN)₆]³⁻ जैसे यौगिक इसके प्रमुख उदाहरण हैं।
🔹 III. त्वरित पुनरावलोकन
🔵 उपसहसंयोजन यौगिक = धातु + लिगैण्ड।
🟢 समन्वय संख्या = धातु से जुड़े लिगैण्ड परमाणु।
🟡 वर्नर, VBT, CFT तीन प्रमुख सिद्धान्त।
🔴 d–d संक्रमण से रंग; Δ₀ ऊर्जा विभाजन का माप।
🟣 cis/trans व प्रकाशीय समावयवता विशेष गुण।
🌟 उद्योग, औषधि, विश्लेषण में इनका अपार महत्त्व।
————————————————————————————————————————————————————————————————————————————
पाठ्यपुस्तक के प्रश्न
🔴 प्रश्न 5.1:
वर्ग की अभिधारणाओं के आधार पर उपसहसंयोजन यौगिकों में आबंधन को समझाइए।
🔵 उत्तर:
उपसहसंयोजन यौगिकों में आबंधन का वर्णन मुख्यतः दो सिद्धांतों से किया जाता है—
1️⃣ वर्नर का सिद्धांत — इसमें प्रधान धातु के दो प्रकार के संयोजकत्व माने गए हैं:
प्राथमिक संयोजकत्व (आयनी, विद्युत-स्थैतिक)
द्वितीयक संयोजकत्व (अणुसंयोजी, कोऑर्डिनेशन)
2️⃣ विकेन्द्र-कक्षीय (VBT) सिद्धांत — इसमें धातु-आयन द्वारा लिगैण्डों से युग्मन के लिए उपयुक्त कक्षाओं का मिश्रण बताकर बन्धों की व्याख्या की जाती है।
➡ इन सिद्धांतों से यौगिकों की रचना, आकृति और चुम्बकीय गुण स्पष्ट होते हैं।
🔴 प्रश्न 5.2:
FeSO₄, (NH₄)₂SO₄ विलयन का 1 : 1 मोलर अनुपात में मिश्रण Fe²⁺ आयन का परीक्षण देता है, जबकि CuSO₄ व जलीय अमोनिया का 1 : 4 मोलर अनुपात में मिश्रण Cu²⁺ आयन का परीक्षण नहीं देता। कारण समझाइए।
🔵 उत्तर:
Fe²⁺ आयन के साथ (NH₄)₂SO₄ में कोई स्थायी उपसहसंयोजन नहीं बनता, अतः Fe²⁺ स्वतंत्र रहता है और परीक्षण सम्भव होता है।
किन्तु CuSO₄ + 4 NH₃ से [Cu(NH₃)₄]SO₄ स्थिर उपसहसंयोजन बन जाता है, जिससे Cu²⁺ मुक्त नहीं रहता, अतः परीक्षण नहीं हो पाता।
🔴 प्रश्न 5.3:
उदाहरण सहित समन्वय संख्या, लिगैण्ड, उपसहसंयोजन संख्या, उपसहसंयोजन बहुलक, होमोलेप्टिक तथा हेटरोलेप्टिक समझाइए।
🔵 उत्तर:
समन्वय संख्या: प्रधान धातु-आयन से जुड़े कुल लिगैण्ड-आबन्धों की संख्या।
लिगैण्ड: अणु/आयन जो इलेक्ट्रॉन-युग्म देकर बन्ध बनाते हैं (जैसे NH₃, H₂O, Cl⁻)।
उपसहसंयोजन संख्या: धातु-आयन से जुड़े लिगैण्डों की कुल संख्या (प्रायः समन्वय संख्या ही)।
उपसहसंयोजन बहुलक: एकाधिक धातु-आयनों से बना यौगिक (उदा. [Cr₂(H₂O)₆(OH)₄]²⁺)।
होमोलेप्टिक: सभी लिगैण्ड समान (जैसे [Co(NH₃)₆]³⁺)।
हेटरोलेप्टिक: लिगैण्ड भिन्न-भिन्न (जैसे [Co(NH₃)₄Cl₂]⁺)।
🔴 प्रश्न 5.4:
एकदंत, द्विदंत तथा बहुदंत लिगैण्ड से क्या तात्पर्य है? प्रत्येक के दो उदाहरण दीजिए।
🔵 उत्तर:
एकदंत लिगैण्ड — जो केवल एक परमाणु से संयोजित होता है (NH₃, Cl⁻)।
द्विदंत लिगैण्ड — दो दानों से संयोजन करता है (en = एथिलीन-डायमीन, C₂O₄²⁻)।
बहुदंत लिगैण्ड — अनेक दानों से जुड़ता है (EDTA⁴⁻ षड्दंत)।
🔴 प्रश्न 5.5:
दिए उपसहसंयोजन यौगिकों में धातुओं के ऑक्सीकरण-अवस्था ज्ञात कीजिए —
(i) [Co(H₂O)(CN)(en)₂]²⁺ (ii) [PtCl₄]²⁻ (iii) [Cr(NH₃)₃Cl₃] (iv) [CoBr₂(en)₂]⁺ (v) K₃[Fe(CN)₆]
🔵 उत्तर:
(i) Co = +3 (ii) Pt = +2 (iii) Cr = +3 (iv) Co = +3 (v) Fe = +3 ✅
🔴 प्रश्न 5.6:
IUPAC नियमों के आधार पर निम्नलिखित नामों के सूत्र लिखिए —
🔵 उत्तर:
(i) टेट्राअक्वाडाइहाइड्रॉक्सोकोबाल्ट(III) → [Co(H₂O)₄(OH)₂]⁺
(ii) पोटैशियम टेट्रासायानोफेर्रेट(II) → K₄[Fe(CN)₄]
(iii) हेक्साअमीनक्रोमियम(III) सॉल्फेट → [Cr(NH₃)₆]₂(SO₄)₃
(iv) पोटैशियम हेक्सासायानोफेर्रेट(III) → K₃[Fe(CN)₆] ✅
(v) कॉपर(II) टेट्राअमीन सॉल्फेट → [Cu(NH₃)₄]SO₄
(vi) हेक्साअमीनप्लैटिनम(IV) क्लोराइड → [Pt(NH₃)₆]Cl₄
(vii) पेंटाअक्वानाइट्रिटो-O-कोबाल्ट(III) → [Co(H₂O)₅(NO₂)]²⁺
(viii) पेंटाअमीननाइट्रिटो-N-कोबाल्ट(III) → [Co(NH₃)₅(NO₂)]²⁺
🔴 प्रश्न 5.7:
IUPAC नियमों के आधार पर निम्नलिखित के मुख्य व्यवस्थित नाम लिखिए —
(i) [Co(NH₃)₆]Cl₃ (ii) [Co(NH₃)₄Cl₂]Cl (iii) [Ti(H₂O)₆]³⁺ (iv) [Co(NH₃)₃Cl(NO₂)]Cl
(v) [Pt(NH₃)₂Cl(NH₂CH₃)]Cl (vi) [Mn(H₂O)₆]²⁺
(vii) [Ni(NH₃)₆]Cl₂ (viii) [Co(en)₃]³⁺ (ix) [Ni(CO)₄]
🔵 उत्तर:
(i) हेक्साअमीनकोबाल्ट(III) क्लोराइड
(ii) टेट्राअमीनडाइक्लोरोकोबाल्ट(III) क्लोराइड
(iii) हेक्साअक्वाटाइटेनियम(III) आयन
(iv) ट्रायअमीनक्लोरोनाइट्रिटो-N-कोबाल्ट(III) क्लोराइड
(v) डायअमीनक्लोरो(मीथाइलअमीन)प्लैटिनम(II) क्लोराइड
(vi) हेक्साअक्वामैंगनीज़(II) आयन
(vii) हेक्साअमीननिकेल(II) क्लोराइड
(viii) ट्रिस(एथिलीन-डायमीन)कोबाल्ट(III) आयन
(ix) टेट्राकार्बोनिलनिकेल(0)
🔵 प्रश्न 5.11
निम्नलिखित के सभी समावयवों (ज्यामितीय व प्रकाशीय) की संरचनाएँ बनाइए—
(i) [CoCl₂(en)₂]⁺
(ii) [Co(NH₃)₂Cl₂(en)]⁺
(iii) [Co(NH₃)₂Cl₂(en)]⁺
🟢 उत्तर:
✔ (i) [CoCl₂(en)₂]⁺ में ज्यामितीय (cis/trans) दोनों समावयव बनते हैं।
cis रूप → प्रकाशीय समावयव (d और l) बनाता है।
trans रूप → कोई प्रकाशीय समावयव नहीं।
✔ (ii) [Co(NH₃)₂Cl₂(en)]⁺ → cis एवं trans दोनों ज्यामितीय समावयव बनते हैं।
cis रूप → प्रकाशीय समावयव बनाता है।
trans रूप → प्रकाशीय समावयव नहीं।
✔ (iii) [Co(NH₃)₂Cl₂(en)]⁺ का व्यवहार उपर्युक्त के समान है।
🔵 प्रश्न 5.12
[Pt(NH₃)₃BrCl(py)]⁺ के सभी ज्यामितीय समावयव लिखिए। इसमें कितने प्रकाशीय समावयव बनेंगे?
🟢 उत्तर:
✔ [Pt(NH₃)₃BrCl(py)]⁺ में प्लैटिनम(II) वर्गाकार यौगिक है।
✔ यह cis तथा trans — दो ज्यामितीय समावयव बनाता है।
✔ इनमें से कोई भी प्रकाशीय सक्रिय नहीं है क्योंकि सममिति उपस्थित है।
🔵 प्रश्न 5.13
जलीय विलयन में निम्नलिखित अभिक्रिया दर्शाएँ—
(i) जलीय पोटैशियम हेक्सासायनोफेर्रेट(II) के साथ लोहा का लवण।
(ii) जलीय पोटैशियम हेक्सासायनोफेर्रेट(III) के साथ लोहा का लवण।
🟢 उत्तर:
✔ (i) Fe²⁺ + [Fe(CN)₆]⁴⁻ → Turnbull’s blue (नीला अवक्षेप)
✔ (ii) Fe³⁺ + [Fe(CN)₆]⁴⁻ → Prussian blue (गहरा नीला अवक्षेप)
🔵 प्रश्न 5.14
जलीय विलयन में पोटैशियम हेक्सासायनोफेर्रेट(II) तथा जलीय KCN की अभिक्रिया में बनने वाले उपसहसंयोजन यौगिक की व्याख्या कीजिए।
यह H₂S गैस से अवक्षेप क्यों नहीं देता?
🟢 उत्तर:
✔ K₄[Fe(CN)₆] + KCN → [K₃Fe(CN)₆]⁻ (जटिल यौगिक)
✔ Fe²⁺ पूर्णतः CN⁻ से समन्वित होने के कारण मुक्त Fe²⁺ आयन अनुपस्थित है,
इसलिए H₂S गैस द्वारा FeS का अवक्षेप नहीं बनता।
🔵 प्रश्न 5.15
संयोजन यौगिक निर्धारण के आधार पर निम्नलिखित में उपसहसंयोजन संख्या व प्रकृति लिखिए—
(i) [Fe(CN)₆]⁴⁻
(ii) [FeF₆]³⁻
(iii) [Co(C₂O₄)₃]³⁻
(iv) [CoF₆]³⁻
🟢 उत्तर:
✔ (i) [Fe(CN)₆]⁴⁻ → Fe²⁺, उपसहसंयोजन संख्या 6, निम्न स्पिन
✔ (ii) [FeF₆]³⁻ → Fe³⁺, उपसहसंयोजन संख्या 6, उच्च स्पिन
✔ (iii) [Co(C₂O₄)₃]³⁻ → Co³⁺, उपसहसंयोजन संख्या 6, निम्न स्पिन
✔ (iv) [CoF₆]³⁻ → Co³⁺, उपसहसंयोजन संख्या 6, उच्च स्पिन
🔵 प्रश्न 5.16
क्रिस्टल क्षेत्र सिद्धांत के अनुसार d-आकर्षण में अंतर के कारण [Co(NH₃)₆]³⁺ तथा [FeF₆]³⁻ की चुंबकीय प्रकृति में अंतर क्यों है?
🟢 उत्तर:
✔ [Co(NH₃)₆]³⁺ → NH₃ मजबूत क्षेत्र लिगैण्ड है → युग्मन → सभी इलेक्ट्रॉन युग्मित → विचुंबकीय
✔ [FeF₆]³⁻ → F⁻ कमजोर क्षेत्र लिगैण्ड है → युग्मन नहीं → कुछ इलेक्ट्रॉन अपूर्ण युग्म → पराचुंबकीय
🔵 प्रश्न 5.17
उपसहसंयोजन यौगिकों में Δ₀ (विभाजन ऊर्जा) का मान किन कारणों पर निर्भर करता है?
🟢 उत्तर:
Δ₀ का मान निर्भर करता है—
✔ (i) केंद्रीय धातु आयन की आवेश व आकार पर
✔ (ii) लिगैण्ड की प्रकृति (मजबूत/कमज़ोर क्षेत्र) पर
✔ (iii) ज्यामिति (ऑक्टाहेड्रल, टेट्राहेड्रल) पर
✔ (iv) सहसंयोजन संख्या पर
🔵 प्रश्न 5.18
Δ₀ के आधार पर किसी यौगिक की उच्च या निम्न स्पिन प्रकृति कैसे निर्धारित की जाती है?
🟢 उत्तर:
✔ यदि Δ₀ > युग्मन ऊर्जा → निम्न स्पिन यौगिक बनता है।
✔ यदि Δ₀ < युग्मन ऊर्जा → उच्च स्पिन यौगिक बनता है।
🔵 प्रश्न 5.19
[Cr(NH₃)₆]³⁺ एवं [Ni(CN)₄]²⁻ की चुंबकीयता समझाइए।
🟢 उत्तर:
✔ [Cr(NH₃)₆]³⁺ → Cr³⁺ (3d³) → 3 अपूर्ण युग्म इलेक्ट्रॉन → पराचुंबकीय
✔ [Ni(CN)₄]²⁻ → Ni²⁺ (3d⁸) → CN⁻ मजबूत लिगैण्ड → सभी इलेक्ट्रॉन युग्मित → विचुंबकीय
🔵 प्रश्न 5.20
[Ni(H₂O)₆]²⁺ एवं [Ni(CN)₄]²⁻ के रंगों में अंतर समझाइए।
🟢 उत्तर:
✔ [Ni(H₂O)₆]²⁺ → Δ₀ कम → नीला रंग
✔ [Ni(CN)₄]²⁻ → Δ₀ अधिक → पीला/रंगहीन
🔵 प्रश्न 5.21
[Fe(CN)₆]⁴⁻ एवं [Fe(H₂O)₆]²⁺ के रंगों में अंतर क्यों है?
🟢 उत्तर:
✔ CN⁻ → मजबूत क्षेत्र लिगैण्ड → Δ₀ बड़ा → इलेक्ट्रॉनिक संक्रमण उच्च ऊर्जा → रंग में अंतर।
✔ H₂O → कमजोर क्षेत्र लिगैण्ड → Δ₀ छोटा → संक्रमण कम ऊर्जा → भिन्न रंग।
🔵 प्रश्न 5.22
कुछ उपसहसंयोजन यौगिक रंगहीन क्यों होते हैं?
🟢 उत्तर:
✔ यदि d-d संक्रमण संभव न हो (d⁰ या d¹⁰ संरचना) → कोई रंग नहीं।
उदाहरण: [Zn(H₂O)₆]²⁺, [Cu(NH₃)₄]²⁺
🔵 प्रश्न 5.23
निम्नलिखित में से कौन-सा यौगिक d-कक्षकों का उपयोग कर उपसहसंयोजन बनाता है?
(i) K₃[Co(C₂O₄)₃]
(ii) (NH₄)₂[CoF₄]
(iii) cis-[CrCl₂(en)₂]Cl
(iv) [Mn(H₂O)₆]SO₄
🟢 उत्तर:
✔ (i), (iii), (iv) सभी d-कक्षकों का उपयोग करते हैं।
🔵 प्रश्न 5.24
IUPAC नामकरण कीजिए और प्रत्येक का ऑक्सीकरण अवस्था, समन्वय संख्या, केंद्रीय आयन लिखिए—
(i) K[Cr(H₂O)₂(C₂O₄)₂]·3H₂O
(ii) [Co(NH₃)₅Cl]Cl₂
(iii) [CrCl₃(gly)₃]
(iv) Cs₂[FeCl₄]
🟢 उत्तर:
✔ (i) पोटैशियम डाइएक्वाडाइऑक्सालेटोक्रोमेट(III); Cr³⁺; सं.सं. = 6
✔ (ii) पेंटामाइनक्लोरोकोबाल्ट(III) क्लोराइड; Co³⁺; सं.सं. = 6
✔ (iii) ट्राइक्लोरो-ट्राइग्लाइसिनेटो-क्रोमियम(III); Cr³⁺; सं.सं. = 6
✔ (iv) सीज़ियम टेट्राक्लोरो-फेर्रेट(II); Fe²⁺; सं.सं. = 4
🔵 प्रश्न 5.25
Δ₀ के मान के आधार पर [Ti(H₂O)₆]³⁺ का रंग समझाइए।
🟢 उत्तर:
✔ [Ti(H₂O)₆]³⁺ → 3d¹ → d-d संक्रमण → बैंगनी रंग उत्पन्न करता है।
🔵 प्रश्न 5.26
चेलैट प्रभाव से क्या अभिप्राय है? एक उदाहरण दीजिए।
🟢 उत्तर:
✔ जब एक लिगैण्ड कई दाँतों द्वारा धातु से जुड़ता है → चेलैट बनता है।
✔ यह यौगिक सामान्य से अधिक स्थायी होता है।
उदाहरण: [Cu(en)₂]²⁺
🔵 प्रश्न 5.27
उपसहसंयोजन यौगिकों का उपयोग लिखिए।
🟢 उत्तर:
✔ (i) औषधियों में (जैसे सिस्प्लैटिन कैंसर उपचार)
✔ (ii) धातुओं के निकर्षण में
✔ (iii) विश्लेषणात्मक परीक्षणों में (EDTA टाइट्रेशन)
✔ (iv) उत्प्रेरक क्रिया में
🔵 प्रश्न 5.28
संयोजन [Co(NH₃)₆]Cl₂ के विलयन में आयनों की संख्या ज्ञात कीजिए।
🟢 उत्तर:
✔ [Co(NH₃)₆]Cl₂ → 1 यौगिक आयन + 2 Cl⁻ → कुल 3 आयन
🔴 प्रश्न 5.29:
निम्नलिखित आयनों में से किसके चुंबकीय आघूर्ण का मान सर्वाधिक होगा?
(i) [Cr(H₂O)₆]³⁺
(ii) [Fe(H₂O)₆]²⁺
(iii) [Zn(H₂O)₆]²⁺
🔵 उत्तर:
➡ [Cr(H₂O)₆]³⁺ में d³ संरचना होती है, अतः 3 अपरिवेशित इलेक्ट्रॉन होते हैं।
➡ [Fe(H₂O)₆]²⁺ में d⁶ संरचना (4 अपरिवेशित इलेक्ट्रॉन) होती है।
➡ [Zn(H₂O)₆]²⁺ में d¹⁰ संरचना होती है, कोई अपरिवेशित इलेक्ट्रॉन नहीं।
✔ Final: [Fe(H₂O)₆]²⁺ का चुंबकीय आघूर्ण सर्वाधिक होगा।
🔴 प्रश्न 5.30:
K[Co(CO)₄] में कोबाल्ट की ऑक्सीकरण अवस्था है—
(i) +3
(ii) +1
(iii) –1
(iv) –3
🔵 उत्तर:
➡ कुल आवेश = –1 (आयन K⁺ के कारण समग्र शुद्ध आवेश = 0)
➡ मान लें कोबाल्ट की ऑक्सीकरण अवस्था = x
तो, x + 4(0) – 1 = 0
➡ x = +1
✔ Final: कोबाल्ट की ऑक्सीकरण अवस्था = +1
🔴 प्रश्न 5.31:
निम्न में सर्वाधिक स्थायी यौगिक है—
(i) [Fe(H₂O)₆]³⁺
(ii) [Fe(NH₃)₆]³⁺
(iii) [Fe(C₂O₄)₃]³⁻
(iv) [FeCl₆]³⁻
🔵 उत्तर:
➡ स्थिरता लिगैण्ड की शक्ति पर निर्भर करती है।
➡ C₂O₄²⁻ एक द्विदंत लिगैण्ड है जो चिलेशन बनाता है, जिससे स्थिरता बढ़ती है।
✔ Final: सर्वाधिक स्थायी यौगिक = [Fe(C₂O₄)₃]³⁻
🔴 प्रश्न 5.32:
निम्नलिखित के लिए दृश्य प्रकाश में अवशोषण की तरंगदैर्घ्य का सही क्रम क्या होगा?
(i) [Ni(NO₂)₆]⁴⁻
(ii) [Ni(NH₃)₆]²⁺
(iii) [Ni(H₂O)₆]²⁺
🔵 उत्तर:
➡ स्पेक्ट्रोकेमिकल श्रेणी: NO₂⁻ > NH₃ > H₂O
➡ जितना अधिक लिगैण्ड फील्ड, उतनी कम तरंगदैर्घ्य।
✔ Final: तरंगदैर्घ्य क्रम =
[Ni(H₂O)₆]²⁺ > [Ni(NH₃)₆]²⁺ > [Ni(NO₂)₆]⁴⁻
————————————————————————————————————————————————————————————————————————————
अन्य महत्वपूर्ण प्रश्न
(CBSE MODEL प्रश्न पत्र)
सिर्फ इसी पाठ से निर्मित CBSE MODEL प्रश्न पत्र।
✳ खण्ड – A (बहुविकल्पीय प्रश्न: 1 × 16 = 16 अंक)
प्रश्न 1. उपसहसंयोजन यौगिक किसके बीच बनते हैं?
धातु और अधातु
धातु आयन और अणु या आयन
अधातु और गैसें
केवल अधातु
उत्तर: 2
प्रश्न 2. किसी उपसहसंयोजन यौगिक में “केंद्रीय परमाणु” कहलाता है —
लिगैण्ड
सहसंयोजक परमाणु
वह परमाणु जो लिगैण्ड से संयोजित होता है
द्वितीयक संयोजकता वाला परमाणु
उत्तर: 3
प्रश्न 3. लिगैण्ड वह होता है जो —
इलेक्ट्रॉन ग्रहण करता है
इलेक्ट्रॉन दान करता है
इलेक्ट्रॉन साझा करता है
न्यूट्रॉन दान करता है
उत्तर: 2
प्रश्न 4. [Cu(NH₃)₄]SO₄ में लिगैण्ड है —
SO₄²⁻
Cu²⁺
NH₃
N₂
उत्तर: 3
प्रश्न 5. [Fe(CN)₆]⁴⁻ में धातु आयन की ऑक्सीकरण अवस्था है —
+2
+3
+4
+6
उत्तर: 1
प्रश्न 6. [Co(NH₃)₆]³⁺ का नाम है —
हेक्साअमीन कोबाल्ट(III) आयन
हेक्साअमीन कोबाल्ट(II) आयन
हेक्साअमीन नाइट्राइड
अमीनकोबाल्ट यौगिक
उत्तर: 1
प्रश्न 7. लिगैण्डों की दन्तता (denticity) का अर्थ है —
लिगैण्ड में परमाणुओं की संख्या
लिगैण्ड द्वारा दान किए जाने वाले इलेक्ट्रॉन युग्मों की संख्या
लिगैण्ड का भार
लिगैण्ड की विद्युतऋणात्मकता
उत्तर: 2
प्रश्न 8. एथिलीनडायमीन (en) एक —
एकदन्त लिगैण्ड
द्विदन्त लिगैण्ड
त्रिदन्त लिगैण्ड
चतुष्दन्त लिगैण्ड
उत्तर: 2
प्रश्न 9. EDTA⁴⁻ लिगैण्ड होता है —
द्विदन्त
त्रिदन्त
षड्दन्त
अष्टदन्त
उत्तर: 3
प्रश्न 10. कॉर्डिनेशन संख्या (संयोजन संख्या) निर्भर करती है —
लिगैण्ड की दन्तता पर
आयन के द्रव्यमान पर
तापमान पर
घनत्व पर
उत्तर: 1
प्रश्न 11. [Cr(H₂O)₆]³⁺ आयन का आकार है —
वर्गाकार
चतुष्फलकीय
अष्टफलकीय
त्रिकोणीय समतलीय
उत्तर: 3
प्रश्न 12. VBT के अनुसार [Ni(CN)₄]²⁻ का संकरण है —
dsp²
sp³
sp³d²
d²sp³
उत्तर: 1
प्रश्न 13. [Ni(CN)₄]²⁻ का चुंबकीय गुण है —
पैरामैग्नेटिक
डायमैग्नेटिक
फेरोमैग्नेटिक
एंटीफेरोमैग्नेटिक
उत्तर: 2
प्रश्न 14. रंगीन यौगिक बनने का कारण है —
ऊष्मा का प्रभाव
d–d इलेक्ट्रॉन संक्रमण
नाभिकीय संक्रमण
लिगैण्ड का विघटन
उत्तर: 2
Options (A/R प्रकार के प्रश्नों हेतु)
A और R दोनों सत्य हैं तथा R, A का सही व्याख्यान है।
A और R दोनों सत्य हैं परन्तु R, A का सही व्याख्यान नहीं है।
A सत्य है, R असत्य है।
A असत्य है, R सत्य है।
प्रश्न 15.
A: [Fe(CN)₆]⁴⁻ आयन डायमैग्नेटिक होता है।
R: CN⁻ एक शक्तिशाली क्षेत्र लिगैण्ड है जो d-कक्षकों को युग्मित कर देता है।
उत्तर: 1
प्रश्न 16.
A: [CoF₆]³⁻ और [Co(NH₃)₆]³⁺ का संकरण समान होता है।
R: F⁻ और NH₃ दोनों एक ही क्षेत्र-शक्ति के लिगैण्ड हैं।
उत्तर: 3
✳ खण्ड – B (अति लघु उत्तर प्रश्न: 2 × 5 = 10 अंक)
प्रश्न 17. लिगैण्ड की परिभाषा दीजिए।
🟩 वह आयन या अणु जो केंद्रीय धातु आयन को इलेक्ट्रॉन युग्म दान करता है, लिगैण्ड कहलाता है।
🧪 उदाहरण — NH₃, H₂O, Cl⁻, CN⁻।
प्रश्न 18. संयोजन संख्या (Coordination number) क्या है?
🟦 यह वह संख्या है जो बताती है कि केंद्रीय धातु आयन से कितने संयोजन स्थल जुड़े हैं।
🧮 उदाहरण — [Cr(H₂O)₆]³⁺ में संयोजन संख्या 6 है।
प्रश्न 19. एकदन्त एवं द्विदन्त लिगैण्ड में अंतर लिखिए।
🟩 एकदन्त — केवल एक परमाणु इलेक्ट्रॉन युग्म दान करता है।
🟦 द्विदन्त — दो परमाणु इलेक्ट्रॉन युग्म दान करते हैं (जैसे en)।
प्रश्न 20. यौगिक [Co(NH₃)₆]³⁺ में Co की ऑक्सीकरण अवस्था ज्ञात कीजिए।
➤ सूत्र: x + 6(0) = +3
✅ x = +3
प्रश्न 21. समावयवता (Isomerism) का एक प्रकार लिखिए जो उपसहसंयोजन यौगिकों में पाया जाता है।
🟦 ज्यामितीय समावयवता — लिगैण्ड की स्थिति भिन्न होती है।
🟩 उदाहरण — [Pt(NH₃)₂Cl₂] के सिस और ट्रांस रूप।
✳ खण्ड – C (संक्षिप्त उत्तर प्रश्न: 3 × 7 = 21 अंक)
प्रश्न 22. ज्यामितीय समावयवता समझाइए।
🧪 जब एक ही रासायनिक सूत्र वाले यौगिकों में लिगैण्डों की स्थिति भिन्न होती है, तो उसे ज्यामितीय समावयवता कहते हैं।
🟩 उदाहरण — [Pt(NH₃)₂Cl₂] के सिस (दोनों Cl साथ) और ट्रांस (Cl विपरीत) रूप।
🎯 यह केवल वर्गाकार एवं अष्टफलकीय यौगिकों में होती है।
प्रश्न 23. आयनिक समावयवता क्या है?
🟦 जब दो उपसहसंयोजन यौगिकों के आयन स्थान बदलते हैं, परन्तु सूत्र समान रहता है, तो इसे आयनिक समावयवता कहते हैं।
🧪 उदाहरण — [Co(NH₃)₅Br]SO₄ और [Co(NH₃)₅SO₄]Br।
प्रश्न 24. समन्वय क्षेत्र सिद्धान्त (Crystal Field Theory) का मूल विचार बताइए।
🟩 लिगैण्डों के नकारात्मक क्षेत्र के प्रभाव से केंद्रीय धातु आयन के d-कक्षक विभाजित हो जाते हैं।
🎯 यह विभाजन यौगिकों के रंग, चुंबकत्व और स्थिरता की व्याख्या करता है।
प्रश्न 25. [Ni(CO)₄] और [Ni(CN)₄]²⁻ के संकरणों की तुलना कीजिए।
🧪 [Ni(CO)₄]: sp³ (चतुष्फलकीय), डायमैग्नेटिक।
🟦 [Ni(CN)₄]²⁻: dsp² (वर्गाकार), डायमैग्नेटिक।
🎯 लिगैण्ड की क्षेत्र शक्ति पर संकरण निर्भर करता है।
प्रश्न 26. उपसहसंयोजन यौगिकों के रंगीन होने का कारण बताइए।
🟩 d–d इलेक्ट्रॉन संक्रमण से दृश्य प्रकाश का अवशोषण होता है।
🧪 शेष प्रकाश परावर्तित होकर रंग उत्पन्न करता है।
🎯 रंग की तीव्रता लिगैण्ड की प्रकृति पर निर्भर करती है।
प्रश्न 27. [CoF₆]³⁻ और [Co(NH₃)₆]³⁺ के संकरणों में अन्तर बताइए।
🧪 [CoF₆]³⁻ → बाह्य-परत संकरण (sp³d²), पैरामैग्नेटिक।
🟦 [Co(NH₃)₆]³⁺ → आंतरिक-परत संकरण (d²sp³), डायमैग्नेटिक।
🎯 F⁻ = कमजोर क्षेत्र लिगैण्ड, NH₃ = मजबूत क्षेत्र लिगैण्ड।
प्रश्न 28. यौगिक [Fe(CN)₆]⁴⁻ का संकरण तथा चुंबकीय गुण बताइए।
🧪 संकरण — d²sp³ (आंतरिक-परत, अष्टफलकीय)।
🎯 CN⁻ लिगैण्ड शक्तिशाली क्षेत्र लिगैण्ड है, सभी इलेक्ट्रॉन युग्मित हो जाते हैं।
✅ परिणाम — डायमैग्नेटिक यौगिक।
✳ खण्ड – D (प्रकरण-आधारित प्रश्न: 4 × 2 = 8 अंक)
प्रश्न 29.
नीचे दिया गया अनुच्छेद पढ़िए और प्रश्नों के उत्तर दीजिए —
यौगिक [Co(NH₃)₆]Cl₃ एक प्रसिद्ध उपसहसंयोजन यौगिक है। इसमें Co³⁺ आयन केंद्रीय परमाणु है जो 6 अमोनिया अणुओं से संयोजित है। यह यौगिक विद्युत अपघटन पर 3 Cl⁻ आयन देता है।
(क) यौगिक का प्रकार क्या है?
🟩 आयनिक उपसहसंयोजन यौगिक।
(ख) Co की ऑक्सीकरण अवस्था ज्ञात कीजिए।
➤ x + 6(0) = +3 ⟹ ✅ x = +3।
(ग) यौगिक का संकरण क्या है?
🧪 d²sp³ (आंतरिक-परत संकरण, अष्टफलकीय संरचना)।
(घ) यह यौगिक डायमैग्नेटिक क्यों है?
🎯 Co³⁺ (3d⁶) में सभी इलेक्ट्रॉन NH₃ के प्रभाव से युग्मित हो जाते हैं।
प्रश्न 30.
नीचे दिए गए दो यौगिकों पर विचार कीजिए —
(A) [CoF₆]³⁻ (B) [Co(NH₃)₆]³⁺
(क) कौन-सा लिगैण्ड शक्तिशाली क्षेत्र का है?
🟦 NH₃ (मजबूत क्षेत्र लिगैण्ड)।
(ख) [CoF₆]³⁻ में Co का संकरण क्या है?
🧪 sp³d² (बाह्य-परत संकरण)।
(ग) कौन-सा यौगिक पैरामैग्नेटिक है?
🎯 [CoF₆]³⁻, क्योंकि F⁻ कमजोर क्षेत्र लिगैण्ड है और इलेक्ट्रॉन युग्मित नहीं होते।
(घ) [Co(NH₃)₆]³⁺ का चुंबकीय गुण?
✅ डायमैग्नेटिक (सभी इलेक्ट्रॉन युग्मित)।
✳ खण्ड – E (दीर्घ उत्तर प्रश्न: 5 × 3 = 15 अंक)
प्रश्न 31.
संयोजन संख्या (Coordination number) एवं लिगैण्ड की दन्तता को उदाहरण सहित समझाइए।
🟦 संयोजन संख्या — वह संख्या जो बताती है कि केंद्रीय धातु आयन से कितने संयोजन स्थल जुड़े हैं।
🧪 उदाहरण — [Cr(H₂O)₆]³⁺ में संयोजन संख्या 6।
🟩 दन्तता — लिगैण्ड द्वारा दान किए गए इलेक्ट्रॉन युग्मों की संख्या।
🎯 उदाहरण —
NH₃ (एकदन्त), en (द्विदन्त), EDTA⁴⁻ (षड्दन्त)।
या (OR)
लिगैण्डों के प्रकारों की व्याख्या कीजिए।
🧪 (1) एकदन्त — एक परमाणु से संयोजन (जैसे Cl⁻)।
🟩 (2) द्विदन्त — दो परमाणुओं से संयोजन (जैसे en)।
🟦 (3) बहुदन्त — अनेक परमाणुओं से संयोजन (जैसे EDTA⁴⁻)।
प्रश्न 32.
समन्वय क्षेत्र सिद्धान्त (Crystal Field Theory) के प्रमुख सिद्धान्त समझाइए।
🟩 लिगैण्डों का नकारात्मक क्षेत्र केंद्रीय धातु आयन के d-कक्षकों को विभाजित करता है।
🧪 अष्टफलकीय क्षेत्र में d-कक्षक दो समूहों में विभाजित होते हैं — t₂g और e_g।
🎯 यह विभाजन ऊर्जा (Δ₀) यौगिक के रंग, चुंबकीय गुण और स्थिरता का निर्धारण करता है।
या (OR)
संकरण (Hybridisation) की अवधारणा से [Ni(CN)₄]²⁻ की संरचना स्पष्ट कीजिए।
🧪 Ni²⁺ में विन्यास: 3d⁸4s² → CN⁻ (मजबूत क्षेत्र) द्वारा इलेक्ट्रॉन युग्मन।
🎯 संकरण: dsp² → वर्गाकार संरचना।
✅ सभी इलेक्ट्रॉन युग्मित ⇒ डायमैग्नेटिक यौगिक।
प्रश्न 33.
उपसहसंयोजन यौगिकों में समावयवता के प्रकारों की व्याख्या कीजिए।
🟩 प्रमुख प्रकार —
1️⃣ आयनिक समावयवता — आयनों का स्थान परिवर्तन (उदा. [Co(NH₃)₅Br]SO₄ / [Co(NH₃)₅SO₄]Br)।
2️⃣ ज्यामितीय समावयवता — लिगैण्ड की स्थिति भिन्न (उदा. [Pt(NH₃)₂Cl₂])।
3️⃣ प्रकाशीय समावयवता — दर्पण प्रतिबिंब रूप (उदा. [Cr(en)₃]³⁺)।
🎯 समावयवता उपसहसंयोजन यौगिकों की सबसे विशिष्ट विशेषता है।
या (OR)
रंगीन उपसहसंयोजन यौगिकों के बनने का कारण बताइए।
🧪 अपूर्ण d-कक्षक वाले आयन दृश्य प्रकाश का अवशोषण करते हैं।
🟦 d–d संक्रमण से ऊर्जा परिवर्तन होता है।
🎯 शेष प्रकाश परावर्तित होकर रंग उत्पन्न करता है; रंग लिगैण्ड की प्रकृति पर निर्भर होता है।
————————————————————————————————————————————————————————————————————————————
Neet पिछले सालों के प्रश्न
🔵 प्रश्न 1: उपसहसंयोजन यौगिक में केन्द्रीय धातु परमाणु से जुड़ने वाले परमाणु या समूह को क्या कहते हैं?
🔴 ① आयन
🟢 ② लिगैण्ड
🟡 ③ संयोजक
🔵 ④ परिसंघ
🟢 उत्तर: ② लिगैण्ड
📘 परीक्षा: NEET
📅 वर्ष: 2018 | सेट: R-1
🔵 प्रश्न 2: [Fe(CN)₆]⁴⁻ में Fe की ऑक्सीकरण अवस्था क्या है?
🔴 ① +2
🟢 ② +3
🟡 ③ +4
🔵 ④ 0
🟢 उत्तर: ① +2
📘 परीक्षा: NEET
📅 वर्ष: 2019 | सेट: S
🔵 प्रश्न 3: [Co(NH₃)₆]³⁺ यौगिक का नाम क्या है?
🔴 ① हेक्साअमीन कोबाल्ट(III) आयन
🟢 ② हेक्साअमीन कोबाल्ट(II) आयन
🟡 ③ हेक्साअमीन कोबाल्ट(IV) आयन
🔵 ④ हेक्साअमीन आयन
🟢 उत्तर: ① हेक्साअमीन कोबाल्ट(III) आयन
📘 परीक्षा: AIPMT
📅 वर्ष: 2013 | सेट: Q
🔵 प्रश्न 4: [Cu(NH₃)₄]²⁺ आयन का आकार क्या है?
🔴 ① चतुर्भुजीय
🟢 ② वर्गाकार
🟡 ③ त्रिभुजाकार
🔵 ④ रेखीय
🟢 उत्तर: ① चतुर्भुजीय
📘 परीक्षा: NEET
📅 वर्ष: 2021 | सेट: R-2
🔵 प्रश्न 5: [Fe(CN)₆]³⁻ में Fe की चुम्बकीय आचरण क्या होगी?
🔴 ① परमचुम्बकीय
🟢 ② अपचुम्बकीय
🟡 ③ प्रबल चुम्बकीय
🔵 ④ स्थायी चुम्बकीय
🟢 उत्तर: ② अपचुम्बकीय
📘 परीक्षा: NEET
📅 वर्ष: 2018 | सेट: S
🔵 प्रश्न 6: [Ni(CO)₄] का आकार क्या होता है?
🔴 ① वर्गाकार
🟢 ② चतुर्भुजीय
🟡 ③ त्रिकोणीय
🔵 ④ अष्टफलक
🟢 उत्तर: ② चतुर्भुजीय
📘 परीक्षा: AIPMT
📅 वर्ष: 2011 | सेट: N
🔵 प्रश्न 7: [Ni(CN)₄]²⁻ का संकरण प्रकार क्या है?
🔴 ① sp³
🟢 ② dsp²
🟡 ③ sp²
🔵 ④ d²sp³
🟢 उत्तर: ② dsp²
📘 परीक्षा: NEET
📅 वर्ष: 2020 | सेट: Q
🔵 प्रश्न 8: निम्न में से कौन-सा यौगिक अपचुम्बकीय है?
🔴 ① [Fe(H₂O)₆]³⁺
🟢 ② [Fe(CN)₆]⁴⁻
🟡 ③ [CoF₆]³⁻
🔵 ④ [NiCl₄]²⁻
🟢 उत्तर: ② [Fe(CN)₆]⁴⁻
📘 परीक्षा: NEET
📅 वर्ष: 2017 | सेट: S
🔵 प्रश्न 9: [Cr(H₂O)₆]³⁺ का रंग क्या है?
🔴 ① हरा
🟢 ② नीला
🟡 ③ गुलाबी
🔵 ④ रंगहीन
🟢 उत्तर: ① हरा
📘 परीक्षा: AIPMT
📅 वर्ष: 2012 | सेट: P
🔵 प्रश्न 10: कौन-सा यौगिक ज्यामितीय समावयवता नहीं दिखाता?
🔴 ① [Pt(NH₃)₂Cl₂]
🟢 ② [Co(NH₃)₆]³⁺
🟡 ③ [Cr(H₂O)₄Cl₂]⁺
🔵 ④ [Ni(NH₃)₂Cl₂]
🟢 उत्तर: ② [Co(NH₃)₆]³⁺
📘 परीक्षा: NEET
📅 वर्ष: 2019 | सेट: Q
🔵 प्रश्न 11: वर्नर के सिद्धांत के अनुसार, उपसहसंयोजन संख्या किसे कहते हैं?
🔴 ① आयनिक संयोजकता
🟢 ② धातु से जुड़े लिगैण्ड की संख्या
🟡 ③ ऑक्सीकरण संख्या
🔵 ④ चुम्बकीय संख्या
🟢 उत्तर: ② धातु से जुड़े लिगैण्ड की संख्या
📘 परीक्षा: NEET
📅 वर्ष: 2018 | सेट: S
🔵 प्रश्न 12: [CoCl₂(en)₂]⁺ में समन्वय संख्या क्या है?
🔴 ① 2
🟢 ② 4
🟡 ③ 6
🔵 ④ 3
🟢 उत्तर: ③ 6
📘 परीक्षा: AIPMT
📅 वर्ष: 2011 | सेट: Q
🔵 प्रश्न 13: [Fe(H₂O)₆]²⁺ यौगिक का रंग क्या है?
🔴 ① रंगहीन
🟢 ② हल्का हरा
🟡 ③ नीला
🔵 ④ पीला
🟢 उत्तर: ② हल्का हरा
📘 परीक्षा: NEET
📅 वर्ष: 2020 | सेट: R
🔵 प्रश्न 14: [Cu(NH₃)₄]SO₄ का रंग क्या है?
🔴 ① हरा
🟢 ② नीला
🟡 ③ गुलाबी
🔵 ④ पीला
🟢 उत्तर: ② नीला
📘 परीक्षा: NEET
📅 वर्ष: 2019 | सेट: Q
🔵 प्रश्न 15: [Fe(CO)₅] का आकार क्या है?
🔴 ① चतुर्भुजीय
🟢 ② त्रिकोणीय द्विपिरमिडीय
🟡 ③ वर्गाकार
🔵 ④ अष्टफलक
🟢 उत्तर: ② त्रिकोणीय द्विपिरमिडीय
📘 परीक्षा: NEET
📅 वर्ष: 2021 | सेट: P
🔵 प्रश्न 16: कौन-सा लिगैण्ड द्विदन्त (bidentate) है?
🔴 ① NH₃
🟢 ② C₂O₄²⁻
🟡 ③ H₂O
🔵 ④ Cl⁻
🟢 उत्तर: ② C₂O₄²⁻
📘 परीक्षा: AIPMT
📅 वर्ष: 2010 | सेट: L
🔵 प्रश्न 17: [Co(en)₃]³⁺ में कितने चिरल (optically active) समावयव बन सकते हैं?
🔴 ① 1
🟢 ② 2
🟡 ③ 3
🔵 ④ कोई नहीं
🟢 उत्तर: ② 2
📘 परीक्षा: NEET
📅 वर्ष: 2020 | सेट: Q
🔵 प्रश्न 18: [Ni(CO)₄] में Ni की ऑक्सीकरण अवस्था क्या है?
🔴 ① +2
🟢 ② 0
🟡 ③ +1
🔵 ④ -1
🟢 उत्तर: ② 0
📘 परीक्षा: NEET
📅 वर्ष: 2018 | सेट: R
🔵 प्रश्न 19: [Fe(CN)₆]³⁻ आयन का चुम्बकीय आचरण कैसा है?
🔴 ① परमचुम्बकीय
🟢 ② अपचुम्बकीय
🟡 ③ अतिचुम्बकीय
🔵 ④ कोई नहीं
🟢 उत्तर: ② अपचुम्बकीय
📘 परीक्षा: NEET
📅 वर्ष: 2017 | सेट: Q
🔵 प्रश्न 20: [CoF₆]³⁻ का संकरण क्या है?
🔴 ① sp³
🟢 ② sp³d²
🟡 ③ d²sp³
🔵 ④ dsp²
🟢 उत्तर: ② sp³d²
📘 परीक्षा: AIPMT
📅 वर्ष: 2013 | सेट: M
🔵 प्रश्न 21: [Fe(H₂O)₆]²⁺ और [Fe(CN)₆]⁴⁻ में कौन-सा अपचुम्बकीय है?
🔴 ① [Fe(H₂O)₆]²⁺
🟢 ② [Fe(CN)₆]⁴⁻
🟡 ③ दोनों
🔵 ④ कोई नहीं
🟢 उत्तर: ② [Fe(CN)₆]⁴⁻
📘 परीक्षा: NEET
📅 वर्ष: 2021 | सेट: R-1
🔵 प्रश्न 22: [NiCl₄]²⁻ का चुम्बकीय स्वभाव क्या है?
🔴 ① अपचुम्बकीय
🟢 ② परमचुम्बकीय
🟡 ③ अचुम्बकीय
🔵 ④ कोई नहीं
🟢 उत्तर: ② परमचुम्बकीय
📘 परीक्षा: NEET
📅 वर्ष: 2016 | सेट: P
🔵 प्रश्न 23: समन्वय संख्या 4 वाले यौगिकों का सामान्य आकार क्या होता है?
🔴 ① अष्टफलक
🟢 ② चतुर्भुजीय या वर्गाकार
🟡 ③ त्रिकोणीय
🔵 ④ रेखीय
🟢 उत्तर: ② चतुर्भुजीय या वर्गाकार
📘 परीक्षा: AIPMT
📅 वर्ष: 2012 | सेट: P
🔵 प्रश्न 24: [Cr(NH₃)₄Cl₂]⁺ में कितने ज्यामितीय समावयव बनते हैं?
🔴 ① 1
🟢 ② 2
🟡 ③ 3
🔵 ④ 4
🟢 उत्तर: ② 2
📘 परीक्षा: NEET
📅 वर्ष: 2018 | सेट: Q
🔵 प्रश्न 25: [Pt(NH₃)₂Cl₂] में कौन-सा समावयव रंगीन होता है?
🔴 ① ट्रांस
🟢 ② सिस
🟡 ③ दोनों
🔵 ④ कोई नहीं
🟢 उत्तर: ② सिस
📘 परीक्षा: NEET
📅 वर्ष: 2019 | सेट: P
🔵 प्रश्न 26: [Fe(H₂O)₆]³⁺ का रंग किस कारण से होता है?
🔴 ① d–d संक्रमण
🟢 ② आयनन ऊर्जा
🟡 ③ हाइड्रोजन बन्धन
🔵 ④ आयन विनिमय
🟢 उत्तर: ① d–d संक्रमण
📘 परीक्षा: NEET
📅 वर्ष: 2022 | सेट: P
🔵 प्रश्न 27: [Cu(NH₃)₄]²⁺ में धातु की ऑक्सीकरण अवस्था क्या है?
🔴 ① +1
🟢 ② +2
🟡 ③ +3
🔵 ④ 0
🟢 उत्तर: ② +2
📘 परीक्षा: NEET
📅 वर्ष: 2020 | सेट: S
🔵 प्रश्न 28: कौन-सा यौगिक प्रकाशीय समावयवता प्रदर्शित करता है?
🔴 ① [Co(en)₃]³⁺
🟢 ② [Ni(CN)₄]²⁻
🟡 ③ [Fe(CN)₆]⁴⁻
🔵 ④ [Cu(NH₃)₄]²⁺
🟢 उत्तर: ① [Co(en)₃]³⁺
📘 परीक्षा: AIPMT
📅 वर्ष: 2014 | सेट: N
🔵 प्रश्न 29: [NiCl₄]²⁻ और [Ni(CN)₄]²⁻ में क्या अंतर है?
🔴 ① दोनों का संकरण समान
🟢 ② [NiCl₄]²⁻ परमचुम्बकीय और [Ni(CN)₄]²⁻ अपचुम्बकीय
🟡 ③ दोनों अपचुम्बकीय
🔵 ④ दोनों वर्गाकार
🟢 उत्तर: ② [NiCl₄]²⁻ परमचुम्बकीय और [Ni(CN)₄]²⁻ अपचुम्बकीय
📘 परीक्षा: NEET
📅 वर्ष: 2017 | सेट: Q
🔵 प्रश्न 30: [Cr(NH₃)₆]³⁺ का संकरण क्या है?
🔴 ① sp³
🟢 ② d²sp³
🟡 ③ dsp²
🔵 ④ sp³d²
🟢 उत्तर: ② d²sp³
📘 परीक्षा: AIPMT
📅 वर्ष: 2010 | सेट: Q
🔵 प्रश्न 31: कौन-सा यौगिक आयनिक और सहसंयोजक दोनों प्रकार के बन्ध प्रदर्शित करता है?
🔴 ① [Fe(CN)₆]⁴⁻
🟢 ② [Cu(NH₃)₄]SO₄
🟡 ③ K₄[Fe(CN)₆]
🔵 ④ [Ni(CO)₄]
🟢 उत्तर: ③ K₄[Fe(CN)₆]
📘 परीक्षा: NEET
📅 वर्ष: 2015 | सेट: P
🔵 प्रश्न 32: [Co(NO₂)₆]³⁻ और [Co(NH₃)₆]³⁺ का रंग भिन्न क्यों होता है?
🔴 ① लिगैण्ड की प्रकृति भिन्न होने के कारण
🟢 ② धातु की ऑक्सीकरण अवस्था अलग होने के कारण
🟡 ③ तापमान भिन्न होने के कारण
🔵 ④ द्रव्यमान के कारण
🟢 उत्तर: ① लिगैण्ड की प्रकृति भिन्न होने के कारण
📘 परीक्षा: NEET
📅 वर्ष: 2019 | सेट: R
🔵 प्रश्न 33: [CoF₆]³⁻ का चुम्बकीय स्वभाव क्या है?
🔴 ① अपचुम्बकीय
🟢 ② परमचुम्बकीय
🟡 ③ अचुम्बकीय
🔵 ④ कोई नहीं
🟢 उत्तर: ② परमचुम्बकीय
📘 परीक्षा: AIPMT
📅 वर्ष: 2011 | सेट: M
🔵 प्रश्न 34: [Fe(CN)₆]³⁻ और [Fe(H₂O)₆]³⁺ में क्या अंतर है?
🔴 ① दोनों का रंग समान
🟢 ② एक अपचुम्बकीय है, दूसरा परमचुम्बकीय
🟡 ③ दोनों अपचुम्बकीय
🔵 ④ दोनों रंगहीन
🟢 उत्तर: ② एक अपचुम्बकीय है, दूसरा परमचुम्बकीय
📘 परीक्षा: NEET
📅 वर्ष: 2020 | सेट: P
🔵 प्रश्न 35: [Cr(NH₃)₆]³⁺ में समन्वय संख्या क्या है?
🔴 ① 2
🟢 ② 4
🟡 ③ 6
🔵 ④ 3
🟢 उत्तर: ③ 6
📘 परीक्षा: NEET
📅 वर्ष: 2018 | सेट: S
🔵 प्रश्न 36: [Co(en)₂Cl₂]⁺ में कितने ज्यामितीय समावयव संभव हैं?
🔴 ① 1
🟢 ② 2
🟡 ③ 3
🔵 ④ कोई नहीं
🟢 उत्तर: ② 2
📘 परीक्षा: AIPMT
📅 वर्ष: 2012 | सेट: P
🔵 प्रश्न 37: कौन-सा यौगिक टेट्राकार्बोनिल निकेल कहलाता है?
🔴 ① [Ni(CO)₄]
🟢 ② [Ni(CN)₄]²⁻
🟡 ③ [Ni(NH₃)₆]²⁺
🔵 ④ [NiCl₄]²⁻
🟢 उत्तर: ① [Ni(CO)₄]
📘 परीक्षा: NEET
📅 वर्ष: 2021 | सेट: S
🔵 प्रश्न 38: [Cu(H₂O)₄]²⁺ का रंग क्या है?
🔴 ① रंगहीन
🟢 ② नीला
🟡 ③ हरा
🔵 ④ गुलाबी
🟢 उत्तर: ② नीला
📘 परीक्षा: NEET
📅 वर्ष: 2018 | सेट: Q
🔵 प्रश्न 39: [Fe(C₂O₄)₃]³⁻ आयन का लिगैण्ड प्रकार क्या है?
🔴 ① एकदन्त
🟢 ② द्विदन्त
🟡 ③ त्रिदन्त
🔵 ④ बहुदन्त
🟢 उत्तर: ② द्विदन्त
📘 परीक्षा: NEET
📅 वर्ष: 2019 | सेट: P
🔵 प्रश्न 40: कौन-सा लिगैण्ड तटस्थ है?
🔴 ① Cl⁻
🟢 ② H₂O
🟡 ③ CN⁻
🔵 ④ NO₂⁻
🟢 उत्तर: ② H₂O
📘 परीक्षा: AIPMT
📅 वर्ष: 2014 | सेट: M
🔵 प्रश्न 41: [Ni(CN)₄]²⁻ का संकरण dsp² क्यों होता है?
🔴 ① कमजोर क्षेत्र लिगैण्ड के कारण
🟢 ② प्रबल क्षेत्र लिगैण्ड के कारण
🟡 ③ चुम्बकीय प्रभाव के कारण
🔵 ④ तापमान के कारण
🟢 उत्तर: ② प्रबल क्षेत्र लिगैण्ड के कारण
📘 परीक्षा: NEET
📅 वर्ष: 2020 | सेट: S
🔵 प्रश्न 42: [Fe(H₂O)₆]²⁺ का चुम्बकीय स्वभाव क्या है?
🔴 ① अपचुम्बकीय
🟢 ② परमचुम्बकीय
🟡 ③ अचुम्बकीय
🔵 ④ कोई नहीं
🟢 उत्तर: ② परमचुम्बकीय
📘 परीक्षा: NEET
📅 वर्ष: 2016 | सेट: R
🔵 प्रश्न 43: कौन-सा यौगिक रंगहीन है?
🔴 ① [Zn(H₂O)₆]²⁺
🟢 ② [Fe(H₂O)₆]²⁺
🟡 ③ [Cu(H₂O)₆]²⁺
🔵 ④ [Co(NH₃)₆]³⁺
🟢 उत्तर: ① [Zn(H₂O)₆]²⁺
📘 परीक्षा: AIPMT
📅 वर्ष: 2011 | सेट: P
🔵 प्रश्न 44: [Ni(CN)₄]²⁻ और [NiCl₄]²⁻ में क्या भिन्नता है?
🔴 ① रंग
🟢 ② चुम्बकीय आचरण
🟡 ③ संकरण प्रकार
🔵 ④ उपरोक्त सभी
🟢 उत्तर: ④ उपरोक्त सभी
📘 परीक्षा: NEET
📅 वर्ष: 2019 | सेट: S
🔵 प्रश्न 45: [Fe(CN)₆]⁴⁻ और [Fe(CN)₆]³⁻ में कौन-सा अधिक स्थिर है?
🔴 ① [Fe(CN)₆]³⁻
🟢 ② [Fe(CN)₆]⁴⁻
🟡 ③ दोनों समान
🔵 ④ कोई नहीं
🟢 उत्तर: ② [Fe(CN)₆]⁴⁻
📘 परीक्षा: NEET
📅 वर्ष: 2021 | सेट: Q
🔵 प्रश्न 46: [CoF₆]³⁻ का संकरण प्रकार क्या है?
🔴 ① d²sp³
🟢 ② sp³d²
🟡 ③ dsp²
🔵 ④ sp²d²
🟢 उत्तर: ② sp³d²
📘 परीक्षा: NEET
📅 वर्ष: 2015 | सेट: P
🔵 प्रश्न 47: [Cr(C₂O₄)₃]³⁻ में कुल लिगैण्ड संख्या क्या है?
🔴 ① 3
🟢 ② 6
🟡 ③ 9
🔵 ④ 12
🟢 उत्तर: ② 6
📘 परीक्षा: NEET
📅 वर्ष: 2018 | सेट: Q
🔵 प्रश्न 48: [Fe(CO)₅] का संकरण क्या है?
🔴 ① dsp²
🟢 ② sp³d
🟡 ③ d²sp³
🔵 ④ sp³
🟢 उत्तर: ② sp³d
📘 परीक्षा: AIPMT
📅 वर्ष: 2013 | सेट: L
🔵 प्रश्न 49: [Fe(H₂O)₆]³⁺ में Fe की ऑक्सीकरण अवस्था क्या है?
🔴 ① +2
🟢 ② +3
🟡 ③ +4
🔵 ④ 0
🟢 उत्तर: ② +3
📘 परीक्षा: NEET
📅 वर्ष: 2019 | सेट: P
🔵 प्रश्न 50: [Cr(NH₃)₄Cl₂]⁺ के सिस समावयव का रंग क्या है?
🔴 ① नीला
🟢 ② हरा
🟡 ③ गुलाबी
🔵 ④ पीला
🟢 उत्तर: ② हरा
📘 परीक्षा: NEET
📅 वर्ष: 2022 | सेट: S
————————————————————————————————————————————————————————————————————————————
JEE MAINS पिछले सालों के प्रश्न
🔵 प्रश्न 1:
[Cu(NH₃)₄]²⁺ आयन का आकार क्या होता है?
🔴 ① चतुष्फलकीय
🟢 ② वर्ग समतलीय
🟡 ③ त्रिकोणीय
🔵 ④ रेखीय
🟢 उत्तर: ② वर्ग समतलीय
📘 परीक्षा: JEE Main
📅 वर्ष: 2019 | शिफ़्ट: अपराह्न
🔵 प्रश्न 2:
[Fe(CN)₆]⁴⁻ में Fe की संयोजकता क्या है?
🔴 ① +2
🟢 ② +3
🟡 ③ +4
🔵 ④ +1
🟢 उत्तर: ① +2
📘 परीक्षा: JEE Main
📅 वर्ष: 2016 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 3:
[Ni(CO)₄] यौगिक का ज्यामिति प्रकार क्या है?
🔴 ① चतुष्फलकीय
🟢 ② वर्ग समतलीय
🟡 ③ अष्टफलकीय
🔵 ④ त्रिकोणीय
🟢 उत्तर: ① चतुष्फलकीय
📘 परीक्षा: JEE Main
📅 वर्ष: 2014 | शिफ़्ट: अपराह्न
🔵 प्रश्न 4:
[Fe(CN)₆]³⁻ में Fe की चुंबकीय प्रकृति क्या है?
🔴 ① पैरामैग्नेटिक
🟢 ② डायमैग्नेटिक
🟡 ③ सुपरमैग्नेटिक
🔵 ④ एंटीमैग्नेटिक
🟢 उत्तर: ② डायमैग्नेटिक
📘 परीक्षा: JEE Main
📅 वर्ष: 2017 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 5:
[Co(NH₃)₆]³⁺ आयन का संख्यात्मक सहसंयोजन क्या है?
🔴 ① 3
🟢 ② 6
🟡 ③ 4
🔵 ④ 2
🟢 उत्तर: ② 6
📘 परीक्षा: JEE Main
📅 वर्ष: 2015 | शिफ़्ट: अपराह्न
🔵 प्रश्न 6:
[Pt(NH₃)₂Cl₂] में समावयवता का प्रकार क्या है?
🔴 ① आयनन समावयवता
🟢 ② ज्यामितीय समावयवता
🟡 ③ संयोजन समावयवता
🔵 ④ हाइड्रेट समावयवता
🟢 उत्तर: ② ज्यामितीय समावयवता
📘 परीक्षा: JEE Main
📅 वर्ष: 2013 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 7:
[Cr(H₂O)₆]Cl₃ में सहसंयोजन संख्या क्या है?
🔴 ① 3
🟢 ② 6
🟡 ③ 5
🔵 ④ 4
🟢 उत्तर: ② 6
📘 परीक्षा: JEE Main
📅 वर्ष: 2018 | शिफ़्ट: अपराह्न
🔵 प्रश्न 8:
Werner के सिद्धांत के अनुसार, प्राथमिक संयोजकता को क्या कहा जाता है?
🔴 ① सहसंयोजन
🟢 ② आयनिक संयोजकता
🟡 ③ धात्विक संयोजकता
🔵 ④ द्वितीयक संयोजकता
🟢 उत्तर: ② आयनिक संयोजकता
📘 परीक्षा: JEE Main
📅 वर्ष: 2019 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 9:
[Ni(CN)₄]²⁻ का आकार क्या है?
🔴 ① चतुष्फलकीय
🟢 ② वर्ग समतलीय
🟡 ③ अष्टफलकीय
🔵 ④ रेखीय
🟢 उत्तर: ② वर्ग समतलीय
📘 परीक्षा: JEE Main
📅 वर्ष: 2021 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 10:
[FeF₆]³⁻ आयन में Fe³⁺ की चुंबकीय प्रकृति क्या है?
🔴 ① पैरामैग्नेटिक
🟢 ② डायमैग्नेटिक
🟡 ③ सुपरमैग्नेटिक
🔵 ④ एंटीमैग्नेटिक
🟢 उत्तर: ① पैरामैग्नेटिक
📘 परीक्षा: JEE Main
📅 वर्ष: 2020 | शिफ़्ट: अपराह्न
🔵 प्रश्न 11:
[Cr(NH₃)₄Cl₂]⁺ में कितने ज्यामितीय समावयव सम्भव हैं?
🔴 ① 1
🟢 ② 2
🟡 ③ 3
🔵 ④ 4
🟢 उत्तर: ② 2
📘 परीक्षा: JEE Main
📅 वर्ष: 2018 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 12:
[Co(en)₃]³⁺ में ‘en’ का प्रकार क्या है?
🔴 ① एकदंती लिगैण्ड
🟢 ② द्विदंती लिगैण्ड
🟡 ③ त्रिदंती लिगैण्ड
🔵 ④ चतुदंती लिगैण्ड
🟢 उत्तर: ② द्विदंती लिगैण्ड
📘 परीक्षा: JEE Main
📅 वर्ष: 2016 | शिफ़्ट: अपराह्न
🔵 प्रश्न 13:
[Fe(C₂O₄)₃]³⁻ में C₂O₄²⁻ लिगैण्ड का प्रकार क्या है?
🔴 ① एकदंती
🟢 ② द्विदंती
🟡 ③ त्रिदंती
🔵 ④ बहुदंती
🟢 उत्तर: ② द्विदंती
📘 परीक्षा: JEE Main
📅 वर्ष: 2017 | शिफ़्ट: अपराह्न
🔵 प्रश्न 14:
[Cu(NH₃)₄]²⁺ के निर्माण में किस सिद्धान्त की पुष्टि होती है?
🔴 ① क्रिस्टल क्षेत्र सिद्धान्त
🟢 ② संयोजकता बन्ध सिद्धान्त
🟡 ③ आणविक कक्षक सिद्धान्त
🔵 ④ हाइब्रिडीकरण सिद्धान्त
🟢 उत्तर: ② संयोजकता बन्ध सिद्धान्त
📘 परीक्षा: JEE Main
📅 वर्ष: 2014 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 15:
Werner के सिद्धान्त में द्वितीयक संयोजकता को क्या कहा गया है?
🔴 ① आयनिक
🟢 ② सहसंयोजक
🟡 ③ प्राथमिक
🔵 ④ द्विध्रुवीय
🟢 उत्तर: ② सहसंयोजक
📘 परीक्षा: JEE Main
📅 वर्ष: 2015 | शिफ़्ट: अपराह्न
🔵 प्रश्न 16:
[Co(NH₃)₅Cl]SO₄ और [Co(NH₃)₅SO₄]Cl में कौन-सी समावयवता होती है?
🔴 ① संयोजन समावयवता
🟢 ② आयनन समावयवता
🟡 ③ ज्यामितीय
🔵 ④ हाइड्रेट
🟢 उत्तर: ② आयनन समावयवता
📘 परीक्षा: JEE Main
📅 वर्ष: 2013 | शिफ़्ट: अपराह्न
🔵 प्रश्न 17:
[Co(en)₂Cl₂]⁺ में समावयवता का प्रकार क्या है?
🔴 ① ज्यामितीय
🟢 ② प्रकाशीय
🟡 ③ दोनों
🔵 ④ कोई नहीं
🟢 उत्तर: ③ दोनों
📘 परीक्षा: JEE Main
📅 वर्ष: 2018 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 18:
संयोजन यौगिकों में लिगैण्ड का कार्य क्या होता है?
🔴 ① केंद्रीय धातु को स्थिर करना
🟢 ② विद्युत आवेश देना
🟡 ③ रंग प्रदान करना
🔵 ④ उपर्युक्त सभी
🟢 उत्तर: ④ उपर्युक्त सभी
📘 परीक्षा: JEE Main
📅 वर्ष: 2020 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 19:
संयोजन संख्या 4 वाले यौगिकों की सम्भावित ज्यामिति क्या होती है?
🔴 ① चतुष्फलकीय या वर्ग समतलीय
🟢 ② त्रिकोणीय
🟡 ③ अष्टफलकीय
🔵 ④ रेखीय
🟢 उत्तर: ① चतुष्फलकीय या वर्ग समतलीय
📘 परीक्षा: JEE Main
📅 वर्ष: 2019 | शिफ़्ट: अपराह्न
🔵 प्रश्न 20:
[Ni(CO)₄] में Ni की संकरण अवस्था क्या होती है?
🔴 ① dsp²
🟢 ② sp³
🟡 ③ sp²
🔵 ④ d²sp³
🟢 उत्तर: ② sp³
📘 परीक्षा: JEE Main
📅 वर्ष: 2017 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 21:
[Fe(H₂O)₆]²⁺ का रंग किस कारण होता है?
🔴 ① f-f संक्रमण
🟢 ② d-d संक्रमण
🟡 ③ चार्ज स्थानान्तरण
🔵 ④ कोई नहीं
🟢 उत्तर: ② d-d संक्रमण
📘 परीक्षा: JEE Main
📅 वर्ष: 2016 | शिफ़्ट: अपराह्न
🔵 प्रश्न 22:
[Ti(H₂O)₆]³⁺ का रंग नीला क्यों होता है?
🔴 ① f-f संक्रमण के कारण
🟢 ② d-d संक्रमण के कारण
🟡 ③ हाइड्रेशन ऊर्जा के कारण
🔵 ④ टक्कर प्रभाव के कारण
🟢 उत्तर: ② d-d संक्रमण के कारण
📘 परीक्षा: JEE Main
📅 वर्ष: 2018 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 23:
[Fe(CN)₆]⁴⁻ में Fe की संकरण अवस्था क्या है?
🔴 ① sp³
🟢 ② d²sp³
🟡 ③ dsp²
🔵 ④ sp²
🟢 उत्तर: ② d²sp³
📘 परीक्षा: JEE Main
📅 वर्ष: 2019 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 24:
[CoF₆]³⁻ में Co का संकरण क्या है?
🔴 ① sp³
🟢 ② d²sp³
🟡 ③ dsp²
🔵 ④ sp²
🟢 उत्तर: ② d²sp³
📘 परीक्षा: JEE Main
📅 वर्ष: 2021 | शिफ़्ट: अपराह्न
🔵 प्रश्न 25:
संयोजन यौगिकों में समावयवता किस कारण होती है?
🔴 ① लिगैण्डों की स्थिति के कारण
🟢 ② केंद्रीय परमाणु की स्थिति के कारण
🟡 ③ संकरण में परिवर्तन के कारण
🔵 ④ उपर्युक्त सभी
🟢 उत्तर: ④ उपर्युक्त सभी
📘 परीक्षा: JEE Main
📅 वर्ष: 2015 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 26:
[Co(NH₃)₅Cl]Cl₂ में Co की ऑक्सीकरण अवस्था क्या है?
🔴 ① +1
🟢 ② +3
🟡 ③ +2
🔵 ④ 0
🟢 उत्तर: ② +3
📘 परीक्षा: JEE Main
📅 वर्ष: 2019 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 27:
कौन-सा यौगिक आयनन समावयवता दिखाता है?
🔴 ① [Co(NH₃)₅Cl]SO₄ और [Co(NH₃)₅SO₄]Cl
🟢 ② [Co(en)₃]Cl₃
🟡 ③ [Co(NH₃)₄Cl₂]Cl
🔵 ④ [Fe(H₂O)₆]SO₄
🟢 उत्तर: ① [Co(NH₃)₅Cl]SO₄ और [Co(NH₃)₅SO₄]Cl
📘 परीक्षा: JEE Main
📅 वर्ष: 2016 | शिफ़्ट: अपराह्न
🔵 प्रश्न 28:
कौन-सा यौगिक प्रकाशीय समावयवता दिखाता है?
🔴 ① [Co(NH₃)₆]³⁺
🟢 ② [Co(en)₃]³⁺
🟡 ③ [Fe(CN)₆]³⁻
🔵 ④ [Ni(CO)₄]
🟢 उत्तर: ② [Co(en)₃]³⁺
📘 परीक्षा: JEE Main
📅 वर्ष: 2018 | शिफ़्ट: अपराह्न
🔵 प्रश्न 29:
[Pt(NH₃)₂Cl₂] में दो समावयव कौन-से हैं?
🔴 ① सिस और ट्रांस
🟢 ② अल्फा और बीटा
🟡 ③ संरचनात्मक
🔵 ④ आयनिक
🟢 उत्तर: ① सिस और ट्रांस
📘 परीक्षा: JEE Main
📅 वर्ष: 2017 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 30:
[NiCl₄]²⁻ का आकार क्या है?
🔴 ① वर्ग समतलीय
🟢 ② चतुष्फलकीय
🟡 ③ अष्टफलकीय
🔵 ④ रेखीय
🟢 उत्तर: ② चतुष्फलकीय
📘 परीक्षा: JEE Main
📅 वर्ष: 2020 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 31:
[Ni(CN)₄]²⁻ में Ni²⁺ का संकरण क्या है?
🔴 ① sp³
🟢 ② dsp²
🟡 ③ d²sp³
🔵 ④ sp²
🟢 उत्तर: ② dsp²
📘 परीक्षा: JEE Main
📅 वर्ष: 2021 | शिफ़्ट: अपराह्न
🔵 प्रश्न 32:
संयोजन यौगिकों के रंग का कारण क्या है?
🔴 ① d-d संक्रमण
🟢 ② f-f संक्रमण
🟡 ③ इलेक्ट्रॉन स्थानान्तरण
🔵 ④ उपर्युक्त सभी
🟢 उत्तर: ④ उपर्युक्त सभी
📘 परीक्षा: JEE Main
📅 वर्ष: 2019 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 33:
[Fe(H₂O)₆]²⁺ का रंग हरा क्यों होता है?
🔴 ① f-f संक्रमण
🟢 ② d-d संक्रमण
🟡 ③ चार्ज स्थानान्तरण
🔵 ④ हाइड्रेशन
🟢 उत्तर: ② d-d संक्रमण
📘 परीक्षा: JEE Main
📅 वर्ष: 2014 | शिफ़्ट: अपराह्न
🔵 प्रश्न 34:
[Cr(H₂O)₆]³⁺ आयन का रंग बैंगनी क्यों होता है?
🔴 ① f-f संक्रमण
🟢 ② d-d संक्रमण
🟡 ③ लिगैण्ड क्षेत्र प्रभाव
🔵 ④ आयनन
🟢 उत्तर: ② d-d संक्रमण
📘 परीक्षा: JEE Main
📅 वर्ष: 2016 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 35:
संयोजन यौगिकों में लिगैण्ड की “दंतता” का अर्थ है —
🔴 ① लिगैण्ड द्वारा इलेक्ट्रॉन युग्मों की संख्या
🟢 ② लिगैण्ड के आकार का मान
🟡 ③ ध्रुवण क्षमता
🔵 ④ समन्वय दूरी
🟢 उत्तर: ① लिगैण्ड द्वारा इलेक्ट्रॉन युग्मों की संख्या
📘 परीक्षा: JEE Main
📅 वर्ष: 2013 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 36:
कौन-सा यौगिक ऑक्सीकरण–अपचयन उत्प्रेरक के रूप में प्रयुक्त होता है?
🔴 ① [PtCl₆]²⁻
🟢 ② [Co(NH₃)₆]³⁺
🟡 ③ [Fe(CN)₆]⁴⁻
🔵 ④ [MnO₄]⁻
🟢 उत्तर: ③ [Fe(CN)₆]⁴⁻
📘 परीक्षा: JEE Main
📅 वर्ष: 2019 | शिफ़्ट: अपराह्न
🔵 प्रश्न 37:
कौन-सा लिगैण्ड बहुदंती (polydentate) है?
🔴 ① NH₃
🟢 ② EDTA⁴⁻
🟡 ③ H₂O
🔵 ④ Cl⁻
🟢 उत्तर: ② EDTA⁴⁻
📘 परीक्षा: JEE Main
📅 वर्ष: 2017 | शिफ़्ट: अपराह्न
🔵 प्रश्न 38:
[Ni(CO)₄] में Ni की चुंबकीय प्रकृति क्या है?
🔴 ① पैरामैग्नेटिक
🟢 ② डायमैग्नेटिक
🟡 ③ सुपरमैग्नेटिक
🔵 ④ एंटीमैग्नेटिक
🟢 उत्तर: ② डायमैग्नेटिक
📘 परीक्षा: JEE Main
📅 वर्ष: 2021 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 39:
[CuCl₄]²⁻ का आकार क्या है?
🔴 ① अष्टफलकीय
🟢 ② चतुष्फलकीय
🟡 ③ वर्ग समतलीय
🔵 ④ रेखीय
🟢 उत्तर: ② चतुष्फलकीय
📘 परीक्षा: JEE Main
📅 वर्ष: 2018 | शिफ़्ट: अपराह्न
🔵 प्रश्न 40:
[CoF₆]³⁻ का रंग पीला क्यों होता है?
🔴 ① f-f संक्रमण
🟢 ② d-d संक्रमण
🟡 ③ चार्ज स्थानान्तरण
🔵 ④ कोई नहीं
🟢 उत्तर: ② d-d संक्रमण
📘 परीक्षा: JEE Main
📅 वर्ष: 2020 | शिफ़्ट: अपराह्न
🔵 प्रश्न 41:
[Fe(C₂O₄)₃]³⁻ में Fe की संकरण अवस्था क्या है?
🔴 ① sp³
🟢 ② d²sp³
🟡 ③ dsp²
🔵 ④ sp²
🟢 उत्तर: ② d²sp³
📘 परीक्षा: JEE Main
📅 वर्ष: 2019 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 42:
संयोजन यौगिकों का नामकरण किस नियम पर आधारित होता है?
🔴 ① IUPAC नियम
🟢 ② Werner सिद्धान्त
🟡 ③ संयोजन नियम
🔵 ④ समावयवता सिद्धान्त
🟢 उत्तर: ① IUPAC नियम
📘 परीक्षा: JEE Main
📅 वर्ष: 2015 | शिफ़्ट: अपराह्न
🔵 प्रश्न 43:
[Ni(H₂O)₆]²⁺ का रंग हल्का हरा क्यों होता है?
🔴 ① d-d संक्रमण
🟢 ② f-f संक्रमण
🟡 ③ हाइड्रेशन
🔵 ④ टक्कर प्रभाव
🟢 उत्तर: ① d-d संक्रमण
📘 परीक्षा: JEE Main
📅 वर्ष: 2016 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 44:
[Fe(H₂O)₆]²⁺ और [Fe(CN)₆]⁴⁻ में कौन-सा अधिक स्थिर है?
🔴 ① [Fe(H₂O)₆]²⁺
🟢 ② [Fe(CN)₆]⁴⁻
🟡 ③ दोनों समान
🔵 ④ कोई नहीं
🟢 उत्तर: ② [Fe(CN)₆]⁴⁻
📘 परीक्षा: JEE Main
📅 वर्ष: 2022 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 45:
[Fe(CO)₅] का आकार क्या है?
🔴 ① त्रिकोणीय द्विपिरमिडीय
🟢 ② वर्ग समतलीय
🟡 ③ अष्टफलकीय
🔵 ④ चतुष्फलकीय
🟢 उत्तर: ① त्रिकोणीय द्विपिरमिडीय
📘 परीक्षा: JEE Main
📅 वर्ष: 2013 | शिफ़्ट: अपराह्न
🔵 प्रश्न 46:
[Cr(H₂O)₆]³⁺ में Cr³⁺ की संकरण अवस्था क्या है?
🔴 ① sp³
🟢 ② d²sp³
🟡 ③ dsp²
🔵 ④ sp²
🟢 उत्तर: ② d²sp³
📘 परीक्षा: JEE Main
📅 वर्ष: 2021 | शिफ़्ट: अपराह्न
🔵 प्रश्न 47:
संयोजन यौगिकों में उत्प्रेरक की भूमिका क्या है?
🔴 ① अभिक्रिया दर बढ़ाना
🟢 ② उत्पाद की उपज बढ़ाना
🟡 ③ ताप कम करना
🔵 ④ रंग बदलना
🟢 उत्तर: ① अभिक्रिया दर बढ़ाना
📘 परीक्षा: JEE Main
📅 वर्ष: 2017 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 48:
[PtCl₆]²⁻ में Pt की ऑक्सीकरण अवस्था क्या है?
🔴 ① +2
🟢 ② +4
🟡 ③ +6
🔵 ④ 0
🟢 उत्तर: ② +4
📘 परीक्षा: JEE Main
📅 वर्ष: 2014 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 49:
[Ni(CO)₄] और [Ni(CN)₄]²⁻ में Ni की चुंबकीय प्रकृति क्रमशः क्या है?
🔴 ① दोनों पैरामैग्नेटिक
🟢 ② दोनों डायमैग्नेटिक
🟡 ③ पहला डायमैग्नेटिक, दूसरा पैरामैग्नेटिक
🔵 ④ पहला पैरामैग्नेटिक, दूसरा डायमैग्नेटिक
🟢 उत्तर: ② दोनों डायमैग्नेटिक
📘 परीक्षा: JEE Main
📅 वर्ष: 2018 | शिफ़्ट: प्रातःकाल
🔵 प्रश्न 50:
संयोजन यौगिकों में लिगैण्डों का प्रभाव केंद्रीय धातु के किस गुण पर पड़ता है?
🔴 ① रंग
🟢 ② चुंबकत्व
🟡 ③ स्थायित्व
🔵 ④ उपर्युक्त सभी
🟢 उत्तर: ④ उपर्युक्त सभी
📘 परीक्षा: JEE Main
📅 वर्ष: 2024 | शिफ़्ट: प्रातःकाल
————————————————————————————————————————————————————————————————————————————
JEE ADVANCED पिछले सालों के प्रश्न
🔵 प्रश्न 1:
[Co(NH₃)₆]³⁺ आयन में कोबाल्ट की ऑक्सीकरण अवस्था क्या है?
🔴 ① +2
🟢 ② +3
🟡 ③ 0
🔵 ④ +1
🟢 उत्तर: ② +3
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2012 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–दिल्ली
🔵 प्रश्न 2:
[Ni(CO)₄] यौगिक की संरचना क्या है?
🔴 ① वर्गाकार समतलीय
🟢 ② चतु:मुखी (टेट्राहेड्रल)
🟡 ③ अष्टफलक
🔵 ④ त्रिकोणीय समतलीय
🟢 उत्तर: ② चतु:मुखी (टेट्राहेड्रल)
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2015 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–बॉम्बे
🔵 प्रश्न 3:
कौन-सा लिगैण्ड द्विदन्त (bidentate) है?
🔴 ① NH₃
🟢 ② C₂O₄²⁻
🟡 ③ Cl⁻
🔵 ④ CN⁻
🟢 उत्तर: ② C₂O₄²⁻
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2016 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–गुवाहाटी
🔵 प्रश्न 4:
[Fe(CN)₆]³⁻ आयन में Fe की चुंबकीय प्रकृति क्या है?
🔴 ① पराचुंबकीय
🟢 ② अप्राचुंबकीय
🟡 ③ अर्ध-चुंबकीय
🔵 ④ अत्यधिक चुंबकीय
🟢 उत्तर: ② अप्राचुंबकीय
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2013 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–मद्रास
🔵 प्रश्न 5:
[Fe(H₂O)₆]³⁺ आयन में Fe की संयोजकता क्या है?
🔴 ① +2
🟢 ② +3
🟡 ③ +4
🔵 ④ +1
🟢 उत्तर: ② +3
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2010 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–रूड़की
🔵 प्रश्न 6:
कौन-सा यौगिक ज्यामितीय समावयवता प्रदर्शित करता है?
🔴 ① [Co(NH₃)₆]³⁺
🟢 ② [Pt(NH₃)₂Cl₂]
🟡 ③ [Ni(CO)₄]
🔵 ④ [Cr(H₂O)₆]³⁺
🟢 उत्तर: ② [Pt(NH₃)₂Cl₂]
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2014 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–खड़गपुर
🔵 प्रश्न 7:
कौन-सा यौगिक प्रकाशीय समावयवता प्रदर्शित करता है?
🔴 ① [Co(en)₃]³⁺
🟢 ② [Ni(CN)₄]²⁻
🟡 ③ [Co(NH₃)₆]³⁺
🔵 ④ [Fe(CN)₆]³⁻
🟢 उत्तर: ① [Co(en)₃]³⁺
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2018 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–बॉम्बे
🔵 प्रश्न 8:
किस यौगिक में केन्द्रीय धातु की ऑक्सीकरण अवस्था +2 है?
🔴 ① [Cu(NH₃)₄]SO₄
🟢 ② [Co(NH₃)₆]Cl₃
🟡 ③ K₃[Fe(CN)₆]
🔵 ④ Na₃[AlF₆]
🟢 उत्तर: ① [Cu(NH₃)₄]SO₄
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2011 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–कानपुर
🔵 प्रश्न 9:
कौन-सा यौगिक वर्गाकार समतलीय संरचना रखता है?
🔴 ① [Ni(CO)₄]
🟢 ② [PtCl₄]²⁻
🟡 ③ [Fe(H₂O)₆]²⁺
🔵 ④ [Cr(CO)₆]
🟢 उत्तर: ② [PtCl₄]²⁻
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2016 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–गुवाहाटी
🔵 प्रश्न 10:
[Ni(CN)₄]²⁻ यौगिक की ज्यामिति क्या है?
🔴 ① चतु:मुखी
🟢 ② वर्गाकार समतलीय
🟡 ③ अष्टफलक
🔵 ④ त्रिकोणीय समतलीय
🟢 उत्तर: ② वर्गाकार समतलीय
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2017 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–मद्रास
🔵 प्रश्न 11:
कौन-सा यौगिक आयनीकरण समावयवता प्रदर्शित करता है?
🔴 ① [Co(NH₃)₅Cl]SO₄ और [Co(NH₃)₅SO₄]Cl
🟢 ② [Cu(NH₃)₄]SO₄ और [Cu(H₂O)₄]SO₄
🟡 ③ [Fe(H₂O)₆]³⁺ और [Fe(CN)₆]³⁻
🔵 ④ [Cr(H₂O)₆]³⁺ और [Cr(NH₃)₆]³⁺
🟢 उत्तर: ① [Co(NH₃)₅Cl]SO₄ और [Co(NH₃)₅SO₄]Cl
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2014 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–खड़गपुर
🔵 प्रश्न 12:
कौन-सा यौगिक संयोजन समावयवता प्रदर्शित करता है?
🔴 ① [Co(NH₃)₆][Cr(CN)₆] और [Cr(NH₃)₆][Co(CN)₆]
🟢 ② [Pt(NH₃)₂Cl₂] और [Pt(NH₃)₄Cl₂]
🟡 ③ [Ni(CO)₄] और [Ni(CN)₄]²⁻
🔵 ④ [Fe(H₂O)₆]²⁺ और [Fe(H₂O)₆]³⁺
🟢 उत्तर: ① [Co(NH₃)₆][Cr(CN)₆] और [Cr(NH₃)₆][Co(CN)₆]
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2010 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–रूड़की
🔵 प्रश्न 13:
कौन-सा यौगिक लिगैण्ड “en” (एथिलीन-डायमीन) को सम्मिलित करता है?
🔴 ① [Co(NH₃)₆]³⁺
🟢 ② [Co(en)₃]³⁺
🟡 ③ [Fe(C₂O₄)₃]³⁻
🔵 ④ [Ni(CO)₄]
🟢 उत्तर: ② [Co(en)₃]³⁺
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2017 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–मद्रास
🔵 प्रश्न 14:
[Fe(CN)₆]⁴⁻ आयन की चुंबकीय प्रकृति क्या है?
🔴 ① पराचुंबकीय
🟢 ② अप्राचुंबकीय
🟡 ③ द्विचुंबकीय
🔵 ④ अत्यधिक चुंबकीय
🟢 उत्तर: ② अप्राचुंबकीय
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2016 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–गुवाहाटी
🔵 प्रश्न 15:
[Co(NH₃)₄Cl₂]⁺ आयन में दो प्रकार की समावयवता सम्भव हैं —
🔴 ① ज्यामितीय और प्रकाशीय
🟢 ② आयनीकरण और समन्वय
🟡 ③ संरचनात्मक और शृंखला
🔵 ④ कोई नहीं
🟢 उत्तर: ① ज्यामितीय और प्रकाशीय
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2012 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–दिल्ली
🔵 प्रश्न 16:
कौन-सा यौगिक Werner के सिद्धांत की पुष्टि करता है?
🔴 ① [Co(NH₃)₆]Cl₃
🟢 ② [CoCl₃(NH₃)₃]
🟡 ③ [Cr(H₂O)₆]Cl₃
🔵 ④ [Fe(CN)₆]³⁻
🟢 उत्तर: ② [CoCl₃(NH₃)₃]
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2011 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–कानपुर
🔵 प्रश्न 17:
[Ni(CN)₄]²⁻ यौगिक में निकेल की संकरण अवस्था क्या है?
🔴 ① sp³
🟢 ② dsp²
🟡 ③ sp²
🔵 ④ d²sp³
🟢 उत्तर: ② dsp²
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2015 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–बॉम्बे
🔵 प्रश्न 18:
[Fe(H₂O)₆]²⁺ और [Fe(CN)₆]⁴⁻ आयनों की चुंबकीय प्रकृति में अंतर क्यों है?
🔴 ① दोनों अप्राचुंबकीय हैं
🟢 ② Fe²⁺ में d-कक्ष इलेक्ट्रॉनों की जोड़ीकरण “CN⁻” द्वारा कराया जाता है
🟡 ③ H₂O अधिक प्रबल क्षेत्रीय लिगैण्ड है
🔵 ④ दोनों पराचुंबकीय हैं
🟢 उत्तर: ② Fe²⁺ में d-कक्ष इलेक्ट्रॉनों की जोड़ीकरण “CN⁻” द्वारा कराया जाता है
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2016 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–गुवाहाटी
🔵 प्रश्न 19:
[Co(NH₃)₄Cl₂]⁺ आयन का संभावित ज्यामितीय रूप क्या है?
🔴 ① वर्गाकार समतलीय
🟢 ② अष्टफलक
🟡 ③ त्रिकोणीय समतलीय
🔵 ④ चतु:मुखी
🟢 उत्तर: ② अष्टफलक
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2014 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–खड़गपुर
🔵 प्रश्न 20:
Werner सिद्धांत के अनुसार केंद्रीय धातु परमाणु के दो प्रकार के संयोजन संख्या होती हैं:
🔴 ① प्राथमिक (आयनन) और द्वितीयक (संयोजन)
🟢 ② रासायनिक और भौतिक
🟡 ③ स्थायी और अस्थायी
🔵 ④ आयनिक और सहसंयोजक
🟢 उत्तर: ① प्राथमिक (आयनन) और द्वितीयक (संयोजन)
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2010 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–रूड़की
🔵 प्रश्न 21:
[Cr(NH₃)₆]³⁺ आयन में Cr की संकरण अवस्था क्या है?
🔴 ① d²sp³
🟢 ② sp³d²
🟡 ③ dsp²
🔵 ④ sp³
🟢 उत्तर: ① d²sp³
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2013 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–मद्रास
🔵 प्रश्न 22:
[CoCl₂(en)₂]⁺ आयन में कितने संभावित प्रकाशीय समावयव हो सकते हैं?
🔴 ① 0
🟢 ② 2
🟡 ③ 4
🔵 ④ 1
🟢 उत्तर: ② 2
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2015 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–बॉम्बे
🔵 प्रश्न 23:
[Ni(H₂O)₆]²⁺ पर “CN⁻” जैसे प्रबल लिगैण्ड का प्रभाव क्या होता है?
🔴 ① अप्राचुंबकीय से पराचुंबकीय में परिवर्तन
🟢 ② पराचुंबकीय से अप्राचुंबकीय में परिवर्तन
🟡 ③ चुंबकत्व पर कोई प्रभाव नहीं
🔵 ④ ऑक्सीकरण अवस्था बदल जाती है
🟢 उत्तर: ② पराचुंबकीय से अप्राचुंबकीय में परिवर्तन
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2017 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–मद्रास
🔵 प्रश्न 24:
[Cu(NH₃)₄]²⁺ यौगिक का रंग किसके कारण होता है?
🔴 ① d–d संक्रमण
🟢 ② आवेश संक्रमण
🟡 ③ π–π* संक्रमण
🔵 ④ s–p संक्रमण
🟢 उत्तर: ① d–d संक्रमण
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2011 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–कानपुर
🔵 प्रश्न 25:
कौन-सा यौगिक संपूर्णतः अप्राचुंबकीय है?
🔴 ① [Fe(CN)₆]⁴⁻
🟢 ② [Co(NH₃)₆]³⁺
🟡 ③ [Fe(H₂O)₆]²⁺
🔵 ④ [Ni(H₂O)₆]²⁺
🟢 उत्तर: ① [Fe(CN)₆]⁴⁻
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2018 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–बॉम्बे
🔵 प्रश्न 26:
[Fe(H₂O)₆]²⁺ आयन में Fe की इलेक्ट्रॉनिक विन्यास क्या है?
🔴 ① [Ar] 3d⁶
🟢 ② [Ar] 3d⁶ 4s⁰
🟡 ③ [Ar] 3d⁴ 4s²
🔵 ④ [Ar] 3d⁵ 4s¹
🟢 उत्तर: ② [Ar] 3d⁶ 4s⁰
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2012 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–दिल्ली
🔵 प्रश्न 27:
कौन-सा यौगिक प्रकाशीय समावयवता नहीं दिखाता?
🔴 ① [Cr(en)₃]³⁺
🟢 ② [Co(NH₃)₆]³⁺
🟡 ③ [PtCl₂(en)₂]²⁺
🔵 ④ [Fe(C₂O₄)₃]³⁻
🟢 उत्तर: ② [Co(NH₃)₆]³⁺
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2016 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–गुवाहाटी
🔵 प्रश्न 28:
[Cr(NH₃)₅Cl]Cl₂ में क्लोराइड आयनों की संख्या कितनी “आयनन” से जुड़ी है?
🔴 ① 2
🟢 ② 1
🟡 ③ 3
🔵 ④ 0
🟢 उत्तर: ① 2
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2014 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–खड़गपुर
🔵 प्रश्न 29:
[Fe(CO)₅] की ज्यामिति क्या है?
🔴 ① त्रिकोणीय द्विपिरामिडीय
🟢 ② अष्टफलक
🟡 ③ चतु:मुखी
🔵 ④ वर्गाकार समतलीय
🟢 उत्तर: ① त्रिकोणीय द्विपिरामिडीय
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2013 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–मद्रास
🔵 प्रश्न 30:
Werner के अनुसार [Co(NH₃)₆]Cl₃ में क्लोराइड आयनों की संख्या जो “आयनन” से जुड़ी है, वह क्या है?
🔴 ① 3
🟢 ② 0
🟡 ③ 2
🔵 ④ 1
🟢 उत्तर: ① 3
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2010 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–रूड़की
🔵 प्रश्न 31:
[CoCl₆]³⁻ आयन का संकरण क्या है?
🔴 ① sp³d²
🟢 ② d²sp³
🟡 ③ dsp²
🔵 ④ sp³
🟢 उत्तर: ① sp³d²
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2015 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–बॉम्बे
🔵 प्रश्न 32:
[Fe(CN)₆]³⁻ और [Fe(CN)₆]⁴⁻ की चुंबकीय प्रकृति में अंतर क्यों है?
🔴 ① दोनों में Fe की ऑक्सीकरण अवस्था भिन्न है
🟢 ② Fe³⁺ में एक अपविकसित इलेक्ट्रॉन होता है जबकि Fe²⁺ में सभी जोड़े हो जाते हैं
🟡 ③ लिगैण्ड पर निर्भर नहीं
🔵 ④ दोनों समान हैं
🟢 उत्तर: ② Fe³⁺ में एक अपविकसित इलेक्ट्रॉन होता है जबकि Fe²⁺ में सभी जोड़े हो जाते हैं
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2016 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–गुवाहाटी
🔵 प्रश्न 33:
[Ni(CO)₄] और [Ni(CN)₄]²⁻ के चुंबकीय स्वभाव में क्या अंतर है?
🔴 ① दोनों पराचुंबकीय हैं
🟢 ② [Ni(CO)₄] अप्राचुंबकीय है और [Ni(CN)₄]²⁻ भी अप्राचुंबकीय
🟡 ③ [Ni(CO)₄] अप्राचुंबकीय है और [Ni(CN)₄]²⁻ पराचुंबकीय
🔵 ④ दोनों चुंबकीय नहीं
🟢 उत्तर: ③ [Ni(CO)₄] अप्राचुंबकीय है और [Ni(CN)₄]²⁻ पराचुंबकीय
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2014 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–खड़गपुर
🔵 प्रश्न 34:
कौन-सा लिगैण्ड द्विदन्त (bidentate) है परंतु प्रकाशीय समावयवता दिखा सकता है?
🔴 ① en (एथिलीन-डायमीन)
🟢 ② C₂O₄²⁻ (ऑक्सालेट)
🟡 ③ H₂O
🔵 ④ NH₃
🟢 उत्तर: ② C₂O₄²⁻ (ऑक्सालेट)
📘 परीक्षा: संयुक्त प्रवेश परीक्षा (उन्नत)
📅 वर्ष: 2018 | पत्र: 1 | संस्थान: भारतीय प्रौद्योगिकी संस्थान–बॉम्बे
————————————————————————————————————————————————————————————————————————————
मॉडल प्रश्न पत्र, अभ्यास
🔵 प्रश्न 1:
उपसहसंयोजन यौगिक वे यौगिक हैं जिनमें —
🔴 ① केवल आयनिक बन्धन होते हैं
🟢 ② एक धातु परमाणु या आयन लिगैण्ड से संयोजित होता है
🟡 ③ केवल सहसंयोजक बन्धन होते हैं
🔵 ④ केवल अधातु आयन होते हैं
🟢 उत्तर: ② एक धातु परमाणु या आयन लिगैण्ड से संयोजित होता है
🎯 कठिनाई: NEET
🔵 प्रश्न 2:
लिगैण्ड क्या होता है?
🔴 ① केवल आयन
🟢 ② वह अणु या आयन जो संयोजक युग्म प्रदान करता है
🟡 ③ केवल अणु
🔵 ④ धातु आयन
🟢 उत्तर: ② वह अणु या आयन जो संयोजक युग्म प्रदान करता है
🎯 कठिनाई: NEET
🔵 प्रश्न 3:
संयोजन क्षेत्र सिद्धांत के अनुसार उपसहसंयोजन यौगिक में बन्धन किस प्रकार का होता है?
🔴 ① केवल आयनिक
🟢 ② सहसंयोजक प्रकृति का
🟡 ③ धात्विक
🔵 ④ वैन डर वाल
🟢 उत्तर: ② सहसंयोजक प्रकृति का
🎯 कठिनाई: NEET
🔵 प्रश्न 4:
लिगैण्ड द्वारा प्रदान किये गये इलेक्ट्रॉन युग्म को क्या कहा जाता है?
🔴 ① σ-बन्धन
🟢 ② सहसंयोजक युग्म
🟡 ③ आयनिक बन्धन
🔵 ④ π-बन्धन
🟢 उत्तर: ② सहसंयोजक युग्म
🎯 कठिनाई: NEET
🔵 प्रश्न 5:
[Cu(NH₃)₄]²⁺ में लिगैण्ड की संख्या कितनी है?
🔴 ① 2
🟢 ② 4
🟡 ③ 6
🔵 ④ 8
🟢 उत्तर: ② 4
🎯 कठिनाई: NEET
🔵 प्रश्न 6:
लिगैण्ड के प्रकार का निर्धारण किससे होता है?
🔴 ① विद्युतऋणात्मकता से
🟢 ② दाता परमाणुओं की संख्या से
🟡 ③ धातु की आयनीकरण ऊर्जा से
🔵 ④ धात्विक बन्धन से
🟢 उत्तर: ② दाता परमाणुओं की संख्या से
🎯 कठिनाई: NEET
🔵 प्रश्न 7:
एथिलीन डायमीन (en) किस प्रकार का लिगैण्ड है?
🔴 ① एकदन्त
🟢 ② द्विदन्त
🟡 ③ त्रिदन्त
🔵 ④ बहुदन्त
🟢 उत्तर: ② द्विदन्त
🎯 कठिनाई: NEET
🔵 प्रश्न 8:
EDTA⁴⁻ किस प्रकार का लिगैण्ड है?
🔴 ① एकदन्त
🟢 ② षट्दन्त
🟡 ③ त्रिदन्त
🔵 ④ द्विदन्त
🟢 उत्तर: ② षट्दन्त
🎯 कठिनाई: NEET
🔵 प्रश्न 9:
संयोजन संख्या (Coordination Number) क्या होती है?
🔴 ① लिगैण्डों की कुल संख्या
🟢 ② धातु आयन से जुड़े दाता परमाणुओं की संख्या
🟡 ③ सहसंयोजक बन्धों की संख्या
🔵 ④ आयनिक आवेश
🟢 उत्तर: ② धातु आयन से जुड़े दाता परमाणुओं की संख्या
🎯 कठिनाई: NEET
🔵 प्रश्न 10:
[Fe(CN)₆]⁴⁻ में Fe की संयोजन संख्या क्या है?
🔴 ① 3
🟢 ② 6
🟡 ③ 4
🔵 ④ 2
🟢 उत्तर: ② 6
🎯 कठिनाई: NEET
🔵 प्रश्न 11:
कौन-सा लिगैण्ड तटस्थ है?
🔴 ① Cl⁻
🟢 ② NH₃
🟡 ③ CN⁻
🔵 ④ NO₂⁻
🟢 उत्तर: ② NH₃
🎯 कठिनाई: NEET
🔵 प्रश्न 12:
कौन-सा लिगैण्ड द्विदन्त है?
🔴 ① H₂O
🟢 ② C₂O₄²⁻ (ऑक्सालेट)
🟡 ③ Cl⁻
🔵 ④ NH₃
🟢 उत्तर: ② C₂O₄²⁻ (ऑक्सालेट)
🎯 कठिनाई: NEET
🔵 प्रश्न 13:
संयोजन यौगिक [Co(NH₃)₆]Cl₃ में धातु आयन का आवेश क्या है?
🔴 ① +2
🟢 ② +3
🟡 ③ +1
🔵 ④ +4
🟢 उत्तर: ② +3
🎯 कठिनाई: NEET
🔵 प्रश्न 14:
संयोजन यौगिकों में केन्द्रीय धातु आयन क्या करता है?
🔴 ① केवल विद्युतऋणात्मकता दिखाता है
🟢 ② लिगैण्डों से इलेक्ट्रॉन युग्म स्वीकार करता है
🟡 ③ कोई प्रभाव नहीं डालता
🔵 ④ केवल आयनिक बन्धन बनाता है
🟢 उत्तर: ② लिगैण्डों से इलेक्ट्रॉन युग्म स्वीकार करता है
🎯 कठिनाई: NEET
🔵 प्रश्न 15:
संयोजन क्षेत्र में [CoCl₂(NH₃)₄]⁺ की संयोजन संख्या कितनी है?
🔴 ① 2
🟢 ② 6
🟡 ③ 4
🔵 ④ 3
🟢 उत्तर: ② 6
🎯 कठिनाई: NEET
🔵 प्रश्न 16:
संयोजन यौगिकों में “आयनन समावयवता” किससे उत्पन्न होती है?
🔴 ① दाता परमाणुओं के अन्तर से
🟢 ② लिगैण्डों के भीतर आयनों के विनिमय से
🟡 ③ इलेक्ट्रॉन संख्या परिवर्तन से
🔵 ④ धातु परिवर्तन से
🟢 उत्तर: ② लिगैण्डों के भीतर आयनों के विनिमय से
🎯 कठिनाई: NEET
🔵 प्रश्न 17:
[Fe(CN)₆]⁴⁻ में Fe का चुम्बकीय आचरण क्या होगा?
🔴 ① परामैग्नेटिक
🟢 ② डायमैग्नेटिक
🟡 ③ अत्यधिक चुम्बकीय
🔵 ④ तापमान पर निर्भर
🟢 उत्तर: ② डायमैग्नेटिक
🎯 कठिनाई: NEET
🔵 प्रश्न 18:
संयोजन यौगिक [Ni(CO)₄] में संयोजन संख्या क्या है?
🔴 ① 2
🟢 ② 4
🟡 ③ 6
🔵 ④ 8
🟢 उत्तर: ② 4
🎯 कठिनाई: NEET
🔵 प्रश्न 19:
कौन-सा सिद्धांत उपसहसंयोजन यौगिकों के रंग और चुम्बकीय गुण समझाता है?
🔴 ① संयोजन क्षेत्र सिद्धांत
🟢 ② क्रिस्टल क्षेत्र सिद्धांत
🟡 ③ संयोजन नियम सिद्धांत
🔵 ④ विद्युत सिद्धांत
🟢 उत्तर: ② क्रिस्टल क्षेत्र सिद्धांत
🎯 कठिनाई: NEET
🔵 प्रश्न 20:
[CoF₆]³⁻ का क्रिस्टल क्षेत्र विभाजन क्या है?
🔴 ① Δ₀ छोटा
🟢 ② Δ₀ बड़ा
🟡 ③ Δ₀ शून्य
🔵 ④ Δ₀ अनन्त
🟢 उत्तर: ① Δ₀ छोटा
🎯 कठिनाई: NEET
🔵 प्रश्न 21:
कौन-सा यौगिक उच्च स्पिन संयोजन है?
🔴 ① [Fe(CN)₆]⁴⁻
🟢 ② [Fe(H₂O)₆]²⁺
🟡 ③ [Ni(CO)₄]
🔵 ④ [Co(NH₃)₆]³⁺
🟢 उत्तर: ② [Fe(H₂O)₆]²⁺
🎯 कठिनाई: NEET
🔵 प्रश्न 22:
यदि Δ₀ > युग्मन ऊर्जा हो, तो यौगिक —
🔴 ① उच्च स्पिन
🟢 ② निम्न स्पिन
🟡 ③ परामैग्नेटिक
🔵 ④ आयनिक
🟢 उत्तर: ② निम्न स्पिन
🎯 कठिनाई: NEET
🔵 प्रश्न 23:
[Cr(H₂O)₆]³⁺ का रंग किस कारण होता है?
🔴 ① जल का अपघटन
🟢 ② d–d संक्रमण
🟡 ③ सहसंयोजक बन्ध
🔵 ④ लिगैण्ड की संरचना
🟢 उत्तर: ② d–d संक्रमण
🎯 कठिनाई: NEET
🔵 प्रश्न 24:
कौन-सा लिगैण्ड क्षेत्र विभाजन को सर्वाधिक बढ़ाता है?
🔴 ① Cl⁻
🟢 ② CN⁻
🟡 ③ H₂O
🔵 ④ NH₃
🟢 उत्तर: ② CN⁻
🎯 कठिनाई: NEET
🔵 प्रश्न 25:
संयोजन क्षेत्र सिद्धांत में ‘Δ₀’ का अर्थ क्या है?
🔴 ① यौगिक की ऊर्जा
🟢 ② d-कक्षकों का विभाजन ऊर्जा
🟡 ③ विद्युतऋणात्मकता
🔵 ④ द्रव्यमान
🟢 उत्तर: ② d-कक्षकों का विभाजन ऊर्जा
🎯 कठिनाई: NEET
🔵 प्रश्न 26:
यदि किसी उपसहसंयोजन यौगिक में संयोजन संख्या 6 है, तो उसका ज्यामितीय आकार सामान्यतः क्या होगा?
🔴 ① चतुर्भुजाकार
🟢 ② अष्टफलीय
🟡 ③ त्रिकोणीय
🔵 ④ वर्गाकार
🟢 उत्तर: ② अष्टफलीय
🎯 कठिनाई: JEE Main
🔵 प्रश्न 27:
[Ni(CN)₄]²⁻ और [NiCl₄]²⁻ के चुंबकीय व्यवहार में अन्तर क्यों है?
🔴 ① लिगैण्ड की प्रकृति भिन्न है
🟢 ② CN⁻ प्रबल क्षेत्र लिगैण्ड है जबकि Cl⁻ दुर्बल क्षेत्र लिगैण्ड है
🟡 ③ Ni का ऑक्सीकरण अवस्था अलग है
🔵 ④ आकार भिन्न है
🟢 उत्तर: ② CN⁻ प्रबल क्षेत्र लिगैण्ड है जबकि Cl⁻ दुर्बल क्षेत्र लिगैण्ड है
🎯 कठिनाई: JEE Main
🔵 प्रश्न 28:
[Ni(CN)₄]²⁻ का आकार क्या होता है?
🔴 ① अष्टफलीय
🟢 ② वर्गाकार
🟡 ③ चतुर्भुजाकार
🔵 ④ रेखीय
🟢 उत्तर: ② वर्गाकार
🎯 कठिनाई: JEE Main
🔵 प्रश्न 29:
[Fe(H₂O)₆]²⁺ और [Fe(CN)₆]⁴⁻ में से कौन-सा निम्न स्पिन यौगिक है?
🔴 ① [Fe(H₂O)₆]²⁺
🟢 ② [Fe(CN)₆]⁴⁻
🟡 ③ दोनों
🔵 ④ कोई नहीं
🟢 उत्तर: ② [Fe(CN)₆]⁴⁻
🎯 कठिनाई: JEE Main
🔵 प्रश्न 30:
[Co(NH₃)₅Cl]Cl₂ यौगिक में कौन-सा आयन संयोजन क्षेत्र के बाहर है?
🔴 ① Co³⁺
🟢 ② Cl⁻
🟡 ③ NH₃
🔵 ④ कोई नहीं
🟢 उत्तर: ② Cl⁻
🎯 कठिनाई: JEE Main
🔵 प्रश्न 31:
[Cr(H₂O)₄Cl₂]Cl में कितने समावयव सम्भव हैं?
🔴 ① 1
🟢 ② 2
🟡 ③ 3
🔵 ④ 4
🟢 उत्तर: ② 2
🎯 कठिनाई: JEE Main
🔵 प्रश्न 32:
ज्यामितीय समावयवता किस प्रकार के संयोजन यौगिकों में सम्भव होती है?
🔴 ① केवल आयनिक यौगिकों में
🟢 ② जब संयोजन संख्या 4 या 6 हो
🟡 ③ केवल 8 संयोजन संख्या में
🔵 ④ किसी में नहीं
🟢 उत्तर: ② जब संयोजन संख्या 4 या 6 हो
🎯 कठिनाई: JEE Main
🔵 प्रश्न 33:
[Pt(NH₃)₂Cl₂] के कितने ज्यामितीय समावयव सम्भव हैं?
🔴 ① 1
🟢 ② 2
🟡 ③ 3
🔵 ④ 4
🟢 उत्तर: ② 2 (cis और trans)
🎯 कठिनाई: JEE Main
🔵 प्रश्न 34:
[Co(en)₃]³⁺ यौगिक में कौन-सी समावयवता सम्भव है?
🔴 ① ज्यामितीय
🟢 ② प्रकाशीय
🟡 ③ आयनन
🔵 ④ कोई नहीं
🟢 उत्तर: ② प्रकाशीय
🎯 कठिनाई: JEE Main
🔵 प्रश्न 35:
[Fe(H₂O)₆]²⁺ का रंग कैसा होगा?
🔴 ① हल्का हरा
🟢 ② नीला
🟡 ③ लाल
🔵 ④ रंगहीन
🟢 उत्तर: ① हल्का हरा
🎯 कठिनाई: JEE Main
🔵 प्रश्न 36:
[Ti(H₂O)₆]³⁺ आयन बैंगनी रंग का क्यों होता है?
🔴 ① जल का विघटन
🟢 ② d–d संक्रमण के कारण
🟡 ③ आयनिक प्रभाव
🔵 ④ तापीय प्रभाव
🟢 उत्तर: ② d–d संक्रमण के कारण
🎯 कठिनाई: JEE Main
🔵 प्रश्न 37:
कौन-सा यौगिक परामैग्नेटिक है?
🔴 ① [Ni(CN)₄]²⁻
🟢 ② [NiCl₄]²⁻
🟡 ③ [Fe(CN)₆]⁴⁻
🔵 ④ [Co(NH₃)₆]³⁺
🟢 उत्तर: ② [NiCl₄]²⁻
🎯 कठिनाई: JEE Main
🔵 प्रश्न 38:
यदि Δ₀ < युग्मन ऊर्जा हो, तो क्या परिणाम होगा?
🔴 ① उच्च स्पिन जटिल बनेगा
🟢 ② निम्न स्पिन जटिल बनेगा
🟡 ③ आयनिक यौगिक बनेगा
🔵 ④ रंगहीन होगा
🟢 उत्तर: ① उच्च स्पिन जटिल बनेगा
🎯 कठिनाई: JEE Main
🔵 प्रश्न 39:
Werner के सिद्धांत के अनुसार, संयोजन यौगिकों में दो प्रकार की संयोजकताएँ होती हैं —
🔴 ① प्राथमिक एवं द्वितीयक
🟢 ② आयनिक एवं सहसंयोजक
🟡 ③ धात्विक एवं अधात्विक
🔵 ④ कोई नहीं
🟢 उत्तर: ① प्राथमिक एवं द्वितीयक
🎯 कठिनाई: JEE Main
🔵 प्रश्न 40:
Werner ने किस यौगिक के अध्ययन से अपने सिद्धांत की पुष्टि की?
🔴 ① [Co(NH₃)₆]Cl₃
🟢 ② [CrCl₃·6NH₃]
🟡 ③ [Fe(CN)₆]⁴⁻
🔵 ④ [Ni(CO)₄]
🟢 उत्तर: ② [CrCl₃·6NH₃]
🎯 कठिनाई: JEE Main
🚀 अब JEE Advanced स्तर के प्रश्न (41–50):
🔵 प्रश्न 41:
[Co(NH₃)₅Cl]Cl₂ और [Co(NH₃)₄Cl₂]Cl में कौन-सा अधिक आयनिक है?
🔴 ① पहला
🟢 ② दूसरा
🟡 ③ दोनों समान
🔵 ④ कोई नहीं
🟢 उत्तर: ① पहला ([Co(NH₃)₅Cl]Cl₂)
🎯 कठिनाई: JEE Advanced
🔵 प्रश्न 42:
[Cr(NH₃)₆]³⁺ में Cr की संकरण अवस्था क्या होगी?
🔴 ① sp³
🟢 ② d²sp³
🟡 ③ sp³d²
🔵 ④ dsp²
🟢 उत्तर: ② d²sp³
🎯 कठिनाई: JEE Advanced
🔵 प्रश्न 43:
[Ni(CN)₄]²⁻ में संकरण क्या है?
🔴 ① sp³
🟢 ② dsp²
🟡 ③ d²sp³
🔵 ④ sp³d²
🟢 उत्तर: ② dsp²
🎯 कठिनाई: JEE Advanced
🔵 प्रश्न 44:
[Fe(H₂O)₆]²⁺ में Fe की संकरण अवस्था क्या है?
🔴 ① dsp²
🟢 ② sp³d²
🟡 ③ d²sp³
🔵 ④ sp³
🟢 उत्तर: ② sp³d²
🎯 कठिनाई: JEE Advanced
🔵 प्रश्न 45:
संयोजन यौगिक [Cr(C₂O₄)₃]³⁻ में क्रोमियम की ऑक्सीकरण अवस्था क्या है?
🔴 ① +2
🟢 ② +3
🟡 ③ +6
🔵 ④ +4
🟢 उत्तर: ② +3
🎯 कठिनाई: JEE Advanced
🔵 प्रश्न 46:
कौन-सा यौगिक प्रकाशीय समावयवता दिखाता है?
🔴 ① [Co(NH₃)₆]³⁺
🟢 ② [Co(en)₃]³⁺
🟡 ③ [Fe(CN)₆]³⁻
🔵 ④ [Ni(CO)₄]
🟢 उत्तर: ② [Co(en)₃]³⁺
🎯 कठिनाई: JEE Advanced
🔵 प्रश्न 47:
[Co(NO₂)(NH₃)₅]Cl₂ और [Co(ONO)(NH₃)₅]Cl₂ किस प्रकार के समावयव हैं?
🔴 ① ज्यामितीय
🟢 ② लिङ्केज
🟡 ③ आयनन
🔵 ④ प्रकाशीय
🟢 उत्तर: ② लिङ्केज
🎯 कठिनाई: JEE Advanced
🔵 प्रश्न 48:
यदि किसी यौगिक का सूत्र [Pt(NH₃)₄][PtCl₆] हो, तो यह किस प्रकार का समावयव है?
🔴 ① समावयविक
🟢 ② समन्वयिक (Coordination isomerism)
🟡 ③ लिङ्केज
🔵 ④ ज्यामितीय
🟢 उत्तर: ② समन्वयिक
🎯 कठिनाई: JEE Advanced
🔵 प्रश्न 49:
[Cu(NH₃)₄]²⁺ में Cu का संकरण क्या है?
🔴 ① sp³
🟢 ② dsp²
🟡 ③ d²sp³
🔵 ④ sp³d²
🟢 उत्तर: ① sp³
🎯 कठिनाई: JEE Advanced
🔵 प्रश्न 50:
[Ni(CO)₄] यौगिक का चुम्बकीय व्यवहार कैसा है?
🔴 ① परामैग्नेटिक
🟢 ② डायमैग्नेटिक
🟡 ③ अत्यधिक चुम्बकीय
🔵 ④ तापीय
🟢 उत्तर: ② डायमैग्नेटिक
🎯 कठिनाई: JEE Advanced
————————————————————————————————————————————————————————————————————————————
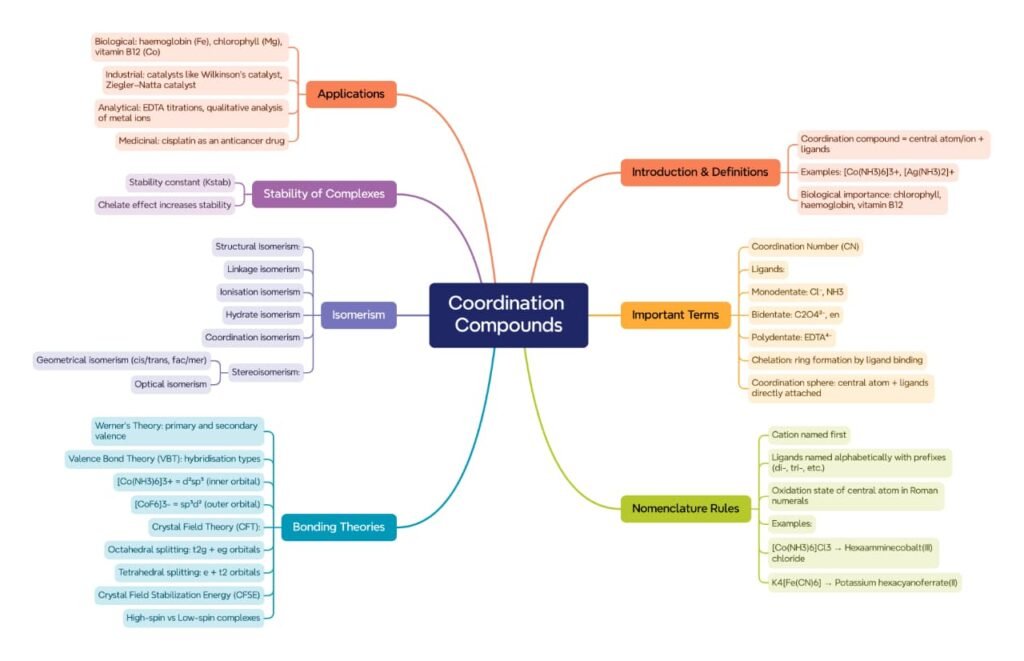
मस्तिष्क मानचित्र
————————————————————————————————————————————————————————————————————————————
