Class 11 : Physics (In Hindi) – अध्याय 11: ऊष्मागतिकी
पाठ का विश्लेषण एवं विवेचन
🌿 परिचय : ऊष्मागतिकी का आधार
ऊष्मागतिकी भौतिकी की वह शाखा है जिसमें ऊष्मा (Heat), कार्य (Work) और ऊर्जा (Energy) के बीच सम्बन्धों का अध्ययन किया जाता है।
यह न केवल भौतिक प्रणालियों के व्यवहार को समझाती है बल्कि यह बताती है कि किस प्रकार ऊर्जा एक रूप से दूसरे रूप में परिवर्तित होती है।
💡 सार:
ऊष्मागतिकी ऊर्जा के रूपान्तरण और संरक्षण के सिद्धान्तों पर आधारित है।
🟢 प्रणाली (System) और परिवेश (Surroundings)
🔹 प्रणाली (System): वह भाग जिसका अध्ययन किया जा रहा है।
🔹 परिवेश (Surroundings): प्रणाली के बाहर का भाग जो प्रणाली के साथ ऊर्जा या पदार्थ का आदान-प्रदान कर सकता है।
✏️ उदाहरण:
एक गैस से भरा पात्र — गैस है प्रणाली, और पात्र तथा वायु है परिवेश।
🔴 प्रणालियों के प्रकार
1️⃣ उदात्त प्रणाली (Open System):
ऊर्जा और पदार्थ दोनों का आदान-प्रदान कर सकती है।
➡️ उदाहरण: खुला पानी का पात्र।
2️⃣ बंद प्रणाली (Closed System):
केवल ऊर्जा का आदान-प्रदान करती है, पदार्थ का नहीं।
➡️ उदाहरण: बंद गैस पात्र।
3️⃣ नियत प्रणाली (Isolated System):
न तो ऊर्जा का और न पदार्थ का आदान-प्रदान करती है।
➡️ उदाहरण: थर्मस बोतल।
🟡 ऊष्मागतिक अवस्था (Thermodynamic State)
किसी गैस या प्रणाली की स्थिति को कुछ मानकों द्वारा वर्णित किया जाता है —
🔹 दाब (P),
🔹 आयतन (V),
🔹 तापमान (T)।
यदि ये तीनों ज्ञात हों, तो प्रणाली की स्थिति निश्चित मानी जाती है।
💡 स्थितिज समीकरण (Equation of State)
किसी गैस की ऊष्मागतिक अवस्था को जोड़ने वाला समीकरण —
P V = n R T
यह समीकरण आदर्श गैस का समीकरण कहलाता है।
🧠 प्रक्रियाओं के प्रकार (Thermodynamic Processes)
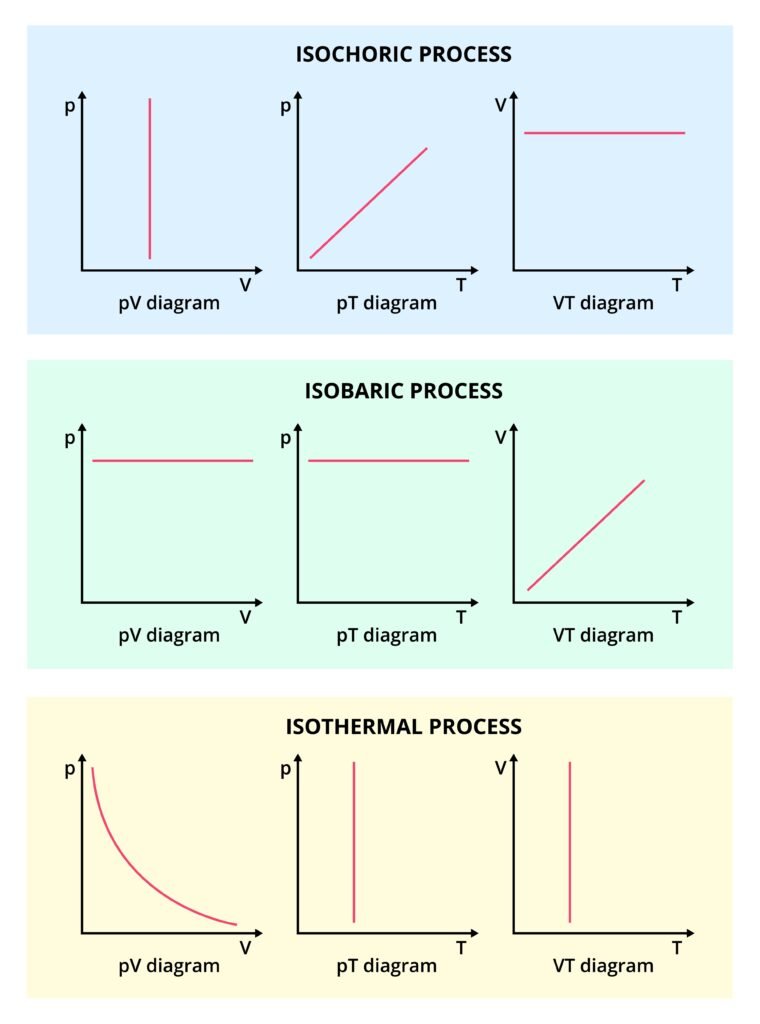
🔵 (1) समतापी प्रक्रिया (Isothermal Process)
➡️ तापमान स्थिर रहता है (ΔT = 0)।
➡️ ऊष्मा का आदान-प्रदान गैस और परिवेश के बीच होता है।
समीकरण: P V = स्थिर।
🟢 (2) समदाब प्रक्रिया (Isobaric Process)
➡️ दाब स्थिर रहता है (ΔP = 0)।
समीकरण: V ∝ T
🟠 (3) समआयतनिकप्रक्रिया (Isochoric Process)
➡️ आयतन स्थिर रहता है (ΔV = 0)।
समीकरण: P ∝ T
🔴 (4) रुद्धोष्म प्रक्रिया (Adiabatic Process)
➡️ कोई ऊष्मा आदान-प्रदान नहीं होता (Q = 0)।
समीकरण: P V^γ = स्थिर, जहाँ γ = Cₚ / Cᵥ।
🌿 ऊष्मागतिकी का प्रथम नियम (First Law of Thermodynamics)
यह ऊर्जा संरक्षण का नियम है।
✏️ विधान:
ऊष्मा और कार्य परस्पर रूपान्तरित हो सकते हैं, परन्तु कुल ऊर्जा स्थिर रहती है।
समीकरण:
ΔQ = ΔU + ΔW
जहाँ —
🔹 ΔQ = प्रणाली को दी गई ऊष्मा
🔹 ΔU = आन्तरिक ऊर्जा में परिवर्तन
🔹 ΔW = प्रणाली द्वारा किया गया कार्य
💡 यदि गैस का प्रसार हो: ΔW = +P ΔV
💡 यदि गैस का संकुचन हो: ΔW = −P ΔV
🔵 आन्तरिक ऊर्जा (Internal Energy)
किसी प्रणाली के अणुओं की सूक्ष्म गति और पारस्परिक बलों से सम्बद्ध कुल ऊर्जा को आन्तरिक ऊर्जा कहते हैं।
यह तापमान, दाब और आयतन पर निर्भर करती है।
🟢 कार्य (Work) की परिभाषा
यदि गैस किसी बाहरी दाब के विरुद्ध ΔV आयतन का प्रसार करे, तो किया गया कार्य —
W = P ΔV
समतापी प्रक्रिया में —
W = n R T ln(V₂ / V₁)
🔴 ऊष्मा (Heat)
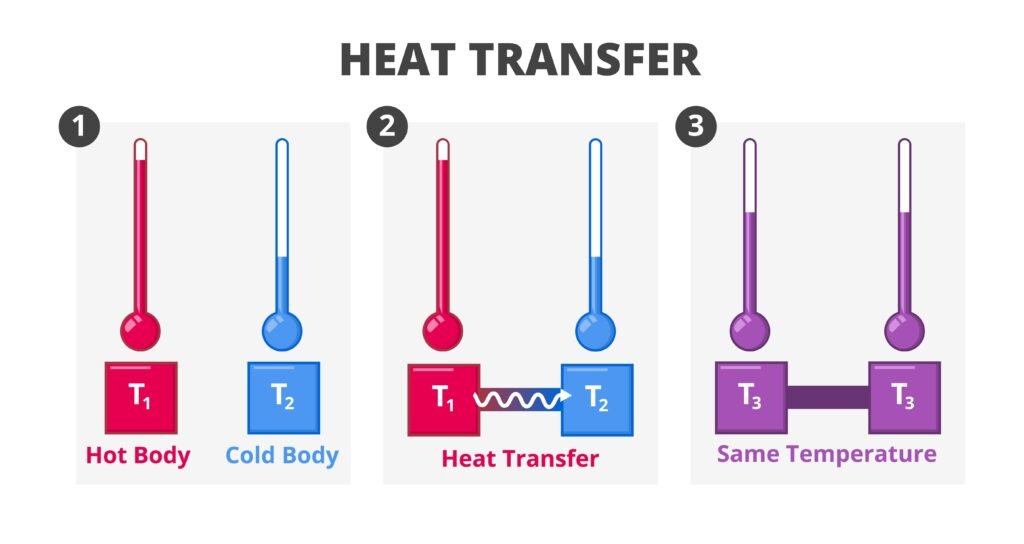
ऊष्मा ऊर्जा का वह रूप है जो तापमान के अन्तर के कारण एक प्रणाली से दूसरी में प्रवाहित होती है।
➡️ जब प्रणाली ऊष्मा प्राप्त करती है, Q धनात्मक होता है।
➡️ जब प्रणाली ऊष्मा खोती है, Q ऋणात्मक होता है।
💡 विशिष्ट ऊष्मा (Specific Heat)
किसी पदार्थ की इकाई द्रव्यमान का तापमान 1°C बढ़ाने के लिए आवश्यक ऊष्मा की मात्रा।
नियत आयतन पर विशिष्ट ऊष्मा: Cᵥ
नियत दाब पर विशिष्ट ऊष्मा: Cₚ
γ = Cₚ / Cᵥ
🌿 ऊष्मागतिकी का द्वितीय नियम (Second Law of Thermodynamics)
✴️ विभिन्न रूप में कथन:
1️⃣ क्लॉसियस कथन: ऊष्मा स्वतः ठण्डे पिण्ड से गरम पिण्ड में नहीं जा सकती।
2️⃣ केल्विन-प्लांक कथन: किसी एक ऊष्मा स्रोत से प्राप्त समस्त ऊष्मा को कार्य में परिवर्तित नहीं किया जा सकता।
💡 यह नियम बताता है कि ऊर्जा परिवर्तन में दिशा का निर्धारण होता है।
🧠 एंट्रॉपी (Entropy)
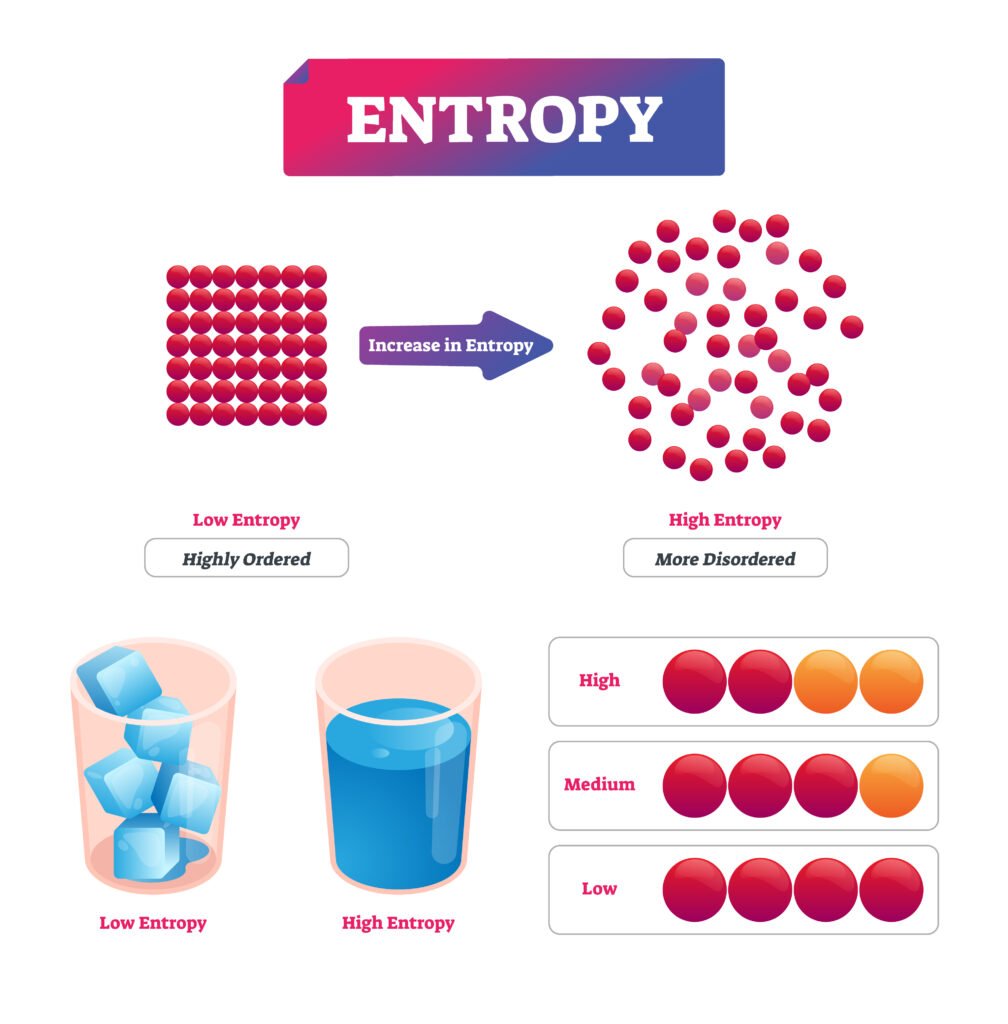
किसी प्रणाली की अव्यवस्था का माप एंट्रॉपी (S) कहलाती है।
समतापी प्रक्रिया के लिए —
ΔS = Q / T
➡️ यदि ΔS = 0 ⇒ प्रत्यावर्ती प्रक्रिया (Reversible Process)
➡️ यदि ΔS > 0 ⇒ अप्रत्यावर्ती प्रक्रिया (Irreversible Process)
⚡ अदियाबतिक प्रक्रिया में सम्बन्ध (Relation in Adiabatic Process)
P V^γ = स्थिर
T V^(γ−1) = स्थिर
T P^((1−γ)/γ) = स्थिर
💡 γ = Cₚ / Cᵥ का मान गैस के प्रकार पर निर्भर करता है।
🔵 ऊष्मा इंजन (Heat Engine)
ऊष्मा इंजन एक ऐसी युक्ति है जो ऊष्मा ऊर्जा को यांत्रिक कार्य में परिवर्तित करती है।
घटक:
1️⃣ ऊष्मा स्रोत (Source)
2️⃣ कार्यकारी पदार्थ (Working Substance)
3️⃣ ऊष्मा पात्र (Sink)
दक्षता (η):
η = W / Q₁ = 1 − (Q₂ / Q₁)
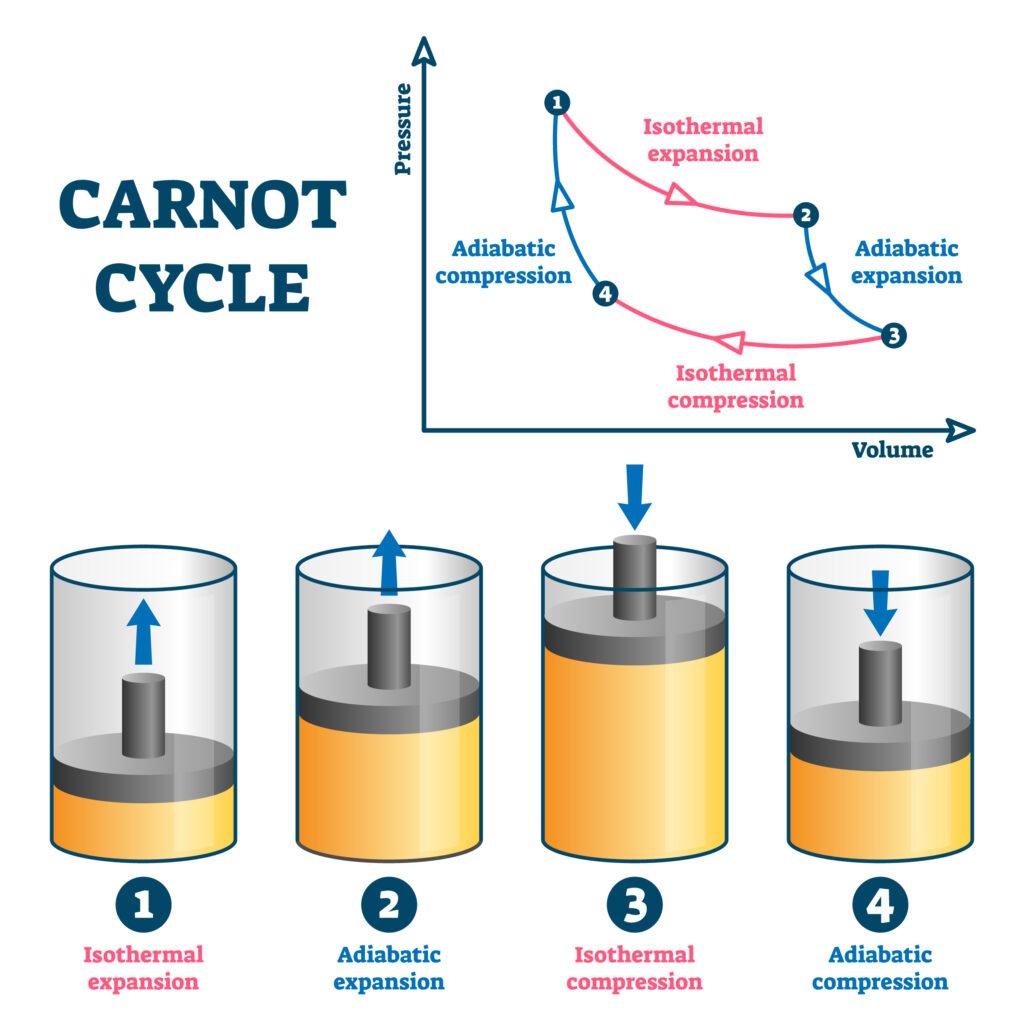
🟢 कार्नो इंजन (Carnot Engine)
सदी का सर्वाधिक दक्ष इंजन जिसका चक्र चार प्रत्यावर्ती प्रक्रियाओं पर आधारित होता है —
🔹 दो समतापी
🔹 दो अदियाबतिक
दक्षता:
η = 1 − (T₂ / T₁)
जहाँ T₁ = स्रोत का तापमान, T₂ = पात्र का तापमान।
🔴 एंट्रॉपी और अपरिवर्तनीयता
किसी वास्तविक इंजन में कुछ ऊर्जा हमेशा अपव्यय होती है, जिससे एंट्रॉपी बढ़ती है।
इसलिए वास्तविक प्रक्रिया सदैव अप्रत्यावर्ती (Irreversible) होती है।
🌿 ऊष्मागतिक संतुलन (Thermodynamic Equilibrium)
यदि प्रणाली में कोई परिवर्तन स्वतः नहीं हो रहा हो, तो वह ऊष्मागतिक संतुलन की अवस्था में होती है।
इसमें तीन संतुलन शामिल होते हैं —
🔹 तापीय संतुलन
🔹 यांत्रिक संतुलन
🔹 रासायनिक संतुलन
💡 ऊष्मागतिक पहचान (Thermodynamic Identity)
किसी सूक्ष्म परिवर्तन के लिए —
dQ = dU + P dV
यह ऊष्मागतिकी के प्रथम नियम का अवकल रूप है।
🟢 भाग 2 – सारांश (Summary ~300 शब्द)
🔸 ऊष्मागतिकी ऊर्जा और कार्य के बीच सम्बन्ध बताने वाला विज्ञान है।
🔸 प्रणाली तीन प्रकार की होती है — उदात्त, बंद, और नियत।
🔸 अवस्था चरों (P, V, T) द्वारा प्रणाली की स्थिति निर्धारित होती है।
🔸 आदर्श गैस का समीकरण: P V = n R T।
🔸 मुख्य प्रक्रियाएँ —
• समतापी (T स्थिर)
• समदाब (P स्थिर)
• समवॉलकीय (V स्थिर)
• अदियाबतिक (Q = 0)।
🔸 ऊष्मागतिकी का प्रथम नियम — ऊर्जा संरक्षण का नियम (ΔQ = ΔU + ΔW)।
🔸 द्वितीय नियम — ऊर्जा रूपान्तरण की दिशा बताता है।
🔸 एंट्रॉपी (S) — अव्यवस्था का माप।
🔸 कार्नो इंजन की दक्षता: η = 1 − (T₂ / T₁)।
🔸 वास्तविक इंजन सदैव अप्रत्यावर्ती होते हैं।
📝 Quick Recap (संक्षिप्त पुनरावृत्ति)
1️⃣ ऊष्मागतिकी ऊर्जा और कार्य के परस्पर रूपान्तरण का अध्ययन है।
2️⃣ ΔQ = ΔU + ΔW — ऊर्जा संरक्षण का गणितीय रूप।
3️⃣ कार्नो इंजन की अधिकतम दक्षता तापमानों पर निर्भर करती है।
4️⃣ एंट्रॉपी का वृद्धि सिद्धान्त प्रकृति की दिशा बताता है।
5️⃣ कोई भी ऊष्मा इंजन 100% दक्ष नहीं हो सकता।
————————————————————————————————————————————————————————————————————————————
पाठ्यपुस्त के प्रश्न
🔷 प्रश्न 11.1
कोई गीज़र 3.0 लीटर प्रति मिनट की दर से बहते हुए जल को 27°C से 77°C तक गर्म करता है। यदि गीज़र का प्रतिफलन (दक्षता) 95% है, तो ईंधन के दहन की दर क्या होगी?
मान लें कि ईंधन का ऊष्मा-मान 4.0×10⁴ J/g है।
उत्तर:
✏️ दिया गया:
जल की मात्रा प्रति मिनट = 3.0 लीटर = 3.0×10⁻³ m³
जल का घनत्व = 10³ kg/m³ ⇒ द्रव्यमान m = 3.0 kg
ΔT = 77 − 27 = 50°C
जल की विशिष्ट ऊष्मा = 4.2×10³ J/(kg·°C)
दक्षता (η) = 95% = 0.95
ईंधन की ऊष्मा क्षमता = 4.0×10⁴ J/g
🟢 चरण 1: जल को दी गई ऊष्मा
Q = m c ΔT
➡️ Q = 3.0 × 4.2×10³ × 50 = 6.3×10⁵ J
🟡 चरण 2: कुल ऊष्मा ईंधन द्वारा दी गई
η = उपयोगी ऊष्मा / कुल ऊष्मा
➡️ कुल ऊष्मा = Q / η = 6.3×10⁵ / 0.95 = 6.63×10⁵ J
🔵 चरण 3: ईंधन का द्रव्यमान
m_fuel = (कुल ऊष्मा) / (ईंधन की ऊष्मा क्षमता)
➡️ m_fuel = 6.63×10⁵ / 4.0×10⁴ = 16.6 g
🔴 चरण 4: समय = 1 मिनट ⇒ दहन की दर
Rate = 16.6 g/min
✔️ अतः ईंधन की दहन दर 16.6 ग्राम प्रति मिनट है।
🔷 प्रश्न 11.2
2.0×10⁻² kg नाइट्रोजन (स्थिर दाब पर) का तापमान 45°C बढ़ाने के लिए कितनी ऊष्मा दी जानी चाहिए?
(N₂ का आणविक द्रव्यमान = 28; R = 8.3 J·mol⁻¹·K⁻¹)
उत्तर:
✏️ दिया गया:
m = 2.0×10⁻² kg = 20 g
M = 28 g/mol
ΔT = 45°C = 45 K
R = 8.3 J·mol⁻¹·K⁻¹
🟢 चरण 1: मोलों की संख्या
n = m / M = 20 / 28 = 0.714 mol
🟡 चरण 2: नाइट्रोजन द्विपरमाणुक गैस ⇒ Cv = (5/2)R, Cp = (7/2)R
🔵 चरण 3: स्थिर दाब पर ऊष्मा
Q = n Cp ΔT
➡️ Q = 0.714 × (7/2) × 8.3 × 45
💡 Q = 0.714 × 3.5 × 8.3 × 45
= 0.714 × 1306.5
= 933 J
✔️ अतः दी गई ऊष्मा = 9.3×10² J (लगभग 933 J)
🔷 प्रश्न 11.3
कथन सही या गलत बताइए —
(a) स्थिर-दाब प्रक्रिया में, गैस को दी गई ऊष्मा उसका आंतरिक ऊर्जा परिवर्तन तथा बाह्य कार्य दोनों के योग के बराबर होती है।
(b) स्थिर-आयतन प्रक्रिया में कोई कार्य नहीं होता।
(c) समतापी प्रक्रिया में गैस की आंतरिक ऊर्जा में कोई परिवर्तन नहीं होता।
(d) ऊष्मा संचरण (हीट ट्रांसफर) का तात्पर्य ऊर्जा का तापांतर के कारण प्रवाह है।
उत्तर:
🟢 (a) ✔️ सही — क्योंकि Q = ΔU + W (ऊष्मागतिक प्रथम नियम)
🟡 (b) ✔️ सही — स्थिर आयतन पर ΔV = 0 ⇒ W = 0
🔵 (c) ✔️ सही — समतापी प्रक्रिया में ΔT = 0 ⇒ ΔU = 0
🔴 (d) ✔️ सही — तापांतर के कारण ऊर्जा का प्रवाह ही ऊष्मा कहलाता है।
🔷 प्रश्न 11.5
(शब्दशः पाठ धुंधला है; पर आशय स्पष्ट है) — एक ऊष्मा-इंजन एक चक्र में उच्च ताप-भंडार A से ऊष्मा ग्रहण करता है और निम्न ताप-भंडार B को 22.3 J ऊष्मा त्यागता है। यदि एक चक्र में किया गया उपयोगी कार्य = 9.35 cal है, तो एक चक्र में भंडार A से ग्रहण की गई ऊष्मा कितनी है?
(1 cal = 4.19 J)
उत्तर:
✏️ दिया गया:
🔵 त्यागी गई ऊष्मा (Q₂) = 22.3 J
🟢 किया गया कार्य (W) = 9.35 cal = 9.35 × 4.19 J = 39.1 J (लगभग)
💡 ऊष्मागतिक प्रथम नियम (एक चक्र):
🔸 Q₁ = W + Q₂ (यहाँ Q₁ = भंडार A से ग्रहण ऊष्मा)
➡️ Q₁ = 39.1 J + 22.3 J = 61.4 J
✔️ उत्तर: एक चक्र में भंडार A से ग्रहण ऊष्मा ≈ 61.4 J (या ≈ 14.7 cal, क्योंकि 61.4/4.19 ≈ 14.7).
💡 (वैकल्पिक) दक्षता η = W/Q₁ = 39.1 / 61.4 ≈ 0.64 (≈ 64%).
🔷 प्रश्न 11.6
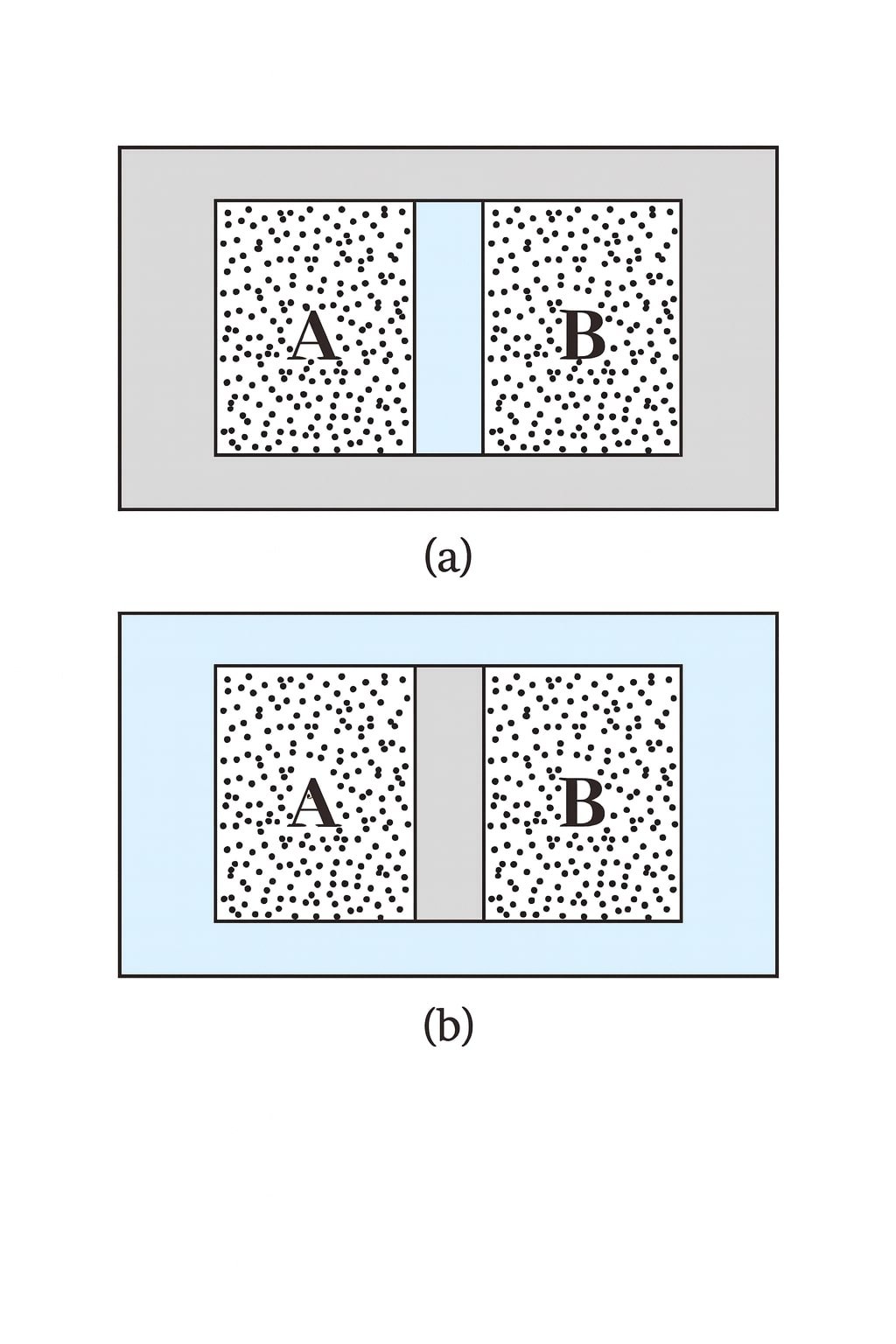
(मानक मुक्त-प्रसार स्थिति) — एक कठोर, ऊष्मारुद्ध पात्र दो समान आयतन वाले भागों A व B में विभक्त है। A में आदर्श गैस है (ताप T, दाब P), B निर्वात है। नलिका तुरन्त खोली जाती है। बताइए:
(a) A व B में अंतिम दाब क्या होगा?
(b) अंतिम तापमान क्या होगा?
(c) गैस द्वारा किया गया कार्य कितना है?
(d) गैस की आंतरिक ऊर्जा में कुल परिवर्तन कितना है?
उत्तर:
✏️ स्थितियाँ: पात्र ऊष्मारुद्ध ⇒ Q = 0, दीवारें कठोर ⇒ बाह्य पर कोई पिस्टन-कार्य नहीं। प्रसार निर्वात में मुक्त-प्रसार है। आदर्श गैस।
(a) 🔵 अंतिम दाब: कुल आयतन दुगुना हो जाता है (V → 2V)। आदर्श गैस के लिए सम ताप स्थिति में P ∝ 1/V, अतः
➡️ अंतिम दाब P’ = P/2।
(b) 🟢 अंतिम तापमान: मुक्त-प्रसार में Q = 0, W = 0 ⇒ ΔU = 0। आदर्श गैस के लिए U = f(T) मात्र, अतः ΔU = 0 ⇒ T’ = T।
✔️ ताप अपरिवर्तित।
(c) 🟡 किया गया कार्य: निर्वात के विरुद्ध प्रसार में कोई प्रतिरोध नहीं ⇒ बाह्य कार्य W = 0।
(d) 🔴 आंतरिक ऊर्जा परिवर्तन: ΔU = Q − W = 0 − 0 = 0।
🔷 प्रश्न 11.7
एक हीटर किसी तंत्र को 100 W की दर से ऊष्मा देता है और तंत्र 75 J s⁻¹ की दर से कार्य करता है। तंत्र की आंतरिक ऊर्जा किस दर से बढ़ेगी?
उत्तर:
✏️ प्रथम नियम (दर के रूप में):
🔹 dQ/dt = dU/dt + dW/dt
दिया गया: dQ/dt = 100 J s⁻¹, dW/dt = 75 J s⁻¹
➡️ dU/dt = dQ/dt − dW/dt = 100 − 75 = 25 J s⁻¹
✔️ आंतरिक ऊर्जा की वृद्धि की दर = 25 J s⁻¹।
🔷 प्रश्न 11.8
चित्र में ऊष्मागतिकीय तंत्र को बिन्दु D (600 N/m², 2.0 m³) से बिन्दु E (300 N/m², 5.0 m³) तक ले जाने की प्रक्रिया दिखाई गई है।
रेखीय (सीधी) रेखा DE के साथ तंत्र को ले जाया गया है।
गणना कीजिए कि इस प्रक्रिया में गैस द्वारा किया गया कार्य कितना है।
उत्तर:
✏️ दिया गया:
🔹 प्रारंभिक बिंदु D : P₁ = 600 N/m², V₁ = 2.0 m³
🔹 अंतिम बिंदु E : P₂ = 300 N/m², V₂ = 5.0 m³
🔹 प्रक्रिया — सीधी रेखा (linear) ⇒ दाब आयतन के साथ समान रूप से घटता है।
🟢 चरण 1: दाब और आयतन के बीच संबंध
रेखीय परिवर्तन के लिए दाब P औसत के रूप में लिखा जा सकता है —
➡️ P_avg = (P₁ + P₂) / 2
P_avg = (600 + 300) / 2 = 450 N/m²
🟡 चरण 2: किया गया कार्य
कार्य (W) = औसत दाब × आयतन परिवर्तन
➡️ W = P_avg × (V₂ − V₁)
W = 450 × (5.0 − 2.0)
W = 450 × 3.0 = 1350 J
🔵 चरण 3: दिशा की जाँच
चूँकि तंत्र का आयतन बढ़ रहा है (2 m³ → 5 m³),
इसलिए गैस द्वारा बाह्य कार्य किया गया है।
✔️ अतः गैस द्वारा किया गया कार्य = 1.35×10³ J
💡 अतिरिक्त अवधारणा (Concept):
यदि वही प्रक्रिया विपरीत दिशा (E → D) में होती, तो
कार्य W = −1350 J होता (क्योंकि गैस पर कार्य किया जाता)।
✅ अंतिम उत्तर:
गैस द्वारा किया गया कार्य = 1350 J (E दिशा में आयतन वृद्धि के साथ)
————————————————————————————————————————————————————————————————————————————
अन्य महत्वपूर्ण प्रश्न
(CBSE MODEL प्रश्न पत्र)
सिर्फ इसी पाठ से निर्मित CBSE MODEL प्रश्न पत्र।
🔵 Section A – बहुविकल्पीय प्रश्न (Q1–Q18)
Question 1. ऊष्मागतिकी का अध्ययन किससे सम्बन्धित है?
🔵 (A) केवल ऊष्मा से
🟢 (B) केवल कार्य से
🟠 (C) ऊष्मा, कार्य और ऊर्जा के परस्पर सम्बन्ध से
🔴 (D) केवल ऊर्जा संरक्षण से
Answer: (C) ऊष्मा, कार्य और ऊर्जा के परस्पर सम्बन्ध से
Question 2. निम्नलिखित में से कौन-सी प्रणाली उदात्त प्रणाली (Open system) है?
🔵 (A) थर्मस बोतल
🟢 (B) बन्द गैस पात्र
🟠 (C) उबलता हुआ पानी
🔴 (D) सील किया हुआ सिलेंडर
Answer: (C) उबलता हुआ पानी
Question 3. समतापी प्रक्रिया में क्या स्थिर रहता है?
🔵 (A) तापमान
🟢 (B) दाब
🟠 (C) आयतन
🔴 (D) ऊर्जा
Answer: (A) तापमान
Question 4. समदाब प्रक्रिया में कार्य का सूत्र क्या है?
🔵 (A) W = nRΔT
🟢 (B) W = PΔV
🟠 (C) W = nRT ln(V₂/V₁)
🔴 (D) W = 0
Answer: (A) W = nRΔT
Question 5. अदियाबतिक प्रक्रिया के लिए कौन-सा सम्बन्ध सत्य है?
🔵 (A) PV = स्थिर
🟢 (B) PV^γ = स्थिर
🟠 (C) PT = स्थिर
🔴 (D) T/V = स्थिर
Answer: (B) PV^γ = स्थिर
Question 6. ऊष्मागतिकी का प्रथम नियम किस सिद्धान्त पर आधारित है?
🔵 (A) ऊर्जा संरक्षण
🟢 (B) संवेग संरक्षण
🟠 (C) द्रव्यमान संरक्षण
🔴 (D) बल संतुलन
Answer: (A) ऊर्जा संरक्षण
Question 7. ऊष्मागतिकी के प्रथम नियम का गणितीय रूप क्या है?
🔵 (A) ΔQ = ΔW − ΔU
🟢 (B) ΔQ = ΔU + ΔW
🟠 (C) ΔQ = ΔU − ΔW
🔴 (D) ΔW = ΔU + ΔQ
Answer: (B) ΔQ = ΔU + ΔW
Question 8. यदि गैस प्रसारित होती है तो कार्य W का चिन्ह क्या होगा?
🔵 (A) धनात्मक
🟢 (B) ऋणात्मक
🟠 (C) शून्य
🔴 (D) अनंत
Answer: (A) धनात्मक
Question 9. यदि गैस का आयतन नियत रहता है तो किया गया कार्य —
🔵 (A) अधिकतम
🟢 (B) शून्य
🟠 (C) न्यूनतम
🔴 (D) ऋणात्मक
Answer: (B) शून्य
Question 10. नियत आयतन पर विशिष्ट ऊष्मा का प्रतीक क्या है?
🔵 (A) Cₚ
🟢 (B) Cᵥ
🟠 (C) R
🔴 (D) γ
Answer: (B) Cᵥ
Question 11. नियत दाब पर विशिष्ट ऊष्मा का प्रतीक —
🔵 (A) Cᵥ
🟢 (B) Cₚ
🟠 (C) R
🔴 (D) γ
Answer: (B) Cₚ
Question 12. γ का परिभाषा क्या है?
🔵 (A) γ = Cᵥ / Cₚ
🟢 (B) γ = Cₚ / Cᵥ
🟠 (C) γ = R / Cₚ
🔴 (D) γ = Cᵥ / R
Answer: (B) γ = Cₚ / Cᵥ
Question 13. किसी आदर्श गैस के लिए, यदि आयतन दोगुना हो जाए, तो समतापी प्रक्रिया में किया गया कार्य —
🔵 (A) nRT ln2
🟢 (B) nRT
🟠 (C) nRT/2
🔴 (D) 2nRT
Answer: (A) nRT ln2
Question 14. किस प्रक्रिया में ऊष्मा का आदान-प्रदान नहीं होता?
🔵 (A) समदाब
🟢 (B) समतापी
🟠 (C) अदियाबतिक
🔴 (D) समवॉलकीय
Answer: (C) अदियाबतिक
Question 15. कार्नो इंजन की दक्षता का सूत्र —
🔵 (A) η = 1 − (Q₂ / Q₁)
🟢 (B) η = 1 − (T₂ / T₁)
🟠 (C) η = Q₁ / Q₂
🔴 (D) η = T₁ / T₂
Answer: (B) η = 1 − (T₂ / T₁)
Question 16. कार्नो इंजन की दक्षता पर कौन-सा कारक प्रभाव नहीं डालता?
🔵 (A) कार्यकारी पदार्थ
🟢 (B) स्रोत और पात्र का तापमान
🟠 (C) तापान्तर
🔴 (D) T₁ और T₂
Answer: (A) कार्यकारी पदार्थ
Question 17. क्लॉसियस कथन किस नियम से सम्बन्धित है?
🔵 (A) प्रथम नियम
🟢 (B) द्वितीय नियम
🟠 (C) तृतीय नियम
🔴 (D) शून्यवाँ नियम
Answer: (B) द्वितीय नियम
Question 18. एंट्रॉपी में परिवर्तन का सूत्र क्या है?
🔵 (A) ΔS = Q / T
🟢 (B) ΔS = T / Q
🟠 (C) ΔS = Q × T
🔴 (D) ΔS = T² / Q
Answer: (A) ΔS = Q / T
Question 19.
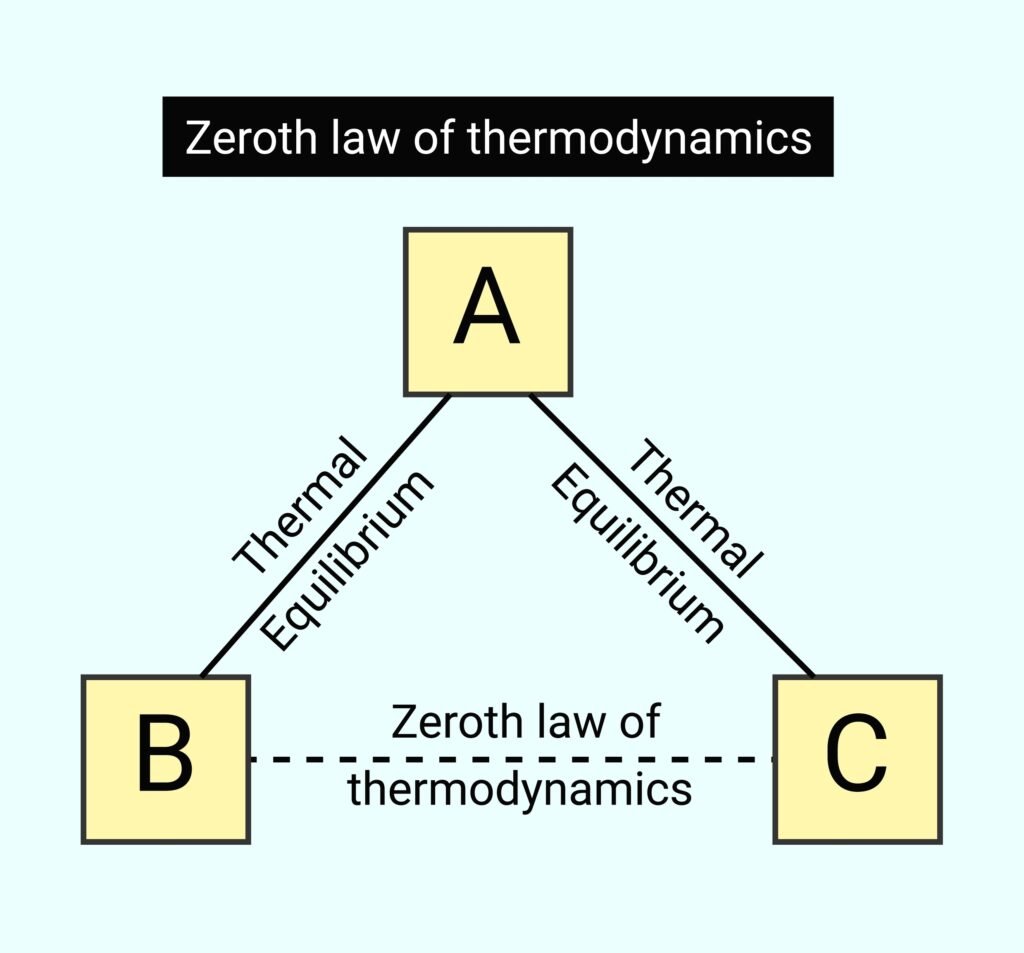
ऊष्मागतिकी के शून्यवाँ नियम (Zeroth Law) को स्पष्ट कीजिए।
Answer:
🔹 यह नियम तापीय संतुलन की अवधारणा को परिभाषित करता है।
✏️ विधान: यदि कोई दो प्रणालियाँ किसी तीसरी प्रणाली के साथ पृथक-पृथक तापीय संतुलन में हों, तो वे दोनों एक-दूसरे के साथ भी तापीय संतुलन में होंगी।
💡 महत्व:
➡️ यह तापमान को परिभाषित करने का आधार प्रदान करता है।
➡️ तापमापी का कार्य इसी नियम पर आधारित है।
Question 20.
ऊष्मागतिकी के प्रथम नियम का कथन कीजिए तथा इसका भौतिक अर्थ बताइए।
Answer:
✏️ विधान:
जब किसी प्रणाली में ऊष्मा ΔQ प्रविष्ट होती है, तो उसका एक भाग प्रणाली की आन्तरिक ऊर्जा ΔU को बढ़ाता है और शेष भाग ΔW प्रणाली द्वारा कार्य के रूप में परिवेश पर किया जाता है।
➡️ गणितीय रूप: ΔQ = ΔU + ΔW
💡 भौतिक अर्थ:
यह नियम ऊर्जा संरक्षण का नियम है — ऊष्मा और कार्य परस्पर रूपान्तरित हो सकते हैं, परन्तु कुल ऊर्जा स्थिर रहती है।
Question 21.
आदर्श गैस के लिए समतापी प्रक्रिया में किया गया कार्य व्युत्पन्न कीजिए।
Answer:
➡️ समतापी प्रक्रिया में तापमान स्थिर रहता है ⇒ ΔT = 0।
P V = n R T ⇒ P = n R T / V
अब किया गया कार्य —
W = ∫ P dV = ∫ (n R T / V) dV = n R T ln(V₂ / V₁)
✔️ निष्कर्ष:
समतापी प्रक्रिया में किया गया कार्य
W = n R T ln(V₂ / V₁)
Question 22.
अदियाबतिक प्रक्रिया में कार्य का व्यंजक लिखिए।
Answer:
अदियाबतिक प्रक्रिया के लिए Q = 0 होता है।
प्रथम नियम के अनुसार —
ΔQ = ΔU + ΔW ⇒ 0 = ΔU + ΔW ⇒ ΔW = −ΔU
आदर्श गैस के लिए ΔU = n Cᵥ (T₂ − T₁)
अतः किया गया कार्य —
W = n Cᵥ (T₁ − T₂)
✔️ निष्कर्ष:
अदियाबतिक प्रसार में (T₂ < T₁) ⇒ W धनात्मक,
अदियाबतिक संपीड़न में (T₂ > T₁) ⇒ W ऋणात्मक।
Question 23.
Cₚ और Cᵥ के बीच सम्बन्ध सिद्ध कीजिए।
Answer:
ऊष्मागतिकी के प्रथम नियम के अनुसार —
ΔQ = ΔU + P ΔV
आदर्श गैस के लिए P V = n R T ⇒ ΔV = (n R ΔT)/P
समदाब प्रक्रिया में:
ΔQ = n Cₚ ΔT = n Cᵥ ΔT + P ΔV
अब, P ΔV = n R ΔT
अतः
n Cₚ ΔT = n Cᵥ ΔT + n R ΔT
⇒ Cₚ − Cᵥ = R
✔️ यह आदर्श गैसों का मूल सम्बन्ध है।
Question 24.
ऊष्मागतिकी के द्वितीय नियम का क्लॉसियस और केल्विन-प्लांक रूप में कथन कीजिए।
Answer:
🔹 क्लॉसियस कथन:
ऊष्मा स्वतः ठण्डे पिण्ड से गरम पिण्ड में नहीं जा सकती।
🔹 केल्विन-प्लांक कथन:
कोई इंजन ऐसा नहीं बनाया जा सकता जो किसी एक स्रोत से ऊष्मा ग्रहण करके उसका सम्पूर्ण भाग कार्य में परिवर्तित कर दे।
✔️ दोनों कथन समान हैं और ऊर्जा परिवर्तन की दिशा को दर्शाते हैं।
Question 25.
कार्नो इंजन की दक्षता का सूत्र सिद्ध कीजिए।
Answer:
कार्नो इंजन दो समतापी और दो अदियाबतिक प्रक्रियाओं से कार्य करता है।
यदि स्रोत से ली गई ऊष्मा Q₁ और पात्र को दी गई ऊष्मा Q₂ हो, तो —
दक्षता (η) = W / Q₁ = 1 − (Q₂ / Q₁)
समतापी प्रक्रियाओं से:
Q₁ / Q₂ = T₁ / T₂
अतः
η = 1 − (T₂ / T₁)
✔️ यह अधिकतम सम्भव दक्षता का व्यंजक है।
Question 26.
एंट्रॉपी (Entropy) का भौतिक अर्थ क्या है?
Answer:
एंट्रॉपी किसी प्रणाली की अव्यवस्था की मात्रा का माप है।
यह बताती है कि किसी प्रक्रिया में ऊर्जा किस दिशा में प्रवाहित होगी।
समतापी प्रक्रिया के लिए —
ΔS = Q / T
➡️ यदि ΔS = 0 ⇒ प्रत्यावर्ती प्रक्रिया
➡️ यदि ΔS > 0 ⇒ अप्रत्यावर्ती प्रक्रिया
✔️ एंट्रॉपी सदैव बढ़ती है; यह प्रकृति की स्वाभाविक दिशा को निर्धारित करती है।
Question 27.
ऊष्मागतिक संतुलन की अवस्था समझाइए।
Answer:
जब प्रणाली में कोई स्वतः परिवर्तन नहीं हो रहा हो, तब वह ऊष्मागतिक संतुलन में होती है।
इसमें तीन प्रकार के संतुलन सम्मिलित होते हैं —
🔹 तापीय संतुलन
🔹 यांत्रिक संतुलन
🔹 रासायनिक संतुलन
✔️ यदि तीनों संतुलन एक साथ विद्यमान हों, तो प्रणाली पूर्ण ऊष्मागतिक संतुलन में कही जाती है।
(दीर्घ एवं केस आधारित प्रश्न)
Question 28.
ऊष्मागतिकी के प्रथम नियम (ΔQ = ΔU + ΔW) को एक गैस के समतापी प्रसार पर लागू करके समझाइए।
Answer:
🔹 समतापी प्रक्रिया में तापमान स्थिर रहता है अर्थात् ΔT = 0।
तापमान न बदलने से गैस की आन्तरिक ऊर्जा (ΔU) भी स्थिर रहती है, अतः ΔU = 0।
✏️ ऊष्मागतिकी का प्रथम नियम:
ΔQ = ΔU + ΔW
अब, ΔU = 0 ⇒ ΔQ = ΔW
➡️ इसका अर्थ है कि गैस द्वारा किया गया कार्य उसी ऊष्मा के बराबर होता है जो उसे दी जाती है।
💡 उदाहरण:
जब गैस को धीरे-धीरे गर्म किया जाता है तो वह फैलती है और बाह्य दाब के विरुद्ध कार्य करती है।
इस स्थिति में सारी ऊष्मा कार्य में परिवर्तित हो जाती है, आन्तरिक ऊर्जा नहीं बदलती।
✔️ निष्कर्ष:
समतापी प्रक्रिया में Q = W तथा ΔU = 0 होता है।
Question 29.
अदियाबतिक प्रक्रिया में दाब और आयतन के बीच सम्बन्ध सिद्ध कीजिए।
Answer:
अदियाबतिक प्रक्रिया में ऊष्मा का आदान-प्रदान नहीं होता, अतः Q = 0।
प्रथम नियम के अनुसार:
ΔQ = ΔU + ΔW ⇒ 0 = ΔU + ΔW ⇒ ΔU = −ΔW
आदर्श गैस के लिए —
ΔU = n Cᵥ (T₂ − T₁) और ΔW = ∫ P dV
अब, P V = n R T ⇒ T = (P V) / (n R)
इन दोनों को जोड़ने पर और ΔU = −ΔW रखने पर मिलता है:
P V^γ = स्थिर, जहाँ γ = Cₚ / Cᵥ
💡 निष्कर्ष:
अदियाबतिक प्रक्रिया में दाब और आयतन का गुणनफल किसी नियत घात (γ) के साथ स्थिर रहता है।
Question 30.
कार्नो इंजन की कार्य प्रणाली का वर्णन कीजिए और दक्षता का व्यंजक व्युत्पन्न कीजिए।
Answer:
🌿 कार्नो इंजन की चार अवस्थाएँ:
1️⃣ समतापी प्रसार (A → B): गैस T₁ ताप पर Q₁ ऊष्मा ग्रहण करती है।
2️⃣ अदियाबतिक प्रसार (B → C): गैस T₁ से T₂ ताप तक फैलती है।
3️⃣ समतापी संपीड़न (C → D): गैस T₂ ताप पर Q₂ ऊष्मा पात्र को देती है।
4️⃣ अदियाबतिक संपीड़न (D → A): गैस पुनः प्रारम्भिक अवस्था में लौटती है।
✏️ कुल कार्य:
W = Q₁ − Q₂
दक्षता (η):
η = W / Q₁ = 1 − (Q₂ / Q₁)
समतापी अवस्था में Q₁ / Q₂ = T₁ / T₂
अतः
η = 1 − (T₂ / T₁)
✔️ निष्कर्ष:
कार्नो इंजन की दक्षता केवल तापमानों पर निर्भर करती है, कार्यकारी पदार्थ पर नहीं।
Question 31.
एंट्रॉपी (Entropy) का सिद्धान्त समझाइए तथा अप्रत्यावर्ती प्रक्रियाओं में एंट्रॉपी का व्यवहार स्पष्ट कीजिए।
Answer:
🔹 एंट्रॉपी किसी प्रणाली की अव्यवस्था का माप है।
🔹 किसी समतापी प्रक्रिया के लिए — ΔS = Q / T
➡️ प्रत्यावर्ती प्रक्रिया में ΔS = 0
➡️ अप्रत्यावर्ती प्रक्रिया में ΔS > 0
💡 भौतिक अर्थ:
अप्रत्यावर्ती प्रक्रिया में ऊर्जा का अपव्यय होता है, जिससे प्रणाली की एंट्रॉपी बढ़ती है।
प्रकृति में सभी प्रक्रियाएँ ऐसी दिशा में चलती हैं जिससे कुल एंट्रॉपी बढ़े।
✔️ निष्कर्ष:
एंट्रॉपी वृद्धि का सिद्धान्त प्रकृति की दिशा को निर्धारित करता है — यह बताता है कि ऊष्मा स्वतः ठण्डे से गरम पिण्ड में नहीं जाएगी।
Question 32.
द्वितीय नियम के आधार पर यह सिद्ध कीजिए कि कोई भी इंजन 100% दक्ष नहीं हो सकता।
Answer:
द्वितीय नियम के अनुसार —
“कोई भी इंजन ऐसा नहीं बनाया जा सकता जो किसी एक ऊष्मा स्रोत से ऊष्मा ग्रहण करके उसे पूर्ण रूप से कार्य में बदल दे।”
✏️ कारण:
हर इंजन को कुछ ऊष्मा Q₂ को निम्न ताप पात्र में छोड़ना ही पड़ता है।
η = 1 − (Q₂ / Q₁)
यहाँ Q₂ > 0, अतः η सदैव 1 से कम होगी।
✔️ निष्कर्ष:
कोई भी वास्तविक इंजन 100% दक्ष नहीं हो सकता क्योंकि कुछ ऊष्मा अनिवार्य रूप से पात्र में चली जाती है।
Question 33.
केस आधारित प्रश्न — एक गैस से भरे बेलन में गतिशील पिस्टन लगा है। गैस को धीरे-धीरे गर्म किया जाता है जिससे वह समदाब प्रक्रिया में 2 L से 4 L तक फैलती है।
यदि दाब 2×10⁵ Pa है, तो गैस द्वारा किया गया कार्य ज्ञात कीजिए।
Answer:
✏️ दिए गए आँकड़े:
P = 2×10⁵ Pa
V₁ = 2 L = 2×10⁻³ m³
V₂ = 4 L = 4×10⁻³ m³
➡️ सूत्र:
W = P (V₂ − V₁)
= 2×10⁵ × (4×10⁻³ − 2×10⁻³)
= 2×10⁵ × 2×10⁻³
= 400 J
✔️ निष्कर्ष:
गैस द्वारा किया गया कार्य W = 400 J है।
Question 28.
ऊष्मागतिकी के प्रथम नियम (ΔQ = ΔU + ΔW) को समदाब प्रक्रिया (Isobaric Process) पर लागू करके समझाइए।
Answer:
🔹 समदाब प्रक्रिया में दाब (P) स्थिर रहता है।
🔹 गैस को दी गई ऊष्मा का एक भाग आन्तरिक ऊर्जा बढ़ाने में तथा शेष भाग बाह्य कार्य में प्रयुक्त होता है।
✏️ प्रथम नियम:
ΔQ = ΔU + ΔW
अब, ΔW = P ΔV
और ΔU = n Cᵥ ΔT
अतः
ΔQ = n Cᵥ ΔT + P ΔV
आदर्श गैस समीकरण से — P ΔV = n R ΔT
अतः
ΔQ = n (Cᵥ + R) ΔT
परंतु, Cₚ = Cᵥ + R
अतः
ΔQ = n Cₚ ΔT
💡 निष्कर्ष:
समदाब प्रक्रिया में प्रणाली को दी गई ऊष्मा प्रणाली की आन्तरिक ऊर्जा को बढ़ाती है और कार्य करने में भी प्रयुक्त होती है।
Question 29.
अदियाबतिक प्रक्रिया के लिए P, V और T के बीच सम्बन्ध सिद्ध कीजिए।
Answer:
अदियाबतिक प्रक्रिया में Q = 0 होता है।
ऊष्मागतिकी के प्रथम नियम के अनुसार:
ΔQ = ΔU + ΔW ⇒ 0 = ΔU + ΔW ⇒ ΔU = −ΔW
अब, ΔU = n Cᵥ (T₂ − T₁),
और कार्य W = ∫ P dV।
P V = n R T ⇒ T = P V / (n R)
गणना करने पर प्राप्त होता है —
P V^γ = स्थिर
जहाँ γ = Cₚ / Cᵥ
इसी से आगे —
T V^(γ−1) = स्थिर तथा T P^((1−γ)/γ) = स्थिर
✔️ निष्कर्ष:
अदियाबतिक प्रक्रिया में तीनों राशियों के बीच यह पारस्परिक सम्बन्ध सदैव सत्य रहता है।
Question 30.
कार्नो चक्र की व्याख्या कीजिए तथा इसकी दक्षता का व्यंजक सिद्ध कीजिए।
Answer:
कार्नो इंजन ऊष्मा को कार्य में परिवर्तित करने की आदर्श प्रणाली है।
यह चार प्रत्यावर्ती अवस्थाओं पर आधारित है —
🌿 (i) समतापी प्रसार (A → B): गैस स्रोत (T₁) से ऊष्मा Q₁ ग्रहण करती है।
🌿 (ii) अदियाबतिक प्रसार (B → C): गैस तापमान T₁ से T₂ तक फैलती है।
🌿 (iii) समतापी संपीड़न (C → D): गैस Q₂ ऊष्मा पात्र (T₂) को छोड़ती है।
🌿 (iv) अदियाबतिक संपीड़न (D → A): गैस पुनः प्रारम्भिक अवस्था में लौटती है।
✏️ दक्षता का व्यंजक:
η = (Q₁ − Q₂) / Q₁ = 1 − (Q₂ / Q₁)
समतापी प्रक्रियाओं में Q₁ / Q₂ = T₁ / T₂
अतः
η = 1 − (T₂ / T₁)
✔️ निष्कर्ष:
कार्नो इंजन की दक्षता केवल तापमानों पर निर्भर करती है, कार्यकारी पदार्थ पर नहीं।
Question 31.
एंट्रॉपी (Entropy) का नियम स्पष्ट कीजिए तथा इसका भौतिक अर्थ बताइए।
Answer:
🔹 एंट्रॉपी किसी प्रणाली की अव्यवस्था की मात्रा का माप है।
🔹 किसी समतापी प्रत्यावर्ती प्रक्रिया के लिए — ΔS = Q / T
➡️ यदि ΔS = 0 → प्रक्रिया प्रत्यावर्ती है।
➡️ यदि ΔS > 0 → प्रक्रिया अप्रत्यावर्ती है।
💡 भौतिक अर्थ:
प्रत्येक वास्तविक प्रक्रिया में कुछ ऊर्जा का अपव्यय होता है।
अतः प्रकृति में एंट्रॉपी सदैव बढ़ती है, जो प्रणाली की अव्यवस्था को दर्शाती है।
✔️ निष्कर्ष:
एंट्रॉपी वृद्धि का सिद्धान्त यह बताता है कि ऊर्जा का प्रवाह सदैव उच्च ताप से निम्न ताप की दिशा में होता है।
Question 32.
द्वितीय नियम के आधार पर सिद्ध कीजिए कि कोई भी इंजन 100% दक्ष नहीं हो सकता।
Answer:
🔹 द्वितीय नियम के केल्विन-प्लांक कथन के अनुसार —
“ऐसा कोई इंजन नहीं बनाया जा सकता जो किसी एक स्रोत से ऊष्मा ग्रहण करके उसकी सम्पूर्ण मात्रा को कार्य में परिवर्तित कर दे।”
✏️ गणितीय रूप:
η = 1 − (Q₂ / Q₁)
यहाँ Q₂ > 0 है, अतः (Q₂ / Q₁) धनात्मक होगा।
इसलिए η < 1
💡 निष्कर्ष:
प्रत्येक इंजन को कुछ ऊष्मा पात्र में छोड़नी ही पड़ती है, अतः कोई इंजन 100% दक्ष नहीं हो सकता।
Question 33.
केस आधारित प्रश्न —
एक गैस से भरे सिलेंडर में गतिशील पिस्टन लगा है। यदि गैस समवॉलकीय प्रक्रिया में 300 K से 600 K तक गरम की जाती है, दाब 2×10⁵ Pa है, तो गैस को दी गई ऊष्मा ज्ञात कीजिए।
(मान लें n = 1 mol, Cᵥ = 3R/2, R = 8.3 J/mol·K)
Answer:
✏️ दिए गए आँकड़े:
P = 2×10⁵ Pa
T₁ = 300 K, T₂ = 600 K
n = 1 mol, Cᵥ = 3R/2
➡️ सूत्र:
Q = n Cᵥ (T₂ − T₁)
= 1 × (3×8.3/2) × (600 − 300)
= (12.45) × 300
= 3735 J
💡 निष्कर्ष:
समवॉलकीय प्रक्रिया में गैस को दी गई ऊष्मा Q = 3.74 × 10³ J है।
————————————————————————————————————————————————————————————————————————————
