Class 11 : Chemistry (In Hindi) – Lesson 9. हाइड्रोकार्बन
पाठ का विश्लेषण एवं विवेचन
🔵 भूमिका ✨
हाइड्रोकार्बन वे यौगिक हैं जो केवल कार्बन और हाइड्रोजन परमाणुओं से बने होते हैं। ये कार्बनिक रसायन का आधार हैं और प्राकृतिक गैस, पेट्रोलियम, कोयला इत्यादि में व्यापक रूप से पाए जाते हैं। इनका अध्ययन अत्यंत महत्त्वपूर्ण है क्योंकि इनसे न केवल ऊर्जा (ईंधन) प्राप्त होती है बल्कि प्लास्टिक, दवा, रंग, विस्फोटक और अन्य कार्बनिक यौगिकों का निर्माण भी किया जाता है।
🟢 हाइड्रोकार्बनों का वर्गीकरण 📌
संतृप्त हाइड्रोकार्बन (Alkanes):
केवल एकल सहसंयोजक बन्ध (C–C)।
सामान्य सूत्र: CnH2n+2
उदाहरण: मीथेन (CH₄), एथेन (C₂H₆), प्रोपेन (C₃H₈)।
असंतृप्त हाइड्रोकार्बन:
(i) अल्कीन्स (Alkenes) → C=C द्वि-बन्ध वाले; सामान्य सूत्र: CnH2n
(ii) अल्काइन्स (Alkynes) → C≡C त्रि-बन्ध वाले; सामान्य सूत्र: CnH2n−2
सुगन्धित हाइड्रोकार्बन (Aromatic):
बेंजीन और उसके व्युत्पन्न।
विशेष स्थिरता: π-इलेक्ट्रॉनों का विस्थापन (resonance)।
हकल नियम (Hückel’s Rule): 4n+2 π-इलेक्ट्रॉन होने पर सुगन्धिता।
🟡 अल्केन (Alkanes) 📘
भौतिक गुण:
रंगहीन, गन्धहीन, जल में अघुलनशील, घनत्व जल से कम।
उबलने व गलने बिन्दु अणु भार बढ़ने पर बढ़ते हैं।
रासायनिक गुण:
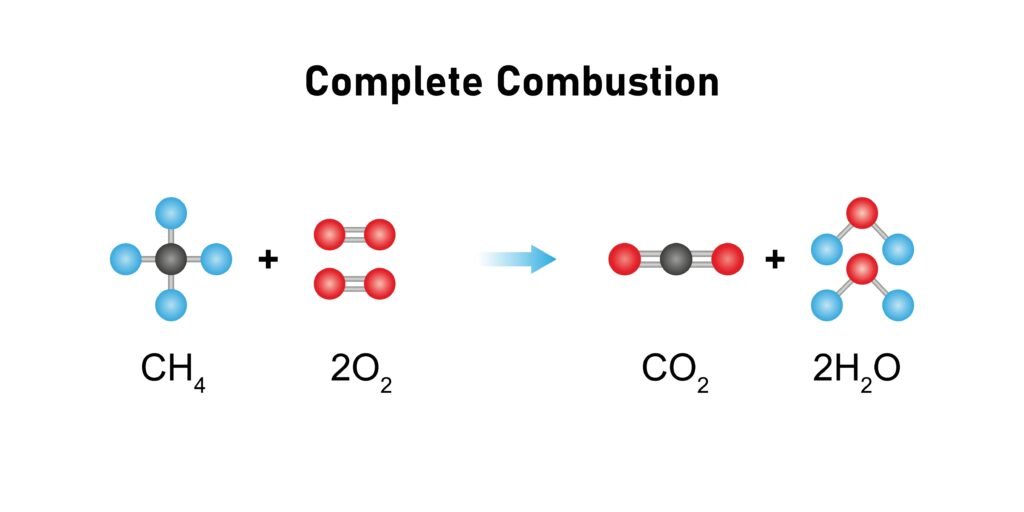
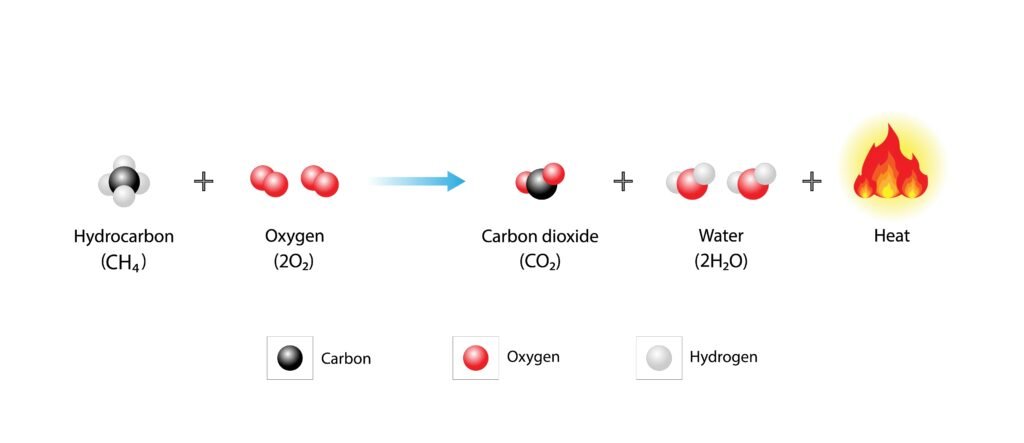
दहन: CH₄ + 2O₂ → CO₂ + 2H₂O (ऊष्माक्षेपी)।
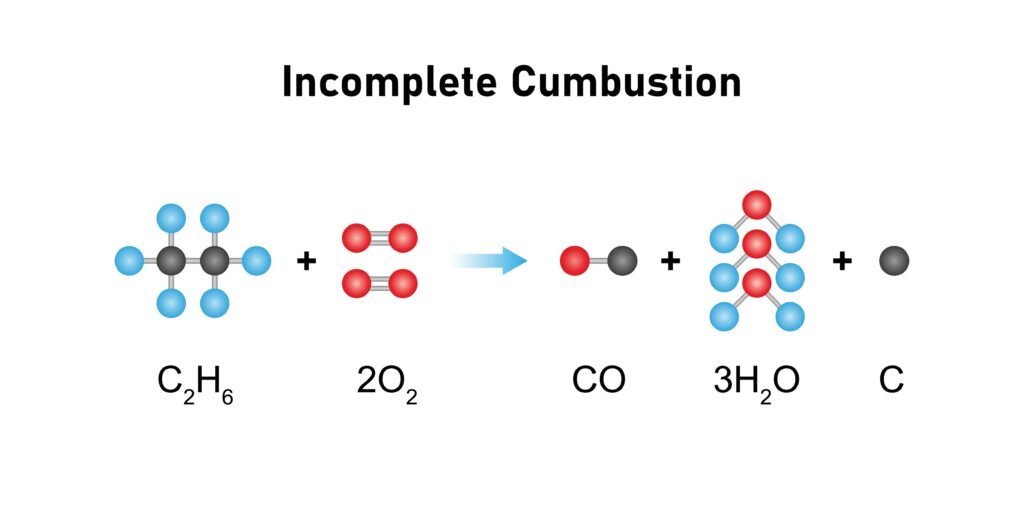
अपूर्ण दहन से CO या कालिख बनती है।
प्रतिस्थापन अभिक्रिया (हैलोजनीकरण): CH₄ + Cl₂ → CH₃Cl + HCl (प्रकाश में)।
संश्लेषण विधियाँ:
वुर्ट्ज अभिक्रिया: 2R–Cl + 2Na → R–R + 2NaCl
कोरी अभिक्रिया: R–COONa + NaOH → R–H + Na₂CO₃
🔴 अल्कीन्स (Alkenes) 🌟
भौतिक गुण:
गैस/तरल, जल में अघुलनशील, घनत्व कम।
रासायनिक गुण:
संयोजन अभिक्रिया:
➤ हाइड्रोजन: CH₂=CH₂ + H₂ → CH₃–CH₃ (उत्प्रेरक Ni पर)।
➤ हैलोजन: CH₂=CH₂ + Br₂ → CH₂Br–CH₂Br (वर्णहीनता से जाँच)।
➤ HCl/HBr का संयोजन (मार्कोवनीकोव नियम):
CH₃–CH=CH₂ + HBr → CH₃–CHBr–CH₃
ऑक्सीकरण:
➤ ठण्डे KMnO₄ से डाइऑल: CH₂=CH₂ → HO–CH₂–CH₂–OH
➤ ओज़ोनोलिसिस: CH₂=CH₂ + O₃ → CH₂O + CH₂O
संश्लेषण विधियाँ:
अल्कोहल का निर्जलीकरण: CH₃–CH₂–OH → CH₂=CH₂ + H₂O (H₂SO₄ द्वारा)।
🟢 अल्काइन्स (Alkynes) 📌
भौतिक गुण:
प्रथम सदस्य एसीटिलीन (C₂H₂) गैस है।
जल में अघुलनशील।
रासायनिक गुण:
संयोजन अभिक्रिया:
➤ H₂ का दो बार जुड़ना → अल्केन।
➤ Br₂ का जुड़ना → डिब्रोमो व टेट्राब्रोमो उत्पाद।
अम्लीय प्रकृति:
CH≡CH + Na → HC≡C⁻ Na⁺ + ½H₂
(टर्मिनल अल्काइन्स में H अम्लीय)।
ऑक्सीकरण:
KMnO₄ या O₃ से अपघटन → कार्बोक्सिलिक अम्ल।
संश्लेषण विधियाँ:
CaC₂ + 2H₂O → C₂H₂ + Ca(OH)₂
🟡 सुगन्धित हाइड्रोकार्बन (Aromatic Hydrocarbons) 🌟
बेंजीन की संरचना:
C₆H₆, षट्कोणीय चक्रीय, 3 द्वि-बन्ध और 3 एकल-बन्ध का रेज़ोनेंस मिश्रण।
सभी C–C बन्ध समान (140 pm)।
गुणधर्म:
दहन पर कालिख उत्पन्न।
अभिक्रियाएँ मुख्यतः विद्युत-आकर्षी प्रतिस्थापन (Electrophilic substitution):
➤ नाइट्रेशन: C₆H₆ + HNO₃ → C₆H₅NO₂
➤ सल्फोनेशन: C₆H₆ + SO₃ → C₆H₅SO₃H
➤ हैलोजनीकरण: C₆H₆ + Cl₂ → C₆H₅Cl
हकल नियम (Hückel’s Rule):
4n+2 π-इलेक्ट्रॉन वाली चक्रीय, समतल प्रणाली सुगन्धित होगी।
बेंजीन (6 π-इलेक्ट्रॉन) सुगन्धित है।
🔴 उपयोग व महत्व 💡
ईंधन: मीथेन, प्रोपेन, ब्यूटेन (LPG, CNG)।
औद्योगिक: बेंजीन, टोल्यून, नेफ्थलीन।
औषधि, कीटनाशक, रबर, प्लास्टिक।
ऊर्जा स्रोत: पेट्रोल, डीज़ल।
🔹 II. पाठ सार
🔵 सार-तत्त्व ✨
हाइड्रोकार्बन केवल C और H से बने होते हैं।
मुख्य प्रकार:
– अल्केन (CnH2n+2, एकल बन्ध) → दहन, प्रतिस्थापन।
– अल्कीन (CnH2n, द्वि-बन्ध) → संयोजन, ऑक्सीकरण।
– अल्काइन (CnH2n−2, त्रि-बन्ध) → संयोजन, अम्लीय प्रकृति।
– सुगन्धित (C₆H₆ व व्युत्पन्न) → प्रतिस्थापन अभिक्रियाएँ।
अल्केन निष्क्रिय, अल्कीन व अल्काइन प्रतिक्रियाशील।
बेंजीन विशेष स्थिरता रेज़ोनेंस से।
हकल नियम: 4n+2 π-इलेक्ट्रॉन सुगन्धिता का आधार।
प्रयोग: ईंधन, औद्योगिक कच्चा माल, औषधि, प्लास्टिक, रंग।
🟢 निष्कर्ष 📌
हाइड्रोकार्बन ऊर्जा और रासायनिक उद्योग का आधार हैं। इनके अभिक्रियात्मक गुण और संरचना आगे कार्बनिक रसायन समझने के लिए आधार तैयार करते हैं।
🔹 III. त्वरित पुनरावृत्ति
🔵 मुख्य बिन्दु 🌟
हाइड्रोकार्बन = C और H यौगिक।
अल्केन: CnH2n+2, एकल बन्ध, प्रतिस्थापन।
अल्कीन: CnH2n, द्वि-बन्ध, संयोजन व ऑक्सीकरण।
अल्काइन: CnH2n−2, त्रि-बन्ध, संयोजन व अम्लीय प्रकृति।
सुगन्धित: बेंजीन व व्युत्पन्न, रेज़ोनेंस व प्रतिस्थापन।
हकल नियम: 4n+2 π-इलेक्ट्रॉन = सुगन्धिता।
उपयोग: ईंधन, औषधि, औद्योगिक कच्चा माल।
————————————————————————————————————————————————————————————————————————————
पाठ्यपुस्त के प्रश्न
🔵 प्रश्न 9.1:
मीथेन के क्लोरीनीकरण के दौरान ऐल्केन कैसे बनती है? आप इसे कैसे समझाएँगे?
🟢 उत्तर:
✏ मीथेन का क्लोरीनीकरण एक श्रृंखला-अभिक्रिया (chain reaction) है, जो तीन चरणों में होती है—
1️⃣ आरंभ (Initiation):
क्लोरीन अणु पर प्रकाश या ऊष्मा डालने से यह मुक्त मूलक (Cl•) में टूट जाता है।
→ Cl₂ → 2Cl•
2️⃣ विकास (Propagation):
Cl• मीथेन से एक हाइड्रोजन हटाता है → CH₃• बनता है।
→ CH₄ + Cl• → CH₃• + HCl
अब CH₃• दूसरा Cl₂ से अभिक्रिया करता है → CH₃Cl बनता है।
→ CH₃• + Cl₂ → CH₃Cl + Cl•
3️⃣ समापन (Termination):
मुक्त मूलक आपस में जुड़कर स्थिर अणु बनाते हैं।
→ Cl• + Cl• → Cl₂
→ CH₃• + Cl• → CH₃Cl
✔ इस प्रकार CH₃Cl, CH₂Cl₂, CHCl₃, CCl₄ बनते हैं।
इसे मुक्त मूलक अभिक्रिया (free radical mechanism) कहा जाता है।
🔵 प्रश्न 9.2
निम्नलिखित यौगिकों के IUPAC नाम लिखिए —
(क) CH₃CH = C(CH₃)₂
🟢 उत्तर:
✳ पहचान: सबसे लंबी श्रृंखला में 3 कार्बन परमाणु व एक द्विबन्ध है।
💡 संरचना विश्लेषण:
CH₃–CH=C(CH₃)₂
इसमें एक मिथाइल उपस्थापक तीसरे कार्बन पर जुड़ा है।
✔ IUPAC नाम: 3-मिथाइल-2-ब्यूटीन (3-Methyl-2-butene)
(ख) CH₂ = CH–C≡C–CH₃
🟢 उत्तर:
✳ पहचान: श्रृंखला में 5 कार्बन परमाणु, एक द्विबन्ध और एक त्रिबन्ध दोनों हैं।
💡 क्रमांकन: द्विबन्ध को न्यूनतम संख्या देना प्राथमिक होता है।
✔ IUPAC नाम: पेंटा-1-इन-3-आइन (Penta-1-en-3-yne)
(ग)
संरचना:
🟢 उत्तर:
✳ पहचान: 4 कार्बन व दो द्विबन्ध।
💡 संरचना: CH₂=CH–CH=CH₂
✔ IUPAC नाम: ब्यूटा-1,3-डाइइन (Buta-1,3-diene)
(घ)
संरचना:
साइक्लोहेक्सीन रिंग से –CH₂–CH=CH₂ जुड़ा है।
🟢 उत्तर:
✳ विश्लेषण: मुख्य श्रृंखला साइक्लोहेक्सीन है, उपस्थापक एलील (–CH₂–CH=CH₂)।
✔ IUPAC नाम: 1-(प्रोप-2-एनिल)साइक्लोहेक्सीन (1-(prop-2-enyl)cyclohexene)
(अन्य स्वीकृत नाम: एलिलसाइक्लोहेक्सीन)
(ङ)
संरचना: CH₃(CH₂)₄CH(CH₂CH(CH₃)₂)CH₂CH(CH₃)₂
🟢 उत्तर:
✳ पहचान: यह अत्यधिक शाखित दीर्घ श्रृंखला है।
💡 लंबी श्रृंखला में 9 कार्बन हैं → नॉनान (Nonane)
मुख्य उपस्थापक: दो आइसोप्रोपिल और एक मिथाइल।
✔ IUPAC नाम: 4,5-डाइआइसोप्रोपिल-3-मिथाइलनॉनान (4,5-diisopropyl-3-methylnonane)
(च)
संरचना:
CH₃–CH=CH–CH₂–CH=CH–CH₂–CH=CH₂
🟢 उत्तर:
✳ पहचान: 9 कार्बन और तीन द्विबन्ध।
💡 क्रमांकन: सबसे बाएँ से → C1, C3, C6 पर डबल बॉन्ड।
✔ IUPAC नाम: नॉना-1,3,6-ट्राइइन (Nona-1,3,6-triene)
✅ सारांश तालिका
क्रमांक
संरचना
IUPAC नाम
(क)
CH₃CH=C(CH₃)₂
3-मिथाइल-2-ब्यूटीन
(ख)
CH₂=CH–C≡C–CH₃
पेंटा-1-इन-3-आइन
(ग)
CH₂=CH–CH=CH₂
ब्यूटा-1,3-डाइइन
(घ)
साइक्लोहेक्सीन–CH₂–CH=CH₂
1-(प्रोप-2-एनिल)साइक्लोहेक्सीन
(ङ)
शाखित नॉनान संरचना
4,5-डाइआइसोप्रोपिल-3-मिथाइलनॉनान
(च)
CH₃CH=CHCH₂CH=CHCH₂CH=CH₂
नॉना-1,3,6-ट्राइइन
🔵 प्रश्न 9.3:
निम्नलिखित यौगिकों, जिनमें द्विबंध तथा त्रिबंध दर्शाए गए हैं, के सभी संभावित स्थायी समावयवों के संरचनात्मक सूत्र एवं IUPAC नाम लिखिए—
(क) C₄H₆ (एक द्विबंध)
(ख) C₅H₈ (एक त्रिबंध)
🟢 उत्तर:
(क) C₄H₆ (एक द्विबंध):
1️⃣ ब्यूट-1-ईन-2-आइन
2️⃣ ब्यूट-2-ईन
3️⃣ साइक्लोब्यूटेन
(ख) C₅H₈ (एक त्रिबंध):
1️⃣ पेंट-1-आइन
2️⃣ पेंट-2-आइन
3️⃣ मिथाइलब्यूट-1-आइन
4️⃣ साइक्लोपेंटीन
🔵 प्रश्न 9.4:
निम्नलिखित यौगिकों के ओजोनोलाइसिस के परिणाम बताइए—
(i) पेंट-2-ईन
(ii) 3,4-डाईमेथाइलहेक्स-3-ईन
(iii) 2-एथाइलहेक्स-2-ईन
(iv) 1-फेनाइलहेप्ट-1-ईन
🟢 उत्तर:
✏ ओजोनोलाइसिस में यौगिक का ओजोनाइड बनता है जो अपचयन द्वारा एल्डिहाइड या कीटोन देता है।
(i) पेंट-2-ईन → 2 अणु प्रोपेनोन (CH₃COCH₃)
(ii) 3,4-डाईमेथाइलहेक्स-3-ईन → 2 अणु 2,3-डाईमेथाइलप्रोपेनोन
(iii) 2-एथाइलहेक्स-2-ईन → ब्यूटेनोन + पेंटानल
(iv) 1-फेनाइलहेप्ट-1-ईन → बेंज़ाल्डिहाइड + हेक्सानोन
🔵 प्रश्न 9.5:
एक ऐल्कीन ‘A’ के ओजोनोलाइसिस से पेंटेन-3-वन तथा पेंटेन-2-वन प्राप्त होते हैं। A का IUPAC नाम लिखिए।
🟢 उत्तर:
✏ ओजोनोलाइसिस में दो कीटोन मिलने का अर्थ है कि द्विबंध के दोनों छोर समान नहीं हैं।
✴ संयोजन से पता चलता है कि यौगिक है:
3-हेक्सीन (Hex-3-ene)
🔵 प्रश्न 9.6:
एक ऐल्केन A में तीन C–C, आठ C–H बंध हैं तथा एक C–C बंध σ और π दोनों है। A में कुल हाइड्रोजन परमाणु 44 हैं। इसका आणविक सूत्र तथा IUPAC नाम लिखिए।
🟢 उत्तर:
✏ C–C π बंध का अर्थ है कि यौगिक ऐल्कीन है।
कुल 44 H का अर्थ है C₂₂H₄₄
✔ यह C₂₂H₄₄ एक संतृप्त ऐल्केन है —
IUPAC नाम: डोकोसेन (Docosane)
🔵 प्रश्न 9.7:
एक यौगिक, जिसके ओजोनोलाइसिस से प्रोपेनोन तथा पेंटेन-3-वन प्राप्त हो, उसका संरचनात्मक सूत्र क्या है?
🟢 उत्तर:
✏ दो कीटोन मिलने से यौगिक में द्विबंध बीच में है।
✔ संरचना: CH₃–CO–CH=CH–CO–CH₃
IUPAC नाम: हेक्स-3-ईन
🔵 प्रश्न 9.8:
निम्नलिखित हाइड्रोकार्बनों के दहन की रासायनिक अभिक्रिया लिखिए—
(i) ब्यूटेन
(ii) पेंटेन
(iii) हेक्साइन
(iv) टोल्यून
🟢 उत्तर:
(i) ब्यूटेन:
C₄H₁₀ + 6½O₂ → 4CO₂ + 5H₂O
(ii) पेंटेन:
C₅H₁₂ + 8O₂ → 5CO₂ + 6H₂O
(iii) हेक्साइन:
C₆H₁₀ + 8½O₂ → 6CO₂ + 5H₂O
(iv) टोल्यून:
C₇H₈ + 9O₂ → 7CO₂ + 4H₂O
🔵 प्रश्न 9.9:
हेक्स-2-ईन की सममिति (सिस) तथा विषमिति (ट्रांस) संरचनाएँ बनाइए। इनमें से कौन-सी समावयव का क्वथनांक ऊँचा होता है और क्यों?
🟢 उत्तर:
✏ हेक्स-2-ईन का आणविक सूत्र: CH₃–CH=CH–CH₂–CH₂–CH₃
1️⃣ सिस-हेक्स-2-ईन — दोनों CH₃ समूह द्विबंध के एक ही ओर।
2️⃣ ट्रांस-हेक्स-2-ईन — दोनों CH₃ समूह द्विबंध के विपरीत ओर।
✔ क्वथनांक अधिक: सिस-हेक्स-2-ईन का, क्योंकि इसमें अणुओं के बीच आकर्षण बल अधिक होते हैं और यह अधिक ध्रुवीय होता है।
🔵 प्रश्न 9.10:
बेंजीन में तीन द्विबंध होते हैं, फिर भी यह असंतृप्त यौगिक नहीं है, क्यों?
🟢 उत्तर:
✏ बेंजीन में एकल व द्विबंध वैकल्पिक रूप से होते हैं, परंतु प्रतिध्वनि (रेज़ोनेंस) के कारण सभी बंध समान लंबाई के होते हैं।
✴ इसमें π-इलेक्ट्रॉन पूरे चक्र में विस्थापित (delocalized) रहते हैं।
✔ इसलिए बेंजीन सामान्य योग अभिक्रियाएँ नहीं करता और यह अरोमैटिक यौगिक कहलाता है, असंतृप्त नहीं।
🔵 प्रश्न 9.11:
किसी निक्षेप द्वारा उत्प्रेरण करने के लिए आवश्यक शर्तें क्या हैं?
🟢 उत्तर:
✏ उत्प्रेरक की आवश्यक शर्तें:
1️⃣ उत्प्रेरक अभिक्रिया की गति बढ़ाता है।
2️⃣ उत्प्रेरक सक्रियण ऊर्जा घटाता है।
3️⃣ उत्प्रेरक अभिक्रिया के अंत में अपरिवर्तित रहता है।
4️⃣ इसकी मात्रा बहुत कम होती है, पर प्रभाव बड़ा होता है।
➡ यह केवल मार्ग बदलता है, अंतिम उत्पाद वही रहता है।
🔵 प्रश्न 9.12:
इनमें से कौन-से चक्र (रिंग) ऐरोमैटिक नहीं हैं? कारण स्पष्ट कीजिए—
(i) CH₂ (साइक्लोप्रोपीन)
(ii) साइक्लोब्यूटाडाइइन
(iii) साइक्लोऑक्टाटेट्राइन
🟢 उत्तर:
✏ ऐरोमैटिकता की शर्तें:
✔ चक्रीय व समतल होना चाहिए
✔ पूर्ण संयुग्मन होना चाहिए
✔ हकिल नियम: π-इलेक्ट्रॉन = 4n + 2
अब परीक्षण करें —
(i) साइक्लोप्रोपीन → 2π इलेक्ट्रॉन → 4n + 2 (n पूर्णांक नहीं) → ऐरोमैटिक नहीं
(ii) साइक्लोब्यूटाडाइइन → 4π इलेक्ट्रॉन → 4n + 2 नहीं → ऐंटी-ऐरोमैटिक
(iii) साइक्लोऑक्टाटेट्राइन → 8π इलेक्ट्रॉन → 4n + 2 नहीं → ऐंटी-ऐरोमैटिक
✔ अतः तीनों ऐरोमैटिक नहीं हैं।
🔵 प्रश्न 9.13:
बेंजीन को निम्नलिखित यौगिकों में कैसे परिवर्तित करेंगे—
(i) p-नाइट्रोब्रोमोबेंजीन
(ii) m-नाइट्रोब्रोमोबेंजीन
(iii) p-नाइट्रोटोल्यून
(iv) p-ब्रोमोटोल्यून
🟢 उत्तर:
✏ परिवर्तन क्रम —
(i) p-नाइट्रोब्रोमोबेंजीन:
बेंजीन → नाइट्रेशन (HNO₃/H₂SO₄) → नाइट्रोबेंजीन → ब्रोमिनेशन (FeBr₃) → p-नाइट्रोब्रोमोबेंजीन
(ii) m-नाइट्रोब्रोमोबेंजीन:
बेंजीन → ब्रोमिनेशन → ब्रोमोबेंजीन → नाइट्रेशन → m-नाइट्रोब्रोमोबेंजीन
(iii) p-नाइट्रोटोल्यून:
बेंजीन → अल्किलेशन (CH₃Cl, AlCl₃) → टोल्यून → नाइट्रेशन → p-नाइट्रोटोल्यून
(iv) p-ब्रोमोटोल्यून:
बेंजीन → टोल्यून → ब्रोमिनेशन (FeBr₃) → p-ब्रोमोटोल्यून
🔵 प्रश्न 9.14:
ऐल्केन H₃C–CH₂–C–(CH₂)₂–CH₂–CH(CH₃)₂ में 1°, 2°, 3° कार्बन परमाणुओं की पहचान कीजिए तथा प्रत्येक की कुल संख्या बताइए।
🟢 उत्तर:
✏
1️⃣ 1° कार्बन — जो केवल 1 अन्य C से जुड़ा है = 5
2️⃣ 2° कार्बन — जो 2 C से जुड़ा है = 2
3️⃣ 3° कार्बन — जो 3 C से जुड़ा है = 1
✔ अतः 1° = 5, 2° = 2, 3° = 1
🔵 प्रश्न 9.15:
प्रोपीन पर HBr के संयोजन से 2-ब्रोमोप्रोपेन बनता है, जबकि पेरॉक्साइड की उपस्थिति में 1-ब्रोमोप्रोपेन बनता है। दोनों अभिक्रियाओं को रासायनिक समीकरण सहित समझाइए।
🟢 उत्तर:
✏ बिना पेरॉक्साइड (मार्कोवनीकोव नियम):
CH₃–CH=CH₂ + HBr → CH₃–CHBr–CH₃ (2-ब्रोमोप्रोपेन)
✏ पेरॉक्साइड की उपस्थिति में (प्रतिमार्कोवनीकोव):
CH₃–CH=CH₂ + HBr → CH₂Br–CH₂–CH₃ (1-ब्रोमोप्रोपेन)
✔ कारण: पेरॉक्साइड की उपस्थिति में रेडिकल तंत्र सक्रिय होता है।
🔵 प्रश्न 9.16:
1,2-डाइमिथॉक्सीएथेन की संरचना बनाइए और बेंजीन के संयुग्मन की व्याख्या कीजिए।
🟢 उत्तर:
✏ 1,2-डाइमिथॉक्सीएथेन: CH₃O–CH₂–CH₂–OCH₃
✴ बेंजीन में वैकल्पिक द्विबंधों का संयुग्मन (conjugation) होता है, जिसमें π-इलेक्ट्रॉन पूरे चक्र में विस्थापित रहते हैं।
✔ यह प्रतिध्वनि संरचना बेंजीन को स्थायित्व देती है।
🔵 प्रश्न 9.17:
n-ब्यूटेन और आइसोब्यूटेन का भौतिक व्यवहार एवं क्वथनांक की तुलना कीजिए और कारण बताइए।
🟢 उत्तर:
✏ n-ब्यूटेन (सीधी श्रृंखला) में अणुओं के बीच आकर्षण बल अधिक → क्वथनांक अधिक (लगभग 273 K)
✏ आइसोब्यूटेन (शाखित) में सतह क्षेत्र कम → आकर्षण बल कम → क्वथनांक कम (लगभग 261 K)
✔ शाखन बढ़ने पर क्वथनांक घटता है।
🔵 प्रश्न 9.18:
n-हेक्सेन तथा साइक्लोहेक्सेन के रासायनिक व्यवहार की तुलना कीजिए और इस भिन्नता का कारण बताइए।
🟢 उत्तर:
✏ n-हेक्सेन एक ऐल्केन है (खुली श्रृंखला यौगिक), जबकि
✏ साइक्लोहेक्सेन एक चक्रीय ऐल्केन है।
✔ दोनों का सामान्य सूत्र C₆H₁₂ होता है, परंतु
➡ n-हेक्सेन योग-अभिक्रियाएँ नहीं करता, केवल प्रतिस्थापन-अभिक्रियाएँ करता है।
➡ साइक्लोहेक्सेन भी सामान्यतः प्रतिस्थापन-अभिक्रिया करता है, पर उसकी संरचना समतल नहीं होती।
🔹 भिन्नता का कारण: संरचनात्मक अंतर और रिंग तान (ring strain) की उपस्थिति।
🔵 प्रश्न 9.19:
एल्कीन इलेक्ट्रोफिलिक अभिक्रियाएँ करते हैं जबकि एल्केन न्यूक्लियोफिलिक अभिक्रियाएँ नहीं करते, इसका कारण बताइए।
🟢 उत्तर:
✏ एल्कीन में π-बंध उपस्थित होते हैं, जो इलेक्ट्रॉन-समृद्ध क्षेत्र बनाते हैं।
✔ अतः वे इलेक्ट्रोफिलिक अभिकर्मकों को आकर्षित करते हैं।
✏ एल्केन में केवल σ-बंध होते हैं, जो स्थिर होते हैं और इलेक्ट्रॉन-घटित क्षेत्र नहीं बनाते।
➡ अतः वे न्यूक्लियोफिलिक अभिक्रियाएँ नहीं करते।
🔵 प्रश्न 9.20:
आप निम्नलिखित यौगिकों को बेंजीन में कैसे परिवर्तित करेंगे—
(i) एथेन (ii) एथीन (iii) एथाइन
🟢 उत्तर:
✏ (i) एथेन → एथीन (डीहाइड्रोजनेशन) → एथाइन (डीहाइड्रोजनेशन) → बेंजीन (त्रिमेराइजेशन, Ni उत्प्रेरक पर):
3C₂H₂ → C₆H₆ (बेंजीन)
✏ (ii) एथीन → एथाइन → बेंजीन
✏ (iii) एथाइन → बेंजीन
✔ अतः सभी अवस्थाओं में अंतिम चरण त्रिमेराइजेशन द्वारा बेंजीन प्राप्त होता है।
🔵 प्रश्न 9.21:
उन सभी ऐल्कीनों की संरचनाएँ बनाइए, जो हाइड्रोजनीकरण करने पर 2-मीथाइलब्यूटेन देती हैं।
🟢 उत्तर:
✏ 2-मीथाइलब्यूटेन का सूत्र: C₅H₁₂
➡ संभावित ऐल्कीन जिनका हाइड्रोजनीकरण इसे देता है:
1️⃣ 2-मीथाइल-1-ब्यूटीन
2️⃣ 2-मीथाइल-2-ब्यूटीन
✔ दोनों के हाइड्रोजनीकरण पर 2-मीथाइलब्यूटेन प्राप्त होता है।
🔵 प्रश्न 9.22:
निम्नलिखित यौगिकों को उनकी इलेक्ट्रोफिलिक प्रतिस्थापन अभिक्रिया में प्रतिक्रियाशीलता के क्रम में व्यवस्थित कीजिए—
(क) क्लोरोबेंजीन, 2,4-डाइमिथाइलक्लोरोबेंजीन, p-नाइट्रोक्लोरोबेंजीन
🟢 उत्तर:
✏ इलेक्ट्रोफिलिक प्रतिस्थापन की गति पर +I तथा –I समूहों का प्रभाव पड़ता है।
✔ इलेक्ट्रॉन-दाता समूह गति बढ़ाते हैं, इलेक्ट्रॉन-आकर्षी समूह गति घटाते हैं।
➤ क्रम:
2,4-डाइमिथाइलक्लोरोबेंजीन > क्लोरोबेंजीन > p-नाइट्रोक्लोरोबेंजीन
🔵 प्रश्न 9.23:
बेंजीन, p-नाइट्रोबेंजीन तथा टोल्यून में से किसका नाइट्रेशन आसानी से होता है और क्यों?
🟢 उत्तर:
✏ टोल्यून का नाइट्रेशन सबसे आसान है क्योंकि CH₃ समूह इलेक्ट्रॉन-दाता है, जिससे रिंग अधिक प्रतिक्रियाशील होती है।
✔ बेंजीन का नाइट्रेशन सामान्य है।
✏ p-नाइट्रोबेंजीन में –NO₂ समूह इलेक्ट्रॉन-आकर्षी है, जिससे रिंग कम प्रतिक्रियाशील होती है।
➡ क्रम: टोल्यून > बेंजीन > p-नाइट्रोबेंजीन
🔵 प्रश्न 9.24:
बेंजीन के प्रतिस्थापन में केवल इलेक्ट्रोफिलिक अभिक्रियाएँ ही क्यों होती हैं? कोई उदाहरण सहित स्पष्ट कीजिए।
🟢 उत्तर:
✏ बेंजीन में π-इलेक्ट्रॉन विस्थापित होते हैं और यह इलेक्ट्रॉन-घटित अभिकर्मकों को आकर्षित करता है।
✔ अतः इसमें इलेक्ट्रोफिलिक प्रतिस्थापन होता है, योग-अभिक्रिया नहीं क्योंकि योग करने से ऐरोमैटिकता नष्ट हो जाएगी।
उदाहरण:
C₆H₆ + HNO₃ → C₆H₅NO₂ + H₂O (नाइट्रेशन)
🔵 प्रश्न 9.25:
क्या कारण है कि कुछ एल्कीनों में नियम संख्या बताने वाले स्थानांक देने की आवश्यकता नहीं होती? एक उदाहरण देकर स्पष्ट कीजिए।
🟢 उत्तर:
✏ जब केवल एक ही द्विबंध संभव होता है और स्थिति किसी भी दिशा से समान रहती है, तब स्थानांक बताना आवश्यक नहीं।
उदाहरण:
एथीन (CH₂=CH₂) — इसमें द्विबंध का स्थान बदलने पर भी संरचना समान रहती है।
✔ अतः स्थानांक की आवश्यकता नहीं।
————————————————————————————————————————————————————————————————————————————
अन्य महत्वपूर्ण प्रश्न
(CBSE MODEL प्रश्न पत्र)
सिर्फ इसी पाठ से निर्मित CBSE MODEL प्रश्न पत्र।
खंड A — बहुविकल्पीय प्रश्न (Q1–Q16, प्रत्येक 1 अंक)
प्रश्न 1. ऐल्केन का सामान्य सूत्र है:
CₙH₂ₙ₊₂
CₙH₂ₙ
CₙH₂ₙ₋₂
CₙH₂ₙ₊₁
Answer: 1
प्रश्न 2. एथीन का आणविक सूत्र है:
C₂H₂
C₂H₄
C₂H₆
CH₄
Answer: 2
प्रश्न 3. ऐल्काइन में कम से कम एक बन्ध होता है:
एकल
द्वि
त्रि
कोई नहीं
Answer: 3
प्रश्न 4. बेन्ज़ीन में कितने π-इलेक्ट्रॉन होते हैं?
2
4
6
8
Answer: 3
कथन–कारण हेतु विकल्प-कुंजी
कथन (A) एवं कारण (R) दोनों सत्य हैं तथा R, A का सही कारण है
कथन (A) एवं कारण (R) दोनों सत्य हैं परन्तु R, A का सही कारण नहीं
कथन (A) सत्य है परन्तु R असत्य
कथन (A) असत्य है परन्तु R सत्य
प्रश्न 5 (A/R).
कथन (A): ऐल्केन को पैराफिन भी कहते हैं।
कारण (R): ये रासायनिक रूप से बहुत कम क्रियाशील होते हैं।
Answer: 1
प्रश्न 6. मिथेन में C–H बन्ध कोण है:
90°
109.5°
120°
180°
Answer: 2
प्रश्न 7. एथाइन में कार्बन परमाणु किस हाइब्रिडीकरण अवस्था में होते हैं?
sp³
sp²
sp
dsp²
Answer: 3
प्रश्न 8. बेन्ज़ीन में प्रत्येक C–C बन्ध की लम्बाई है:
154 pm
134 pm
120 pm
100 pm
Answer: 2
प्रश्न 9. मिथेन का क्लोरीनीकरण किस प्रकार की अभिक्रिया है?
योग
प्रतिस्थापन
उन्मूलन
पुनर्विन्यास
Answer: 2
प्रश्न 10 (A/R).
कथन (A): एथीन ब्रोमीन जल का वर्ण हटाता है।
कारण (R): इसमें द्वि बन्ध के कारण योग अभिक्रिया होती है।
Answer: 1
प्रश्न 11. ऐल्केन का प्रमुख औद्योगिक स्रोत है:
कोयला
पेट्रोलियम
प्राकृतिक गैस
लकड़ी
Answer: 2
प्रश्न 12. एथीन के दहन में मुख्य उत्पाद हैं:
CO और H₂O
CO₂ और H₂O
CO₂ और H₂
केवल H₂O
Answer: 2
प्रश्न 13. टॉल्यून का आणविक सूत्र है:
C₆H₆
C₆H₅CH₃
C₆H₅OH
C₆H₄Cl₂
Answer: 2
प्रश्न 14. ह्यूमोल (C₆H₅OH) किस वर्ग का यौगिक है?
ऐल्कोहल
फिनॉल
ईथर
ऐल्डिहाइड
Answer: 2
प्रश्न 15 (A/R).
कथन (A): बेन्ज़ीन इलेक्ट्रोफिलिक प्रतिस्थापन अभिक्रियाएँ करता है।
कारण (R): बेन्ज़ीन का π-इलेक्ट्रॉन बादल इलेक्ट्रोफाइल को आकर्षित करता है।
Answer: 1
प्रश्न 16. एथाइन जल के साथ H₂SO₄ व HgSO₄ की उपस्थिति में कौन-सा यौगिक देता है?
एथेनॉल
एथेनल
एथेनोन (ऐसीटोन)
एथेनिक अम्ल
Answer: 4
खंड B — अति लघु उत्तरीय प्रश्न (Q17–Q21, प्रत्येक 2 अंक)
प्रश्न 17. ऐल्केन के दो गुणधर्म लिखिए।
उत्तर:
🟦 संतृप्त हाइड्रोकार्बन होते हैं।
🟩 दहन में CO₂ और H₂O बनाते हैं।
प्रश्न 18. एथीन का औद्योगिक उपयोग लिखिए।
उत्तर:
🟦 पॉलिथीन (प्लास्टिक) बनाने में प्रयुक्त।
🟩 अल्कोहल (एथेनॉल) के संश्लेषण में प्रयुक्त।
प्रश्न 19. ऐल्काइन का एक प्रयोग लिखिए।
उत्तर:
🟦 एथाइन वायु में जलकर तीव्र ऊष्मा उत्पन्न करता है।
🟩 वेल्डिंग में प्रयुक्त।
प्रश्न 20. बेन्ज़ीन की एक विशिष्ट अभिक्रिया लिखिए।
उत्तर:
🟦 नाइट्रेशन: C₆H₆ + HNO₃ → C₆H₅NO₂ + H₂O (H₂SO₄ की उपस्थिति में)।
प्रश्न 21. टॉल्यून का एक उपयोग लिखिए।
उत्तर:
🟦 विस्फोटक TNT (ट्राइनाइट्रोटॉल्यून) बनाने में प्रयुक्त।
खंड C — लघु उत्तरीय प्रश्न (Q22–Q28, प्रत्येक 3 अंक)
प्रश्न 22. ऐल्केन का दहन अभिक्रिया लिखिए।
उत्तर:
🟦 सामान्य सूत्र: CₙH₂ₙ₊₂ + (3n+1)/2 O₂ → nCO₂ + (n+1)H₂O
🟩 उदाहरण: CH₄ + 2O₂ → CO₂ + 2H₂O + ऊष्मा
प्रश्न 23. एथीन का हाइड्रोजनीकरण अभिक्रिया लिखिए।
उत्तर:
🟦 CH₂=CH₂ + H₂ → CH₃–CH₃ (Ni उत्प्रेरक, Δ)।
प्रश्न 24. ऐल्काइन की जल योग अभिक्रिया (H₂SO₄ व HgSO₄ की उपस्थिति में) लिखिए।
उत्तर:
🟦 CH≡CH + H₂O → CH₃–CHO (एथेनल)।
🟩 केटो–एनॉल टॉटोमरी से स्थिर रूप: CH₃–CO–H (एथेनल)।
प्रश्न 25. बेन्ज़ीन का हैलोजनीकरण समझाइए।
उत्तर:
🟦 C₆H₆ + Cl₂ → C₆H₅Cl + HCl (FeCl₃ उत्प्रेरक में)।
🟩 यह इलेक्ट्रोफिलिक प्रतिस्थापन अभिक्रिया है।
प्रश्न 26. बेन्ज़ीन की संरचना में अनुनाद का सिद्धान्त लिखिए।
उत्तर:
🟦 केकुले संरचनाएँ दो विकल्प देती हैं।
🟩 वास्तविक बेन्ज़ीन में सभी C–C बन्ध समान (134 pm)।
🟪 अनुनाद ऊर्जा के कारण बेन्ज़ीन स्थायी होता है।
प्रश्न 27. एथाइन की वेल्डिंग में उपयोगिता क्यों है?
उत्तर:
🟦 एथाइन + O₂ → CO₂ + H₂O + बहुत अधिक ऊष्मा।
🟩 ज्वाला का ताप ~ 3000 °C तक।
🟪 धातुओं की वेल्डिंग में उपयुक्त।
प्रश्न 28. टॉल्यून का नाइट्रेशन अभिक्रिया समीकरण लिखिए।
उत्तर:
🟦 C₆H₅CH₃ + HNO₃ → C₆H₄CH₃NO₂ + H₂O (H₂SO₄ की उपस्थिति में)।
🟩 उत्पाद: नाइट्रोटॉल्यून।
✅ यहाँ तक Q1–Q28 (खंड A–C) पूरे उत्तर सहित प्रस्तुत हैं।
👉 क्या आप चाहेंगे कि मैं अब प्रतिक्रिया 2 (Q29–Q33, खंड D–E, दीर्घ प्रश्न + अन्तरविकल्प) भी बना दूँ?कोड 3 — रसायन विज्ञान (कक्षा 11)
पाठ का नाम: हाइड्रोकार्बन
समय: 3 घंटे अधिकतम अंक: 70
खंड D — प्रकरण आधारित प्रश्न (Q29–Q30, प्रत्येक 4 अंक)
प्रश्न 29.
“एथीन (CH₂=CH₂) ब्रोमीन जल का वर्ण हटाता है।”
(i) यह अभिक्रिया किस प्रकार की है? (1)
(ii) अभिक्रिया का समीकरण लिखिए। (1)
(iii) यह परीक्षण किसके लिए उपयोगी है? (2)
उत्तर:
🟦 (i) यह योग अभिक्रिया है।
🟩 (ii) CH₂=CH₂ + Br₂ → CH₂Br–CH₂Br
🟪 (iii) यह असंतृप्त हाइड्रोकार्बनों (ऐल्कीन, ऐल्काइन) की पहचान हेतु प्रयोग होता है।
प्रश्न 30.
“एथाइन (C₂H₂) का वेल्डिंग में उपयोग किया जाता है।”
(i) एथाइन की दहन अभिक्रिया लिखिए। (1)
(ii) इस ज्वाला का ताप लगभग कितना होता है? (1)
(iii) वेल्डिंग में इसका उपयोग क्यों उपयुक्त है? (2)
उत्तर:
🟦 (i) 2C₂H₂ + 5O₂ → 4CO₂ + 2H₂O + ऊष्मा
🟩 (ii) ताप ~ 3000 °C तक पहुँचता है।
🟪 (iii) उच्च ताप उत्पन्न करने से धातुओं को पिघलाकर जोड़ने में सक्षम ⇒ वेल्डिंग हेतु उपयुक्त।
खंड E — दीर्घ उत्तरीय प्रश्न (Q31–Q33, प्रत्येक 5 अंक)
प्रश्न 31.
ऐल्केन, ऐल्कीन और ऐल्काइन के प्रमुख भेद लिखिए।
उत्तर:
🟦 ऐल्केन:
सामान्य सूत्र CₙH₂ₙ₊₂
केवल एकल बन्ध
उदाहरण: CH₄
🟩 ऐल्कीन:
सामान्य सूत्र CₙH₂ₙ
कम से कम एक द्वि बन्ध
उदाहरण: C₂H₄
🟪 ऐल्काइन:
सामान्य सूत्र CₙH₂ₙ₋₂
कम से कम एक त्रि बन्ध
उदाहरण: C₂H₂
✅ निष्कर्ष: बन्ध प्रकार और सामान्य सूत्र के आधार पर अंतर।
या
ऐल्केन के क्लोरीनीकरण की श्रृंखला अभिक्रिया (आरम्भ, प्रसार, समापन) समझाइए।
प्रश्न 32.
बेन्ज़ीन की इलेक्ट्रोफिलिक प्रतिस्थापन अभिक्रिया का तंत्र (नाइट्रेशन) समझाइए।
उत्तर:
🟦 चरण 1: इलेक्ट्रोफाइल (NO₂⁺) का निर्माण → HNO₃ + H₂SO₄ → NO₂⁺ + HSO₄⁻ + H₂O
🟩 चरण 2: NO₂⁺ बेन्ज़ीन के π-इलेक्ट्रॉन बादल पर आक्रमण करता है।
🟪 चरण 3: कार्बोकैटायनिक मध्यवर्ती बनता है और पुनः स्थिरता हेतु H⁺ हटता है।
✅ अंतिम उत्पाद: नाइट्रोबेन्ज़ीन।
या
बेन्ज़ीन की अनुनाद संरचनाओं को समझाइए और इससे उसकी स्थिरता पर टिप्पणी कीजिए।
प्रश्न 33.
एथीन की योग अभिक्रियाएँ लिखिए और उनका महत्व समझाइए।
उत्तर:
🟦 (i) हाइड्रोजनीकरण: CH₂=CH₂ + H₂ → CH₃–CH₃ (Ni उत्प्रेरक)
🟩 (ii) हैलोजन योग: CH₂=CH₂ + Cl₂ → CH₂Cl–CH₂Cl
🟪 (iii) जल योग: CH₂=CH₂ + H₂O → CH₃–CH₂OH (H₂SO₄ उत्प्रेरक)
✅ महत्व: प्लास्टिक, अल्कोहल, डाईक्लोरोएथेन आदि उद्योगों में आधार।
या
एथाइन की प्रमुख अभिक्रियाएँ (दहन, योग, प्रतिस्थापन) उदाहरण सहित लिखिए।
————————————————————————————————————————————————————————————————————————————
