Class 10 : Science (In Hindi) – Lesson 1. रासायनिक अभिक्रियाएँ एवं समीकरण
पाठ का विश्लेषण एवं विवेचन
🔵 व्याख्या (Explanation)
रसायन विज्ञान का यह अध्याय हमें यह सिखाता है कि पदार्थ किस प्रकार आपस में क्रिया करके नए पदार्थों का निर्माण करते हैं। इन परिवर्तनों को हम रासायनिक अभिक्रियाओं और समीकरणों के रूप में व्यक्त करते हैं। आइए इसे चरणबद्ध ढंग से समझें।
🟢 1️⃣ रासायनिक अभिक्रिया क्या है
जब एक या अधिक पदार्थ (अभिकारक) मिलकर एक या अधिक नए पदार्थ (उत्पाद) बनाते हैं, तो इसे रासायनिक अभिक्रिया कहते हैं।
💡 उदाहरण:
जब मैग्नीशियम की पट्टी को जलाकर ऑक्सीजन में जलाया जाता है, तो सफेद रंग का मैग्नीशियम ऑक्साइड बनता है।
➡️ Mg + O₂ → MgO
✏️ ध्यान दें: रासायनिक अभिक्रिया में पदार्थों की संरचना बदल जाती है, केवल अवस्था नहीं।
🟢 2️⃣ रासायनिक अभिक्रिया के लक्षण
रासायनिक अभिक्रिया के समय निम्नलिखित परिवर्तन देखे जा सकते हैं –
🔵 रंग में परिवर्तन
🟢 ऊष्मा का निकलना या अवशोषण
🟡 गैस का उत्सर्जन
🔴 ठोस पदार्थ (अवक्षेप) का बनना
💡 उदाहरण: जब लोहा (Fe) कॉपर सल्फेट (CuSO₄) के विलयन में डाला जाता है, तो नीला रंग हल्का हरा हो जाता है और ताँबे की परत जम जाती है।
✔️ Fe + CuSO₄ → FeSO₄ + Cu
🟢 3️⃣ रासायनिक समीकरण (Chemical Equation)
रासायनिक अभिक्रिया को प्रतीकों द्वारा व्यक्त करने को रासायनिक समीकरण कहते हैं।
💡 उदाहरण: हाइड्रोजन और ऑक्सीजन मिलकर जल बनाते हैं।
➡️ H₂ + O₂ → H₂O
✏️ ध्यान दें: यह असंतुलित समीकरण है।
संतुलित रूप: 2H₂ + O₂ → 2H₂O
🟢 4️⃣ संतुलित रासायनिक समीकरण
➡️ द्रव्यमान संरक्षण का नियम: “किसी भी रासायनिक अभिक्रिया में अभिकारकों और उत्पादों में परमाणुओं की संख्या समान रहती है।”
💡 उदाहरण:
Zn + HCl → ZnCl₂ + H₂
यह समीकरण संतुलित है क्योंकि Zn, Cl और H दोनों ओर समान हैं।
🟢 5️⃣ समीकरण संतुलन की विधि
✏️ चरण 1: सबसे जटिल पदार्थ से संतुलन प्रारम्भ करें।
✏️ चरण 2: पहले धातु, फिर अधातु, फिर हाइड्रोजन और अंत में ऑक्सीजन को संतुलित करें।
✏️ चरण 3: समीकरण में आवश्यक गुणांक जोड़ें।
💡 उदाहरण: Fe + H₂O → Fe₃O₄ + H₂
➡️ 3Fe + 4H₂O → Fe₃O₄ + 4H₂
✔️ अब समीकरण संतुलित है।
🟢 6️⃣ रासायनिक अभिक्रियाओं के प्रकार
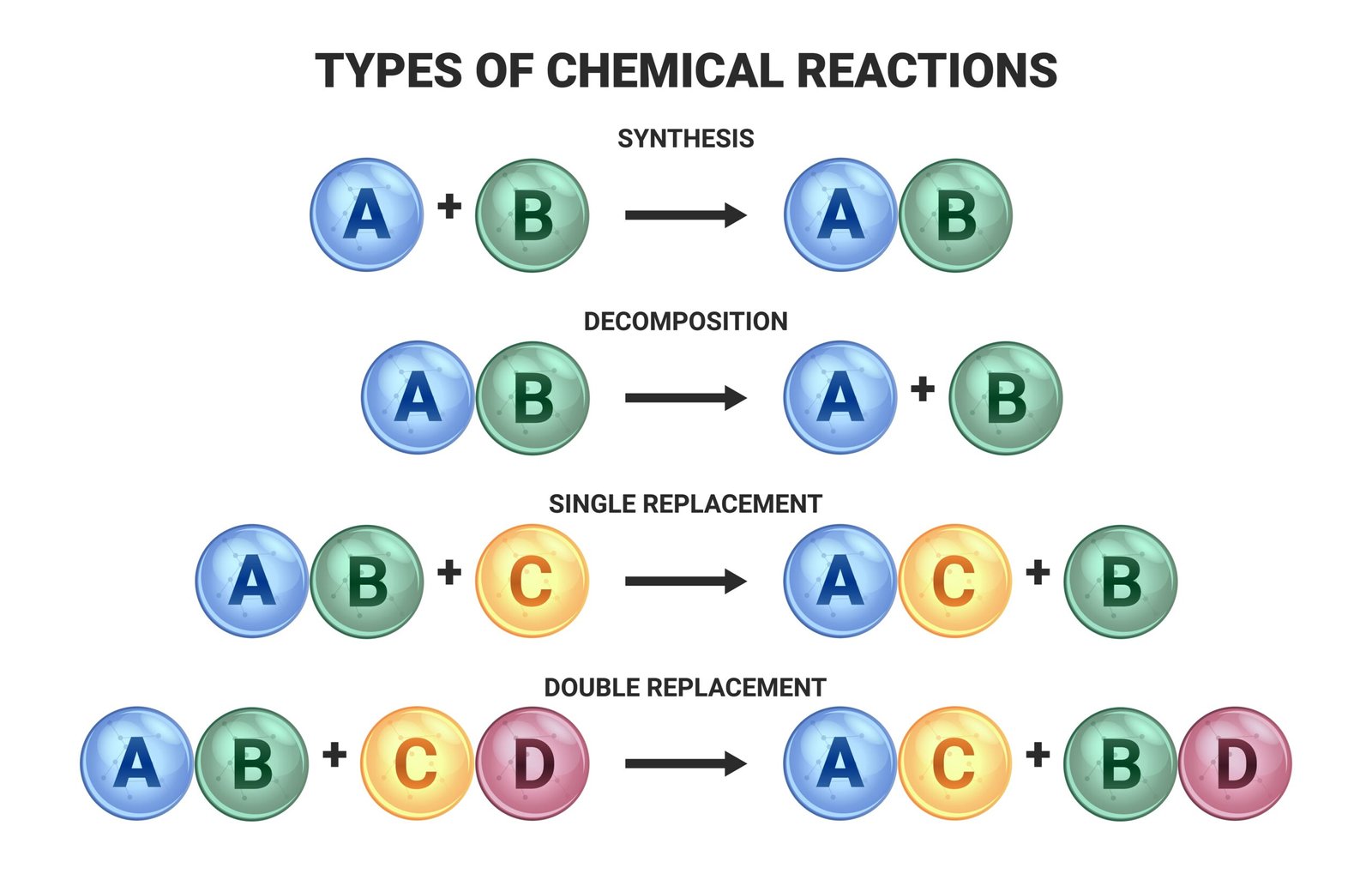
🔵 (i) संयोजन अभिक्रिया: दो या अधिक पदार्थ मिलकर एक नया पदार्थ बनाते हैं।
➡️ A + B → AB
उदाहरण: CaO + H₂O → Ca(OH)₂
🟢 (ii) अपघटन अभिक्रिया: एक यौगिक टूटकर दो या अधिक पदार्थ बनाता है।
➡️ AB → A + B
उदाहरण: 2Pb(NO₃)₂ → 2PbO + 4NO₂ + O₂
🟡 (iii) विस्थापन अभिक्रिया: अधिक क्रियाशील धातु कम क्रियाशील धातु को उसके यौगिक से विस्थापित करती है।
➡️ A + BC → AC + B
उदाहरण: Zn + CuSO₄ → ZnSO₄ + Cu
🔴 (iv) द्विविस्थापन अभिक्रिया: दो यौगिक अपने आयनों का आदान-प्रदान करते हैं।
➡️ AB + CD → AD + CB
उदाहरण: Na₂SO₄ + BaCl₂ → BaSO₄ + 2NaCl
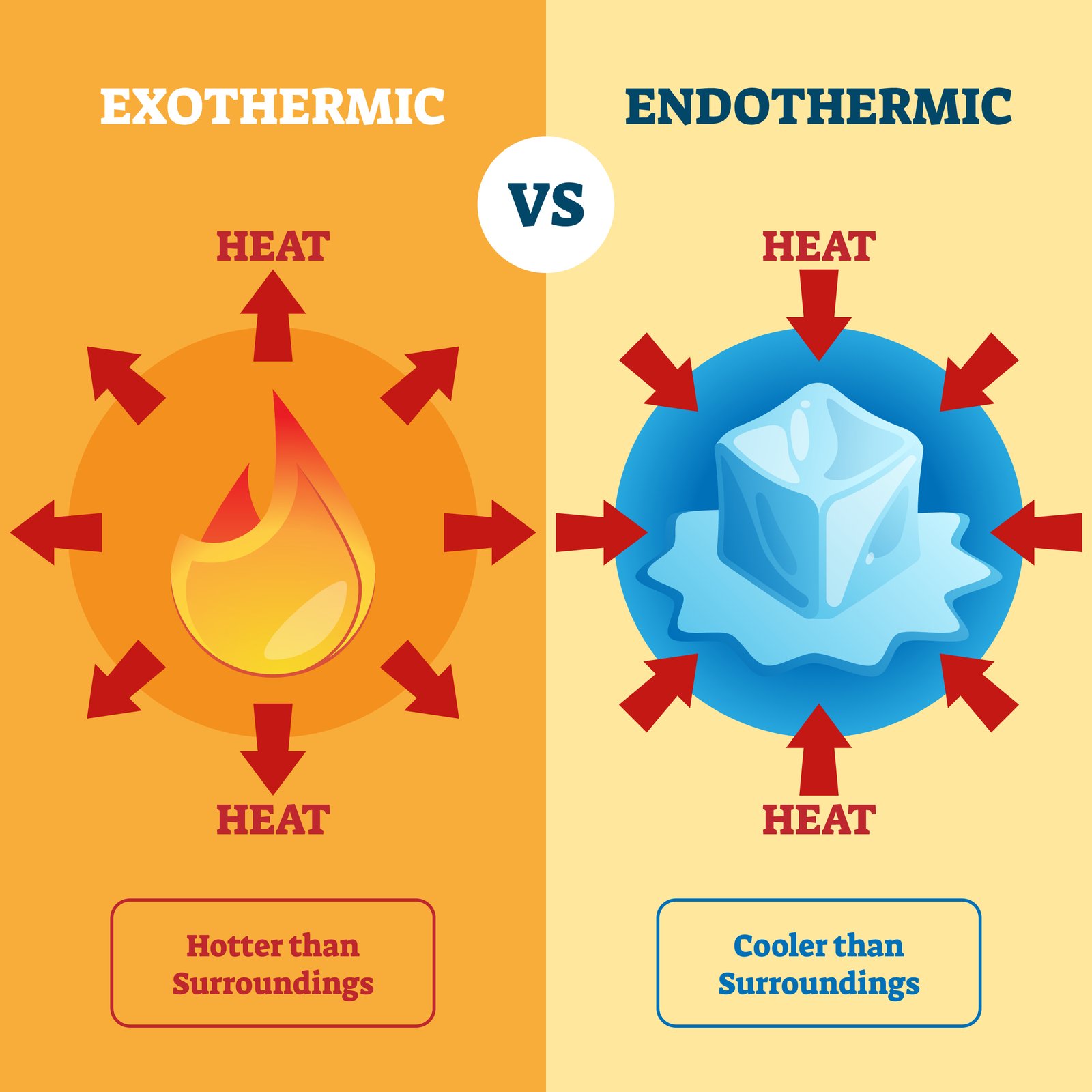
⚡ (v) उष्माक्षेपी और उष्माशोषी अभिक्रिया:
उष्माक्षेपी में ऊष्मा निकलती है जबकि उष्माशोषी में ऊष्मा अवशोषित होती है।
💡 उदाहरण:
➡️ उष्माक्षेपी: CH₄ + 2O₂ → CO₂ + 2H₂O + ऊष्मा
➡️ उष्माशोषी: 6CO₂ + 6H₂O + ऊष्मा → C₆H₁₂O₆ + 6O₂
🟢 7️⃣ ऑक्सीकरण और अपचयन अभिक्रिया
💡 ऑक्सीकरण: जब किसी पदार्थ में ऑक्सीजन जुड़ती है या हाइड्रोजन निकलती है।
💡 अपचयन: जब ऑक्सीजन निकलती है या हाइड्रोजन जुड़ती है।
✏️ उदाहरण: CuO + H₂ → Cu + H₂O
➡️ यहाँ CuO का अपचयन हुआ और H₂ का ऑक्सीकरण।
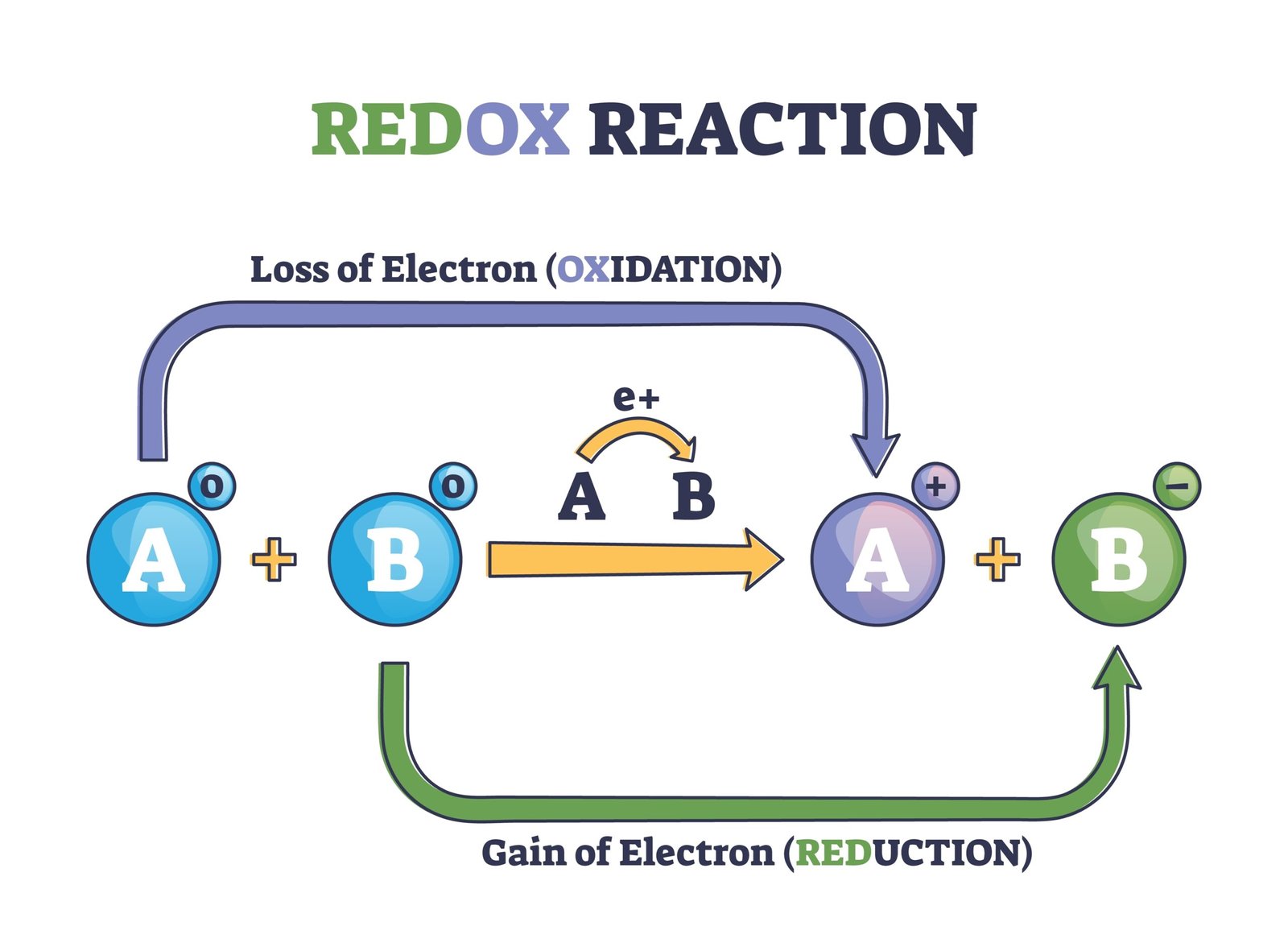
🟢 8️⃣ रिडॉक्स अभिक्रिया (Redox Reaction)
जब एक ही अभिक्रिया में ऑक्सीकरण और अपचयन दोनों होते हैं, उसे रिडॉक्स अभिक्रिया कहते हैं।
💡 उदाहरण: Zn + CuO → ZnO + Cu
➡️ Zn का ऑक्सीकरण, CuO का अपचयन होता है।
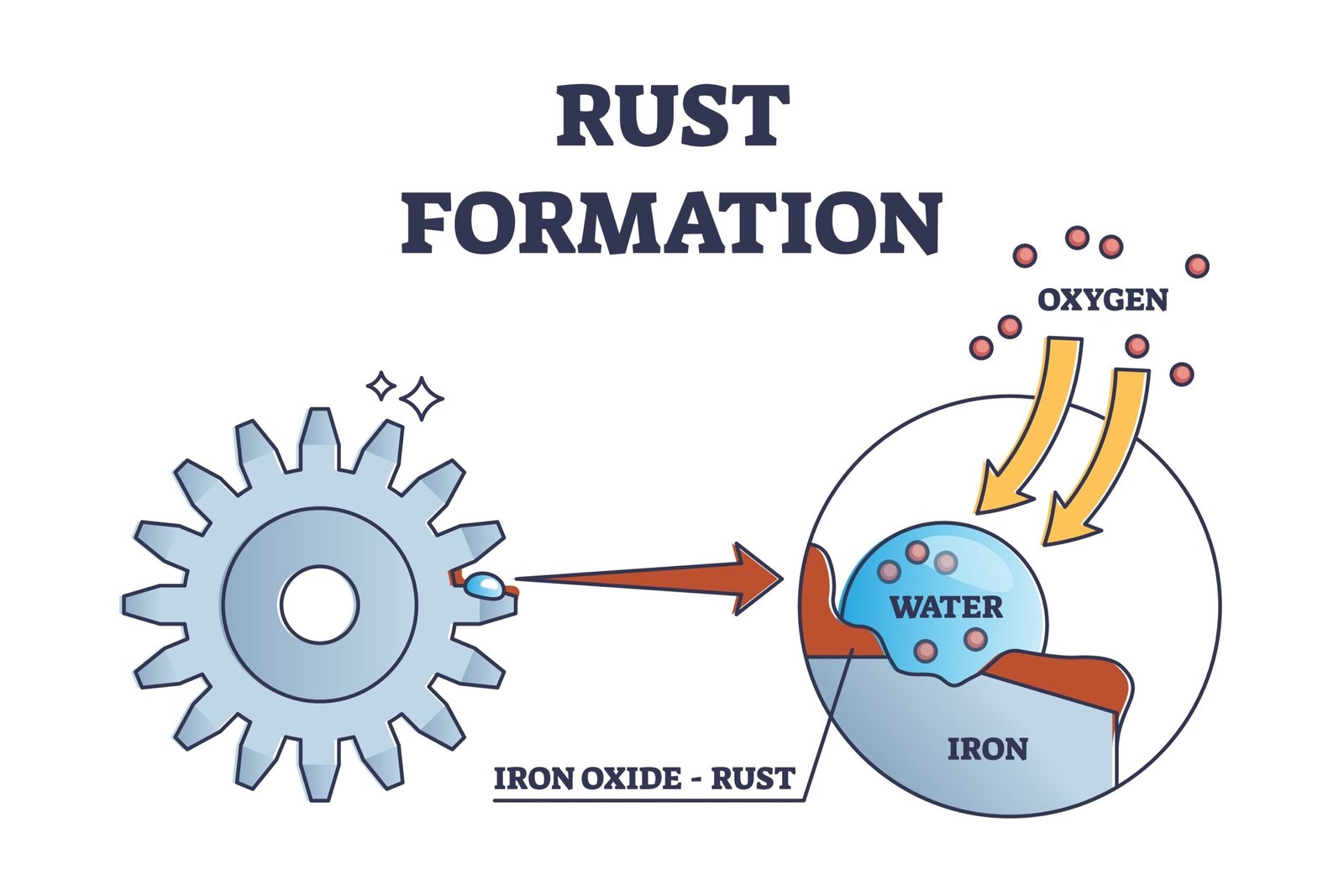
🟢 9️⃣ दैनिक जीवन में अभिक्रियाओं के उपयोग
🔵 लोहे में जंग लगना (Fe → Fe₂O₃·xH₂O)
🟢 भोजन का अपघटन
🟡 मोमबत्ती का जलना
🔴 प्रकाश संश्लेषण
🟢 10️⃣ द्रव्यमान संरक्षण का नियम
➡️ किसी रासायनिक अभिक्रिया में अभिकारकों और उत्पादों का कुल द्रव्यमान समान रहता है।
💡 उदाहरण:
BaCl₂ + Na₂SO₄ → BaSO₄ + 2NaCl
दोनों पक्षों पर परमाणुओं की संख्या समान है।
🟢 11️⃣ उत्प्रेरक (Catalyst)
अभिक्रिया की गति को नियंत्रित करने हेतु उत्प्रेरक का प्रयोग किया जाता है।
💡 उदाहरण: MnO₂, KClO₃ के अपघटन में उत्प्रेरक का कार्य करता है।
➡️ 2KClO₃ → 2KCl + 3O₂ (MnO₂ की उपस्थिति में)
🔵 सारांश (Summary)
✔️ रासायनिक अभिक्रिया में नए पदार्थ बनते हैं।
✔️ रासायनिक समीकरण द्वारा अभिक्रिया को प्रतीकात्मक रूप में लिखा जाता है।
✔️ समीकरण संतुलन से परमाणुओं की संख्या दोनों ओर समान रहती है।
✔️ अभिक्रियाओं के पाँच मुख्य प्रकार – संयोजन, अपघटन, विस्थापन, द्विविस्थापन, उष्माक्षेपी/उष्माशोषी।
✔️ रिडॉक्स अभिक्रिया में ऑक्सीकरण व अपचयन दोनों घटित होते हैं।
✔️ द्रव्यमान संरक्षण का नियम हर अभिक्रिया पर लागू होता है।
✔️ उत्प्रेरक अभिक्रिया की गति को प्रभावित करता है।
📝 Quick Recap
🔵 रासायनिक अभिक्रिया = नए पदार्थों का निर्माण
🟢 रासायनिक समीकरण = प्रतीकात्मक प्रदर्शन
🟡 संतुलन = दोनों ओर समान परमाणु
🔴 मुख्य प्रकार = संयोजन, अपघटन, विस्थापन, द्विविस्थापन
⚡ रिडॉक्स = ऑक्सीकरण + अपचयन
✔️ नियम = द्रव्यमान संरक्षण सिद्धांत
————————————————————————————————————————————————————————————————————————————
पाठ्यपुस्तक के प्रश्न
🔵 Question 1:
नीचे दी गई अभिक्रियाओं के संबंध में कौन-सा कथन असत्य है?
2PbO(s) + C(s) → 2Pb(s) + CO₂(g)
(a) सीसा अपचयित हो रहा है।
(b) कार्बन डाइऑक्साइड उत्पन्न हो रही है।
(c) कार्बन अपचयित हो रहा है।
(d) कार्बन ऑक्साइड अपचयित हो रहा है।
(i) (a) एवं (b)
(ii) (a) एवं (c)
(iii) (b) एवं (c)
(iv) सभी
🟢 Answer:
🔵 अभिक्रिया में PbO का अपचयन होता है क्योंकि Pb बन रहा है।
🟢 C (कार्बन) का ऑक्सीकरण होकर CO₂ बन रहा है।
🟡 अतः (a) और (b) कथन सही हैं पर (c) असत्य है क्योंकि कार्बन का अपचयन नहीं बल्कि ऑक्सीकरण हो रहा है।
✔️ सही उत्तर: (ii) (a) एवं (c)
🔵 Question 2:
Fe₂O₃ + 2Al → Al₂O₃ + 2Fe
उपरोक्त अभिक्रिया किस प्रकार की है?
(a) संयोजन अभिक्रिया
(b) द्विविस्थापन अभिक्रिया
(c) विस्थापन अभिक्रिया
(d) विघटन अभिक्रिया
🟢 Answer:
🔵 यहाँ Al, Fe को उसके यौगिक Fe₂O₃ से विस्थापित करता है।
🟢 यह एक विस्थापन अभिक्रिया (Displacement Reaction) है।
💡 इसे थर्माइट अभिक्रिया भी कहा जाता है, जिसमें तीव्र ऊष्मा उत्पन्न होती है।
✔️ सही उत्तर: (c) विस्थापन अभिक्रिया
🔵 Question 3:
लोहे-तांबे पर हाइड्रोक्लोरिक अम्ल डालने से क्या होता है? सही उत्तर पर निशान लगाइए –
(a) हाइड्रोजन गैस एवं आयरन क्लोराइड बनता है।
(b) क्लोरीन गैस एवं आयरन हाइड्रॉक्साइड बनता है।
(c) कोई अभिक्रिया नहीं होती है।
(d) आयरन लवण एवं जल बनता है।
🟢 Answer:
🔵 जब लोहा (Fe) हाइड्रोक्लोरिक अम्ल (HCl) के साथ क्रिया करता है –
➡️ Fe + 2HCl → FeCl₂ + H₂↑
🟢 हाइड्रोजन गैस निकलती है और आयरन क्लोराइड बनता है।
✔️ सही उत्तर: (a) हाइड्रोजन गैस एवं आयरन क्लोराइड बनता है।
🔵 Question 4:
संतुलित रासायनिक समीकरण क्या है? रासायनिक समीकरण को संतुलित करना क्यों आवश्यक है?
🟢 Answer:
💡 संतुलित रासायनिक समीकरण: वह समीकरण जिसमें अभिकारकों और उत्पादों में प्रत्येक तत्व के परमाणुओं की संख्या समान हो।
✏️ आवश्यकता:
🔵 द्रव्यमान संरक्षण का नियम कहता है कि अभिक्रिया के दोनों ओर द्रव्यमान समान रहता है।
🟢 अतः समीकरण को संतुलित करना आवश्यक है ताकि परमाणुओं की संख्या दोनों ओर बराबर रहे।
💡 उदाहरण:
➡️ असंतुलित – H₂ + O₂ → H₂O
➡️ संतुलित – 2H₂ + O₂ → 2H₂O
✔️ इसलिए समीकरण संतुलन वैज्ञानिक रूप से अनिवार्य है।
🔵 Question 5:
निम्न कथनों को रासायनिक समीकरणों के रूप में परिवर्तित कर उन्हें संतुलित कीजिए।
(a) नाइट्रोजन हाइड्रोजन गैस के संयोग से अमोनिया बनाती है।
(b) हाइड्रोजन सल्फाइड गैस का वायु में जलने पर सल्फर डाइऑक्साइड बनता है।
(c) एल्यूमिनियम सल्फेट के साथ अभिक्रिया कर सोडियम क्लोराइड, एल्यूमिनियम हाइड्रॉक्साइड एवं बेरियम सल्फेट का अवक्षेप देता है।
(d) पोटेशियम धातु जल के साथ अभिक्रिया कर पोटेशियम हाइड्रॉक्साइड एवं हाइड्रोजन गैस देती है।
🟢 Answer:
🔵 (a) N₂ + 3H₂ → 2NH₃
🟢 (b) 2H₂S + 3O₂ → 2SO₂ + 2H₂O
🟡 (c) Al₂(SO₄)₃ + 3BaCl₂ → 2AlCl₃ + 3BaSO₄↓
🔴 (d) 2K + 2H₂O → 2KOH + H₂↑
✔️ सभी समीकरण संतुलित रूप में प्रदर्शित हैं।
🔵 Question 6:
निम्न रासायनिक समीकरणों को संतुलित कीजिए –
(a) HNO₃ + Ca(OH)₂ → Ca(NO₃)₂ + H₂O
(b) NaOH + H₂SO₄ → Na₂SO₄ + H₂O
(c) NaCl + AgNO₃ → AgCl + NaNO₃
(d) BaCl₂ + H₂SO₄ → BaSO₄ + HCl
🟢 Answer:
🔵 (a) 2HNO₃ + Ca(OH)₂ → Ca(NO₃)₂ + 2H₂O
🟢 (b) 2NaOH + H₂SO₄ → Na₂SO₄ + 2H₂O
🟡 (c) NaCl + AgNO₃ → AgCl + NaNO₃
🔴 (d) BaCl₂ + H₂SO₄ → BaSO₄ + 2HCl
✔️ सभी समीकरण संतुलित हैं और प्रत्येक में परमाणुओं की संख्या समान है।
🔵 Question 7:
निम्न अभिक्रियाओं के लिए रासायनिक समीकरण लिखिए और उन्हें संतुलित कीजिए –
(a) कैल्शियम हाइड्रॉक्साइड एवं कार्बन डाइऑक्साइड → कैल्शियम कार्बोनेट + जल
(b) जिंक एवं हाइड्रोक्लोरिक अम्ल → जिंक क्लोराइड + हाइड्रोजन गैस
(c) अमोनियम क्लोराइड → अमोनिया + हाइड्रोजन क्लोराइड
🟢 Answer:
🔵 (a) Ca(OH)₂ + CO₂ → CaCO₃ + H₂O
🟢 (b) Zn + 2HCl → ZnCl₂ + H₂↑
🟡 (c) NH₄Cl → NH₃ + HCl
✔️ सभी समीकरण संतुलित हैं और पदार्थों की पहचान सही है।
🔵 Question 8
निम्न अभिक्रियाओं के लिए संतुलित रासायनिक समीकरण लिखिए एवं प्रत्येक अभिक्रिया का प्रकार बताइए
(a) पोटेशियम ब्रोमाइड (aq) + बेरियम आयोडाइड (aq) → पोटेशियम आयोडाइड (aq) + बेरियम ब्रोमाइड (aq)
(b) जिंक कार्बोनेट (s) → जिंक ऑक्साइड (s) + कार्बन डाइऑक्साइड (g)
(c) हाइड्रोजन (g) + क्लोरीन (g) → हाइड्रोजन क्लोराइड (g)
(d) मैग्नीशियम + हाइड्रोक्लोरिक अम्ल (aq) → मैग्नीशियम क्लोराइड (aq) + हाइड्रोजन (g)
🟢 Answer
(a) संतुलित समीकरण
🔵 2KBr (aq) + BaI₂ (aq) → 2KI (aq) + BaBr₂ (aq)
🟢 प्रकार
💡 यह एक द्विविस्थापन अभिक्रिया है, क्योंकि आयनों का परस्पर आदान-प्रदान होता है।
✔️ प्रकार: द्विविस्थापन अभिक्रिया
(b) संतुलित समीकरण
🔵 ZnCO₃ (s) → ZnO (s) + CO₂ (g)
🟢 प्रकार
💡 यह एक अपघटन अभिक्रिया है क्योंकि एक यौगिक (ZnCO₃) टूटकर दो सरल पदार्थ (ZnO और CO₂) बनाता है।
✔️ प्रकार: अपघटन अभिक्रिया
(c) संतुलित समीकरण
🔵 H₂ (g) + Cl₂ (g) → 2HCl (g)
🟢 प्रकार
💡 यह एक संयोजन अभिक्रिया है क्योंकि दो तत्त्व (H₂ और Cl₂) मिलकर एक नया यौगिक (HCl) बनाते हैं।
✔️ प्रकार: संयोजन अभिक्रिया
(d) संतुलित समीकरण
🔵 Mg (s) + 2HCl (aq) → MgCl₂ (aq) + H₂ (g)
🟢 प्रकार
💡 यह एक विस्थापन अभिक्रिया है क्योंकि मैग्नीशियम, हाइड्रोजन को उसके यौगिक (HCl) से विस्थापित करता है।
✔️ प्रकार: विस्थापन अभिक्रिया
🔵 Question 9
अभ्यासों में दर्शाई गई अभिक्रियाएँ ऊष्माक्षेपी हैं अथवा उष्माशोषी हैं? क्या आपको ऐसा लगता है? इन अभिक्रियाओं के लिए अपने उत्तर का कारण बताइए।
🟢 Answer
✏️ सबसे पहले
🔵 उष्माक्षेपी अभिक्रिया वह है जिसमें ऊष्मा निकलती है।
🟢 उष्माशोषी अभिक्रिया वह है जिसमें ऊष्मा अवशोषित होती है।
💡 अब देखें
🟡 मैग्नीशियम + हाइड्रोक्लोरिक अम्ल → मैग्नीशियम क्लोराइड + हाइड्रोजन
➡️ Mg (s) + 2HCl (aq) → MgCl₂ (aq) + H₂ (g)
⚡ यह अभिक्रिया ऊष्मा उत्पन्न करती है, अर्थात उष्माक्षेपी है।
🔴 जिंक कार्बोनेट का जिंक ऑक्साइड और कार्बन डाइऑक्साइड में विघटन
➡️ ZnCO₃ (s) → ZnO (s) + CO₂ (g)
⚡ यह अपघटन प्रायः ऊष्मा देकर कराया जाता है, अर्थात ऊष्मा अवशोषित की जाती है, इसलिए यह उष्माशोषी है।
✔️ निष्कर्ष
🔵 कुछ अभिक्रियाएँ (जैसे धातु + अम्ल) उष्माक्षेपी हैं।
🟢 कुछ अभिक्रियाएँ (जैसे अपघटन ऊष्मा देकर) उष्माशोषी हैं।
✔️ Final: उत्तर इस बात पर आधारित है कि ऊष्मा बाहर निकल रही है या भीतर ली जा रही है।
🔵 Question 10
स्वतः स्फूर्त अभिक्रियाएँ अप्रिय क्यों होती हैं?
🟢 Answer
💡 स्वतः स्फूर्त अभिक्रिया वह है जो अपने आप घटित होती है, बिना बाहरी बाध्यता के।
🔵 कई स्वतः स्फूर्त अभिक्रियाएँ धातुओं को नष्ट करती हैं, जैसे लोहे में जंग लगना।
🟢 जंग की प्रक्रिया Fe → Fe₂O₃·xH₂O धातु को कमजोर करती है और वस्तु की शक्ति घटाती है।
🟡 इसी प्रकार भोजन का सड़ना भी स्वतः होने वाली रासायनिक अभिक्रिया है जो हानिकर है।
✔️ इसलिए स्वतः स्फूर्त अभिक्रियाएँ अक्सर अवांछनीय होती हैं क्योंकि वे पदार्थों को क्षति पहुँचाती हैं, गुणवत्ता घटाती हैं, और नियंत्रण में नहीं रहतीं।
🔵 Question 11
कई बार रासायनिक अभिक्रिया को रोका जाना क्यों आवश्यक होता है? इन अभिक्रियाओं के लिए कारण दीजिए।
🟢 Answer
🔵 कुछ अभिक्रियाएँ हानिकर उत्पाद उत्पन्न करती हैं, जैसे विषैली गैसें।
🟢 कुछ अभिक्रियाएँ पदार्थों को नष्ट करती हैं (धातु का क्षरण, भोजन का खराब होना)।
🟡 कुछ अभिक्रियाएँ यदि चलती रहें तो ऊष्मा बहुत अधिक निकल सकती है जिससे दुर्घटना हो सकती है।
💡 उदाहरण: धातु और प्रबल अम्ल के बीच तीव्र अभिक्रिया से अत्यधिक ऊष्मा और गैस उत्पन्न होती है।
✔️ इसलिए नियंत्रण (या रोकना) सुरक्षित उपयोग, संरक्षण, और गुणवत्ता बनाए रखने के लिए आवश्यक है।
🔵 Question 12
हम विभिन्न अभिक्रियाओं के एक-एक उदाहरण लिखिए, जिनमें ऊष्मा, प्रकाश तथा विद्युत के रूप में ऊर्जा प्रदान की जाती है।
🟢 Answer
✴️ (A) ऊष्मा द्वारा आरंभ की गई अभिक्रिया
🔵 CaCO₃ (s) → CaO (s) + CO₂ (g)
➡️ यह अपघटन अभिक्रिया ऊष्मा देकर कराई जाती है।
✔️ यहाँ ऊष्मा ऊर्जा दी जाती है।
✴️ (B) प्रकाश द्वारा आरंभ की गई अभिक्रिया
🔵 2AgCl (s) → 2Ag (s) + Cl₂ (g)
➡️ यह अभिक्रिया प्रकाश के प्रभाव में होती है।
✔️ यह प्रकाशीय अपघटन है।
✴️ (C) विद्युत द्वारा आरंभ की गई अभिक्रिया
🔵 2H₂O (l) → 2H₂ (g) + O₂ (g)
➡️ यह अपघटन विद्युत धारा से होता है (जल का विद्युत अपघटन)।
✔️ यहाँ ऊर्जा विद्युत के रूप में दी जाती है।
✔️ Final: अलग-अलग अभिक्रियाएँ अलग-अलग ऊर्जा रूप से आरंभ की जा सकती हैं — ऊष्मा, प्रकाश, विद्युत।
🔵 Question 13
विघटन एवं द्विविघटन अभिक्रिया में क्या अंतर है? इन अभिक्रियाओं के लिए उदाहरण दीजिए।
🟢 Answer
💡 विघटन अभिक्रिया (अपघटन)
🔵 एक यौगिक टूटकर दो या अधिक सरल पदार्थ बनाता है।
➡️ उदाहरण: 2Pb(NO₃)₂ → 2PbO + 4NO₂ + O₂
🟢 यहाँ एक यौगिक से अनेक उत्पाद बने, इसलिए यह अपघटन है।
💡 द्विविघटन अभिक्रिया (द्विविस्थापन)
🟡 दो यौगिक अपने आयनों का परस्पर आदान-प्रदान करते हैं और नए यौगिक बनते हैं।
➡️ उदाहरण: Na₂SO₄ + BaCl₂ → BaSO₄ + 2NaCl
🔴 यहाँ आयनों का विनिमय हुआ है (Na ↔ Ba के साथ SO₄ और Cl का अदला-बदली), इसलिए यह द्विविस्थापन है।
✔️ Final:
विघटन = एक यौगिक टूटता है।
द्विविघटन (द्विविस्थापन) = दो यौगिक आपस में आयन बदलते हैं।
🔵 Question 14
विकिरण के कारण, फिटकरी लगाने से घाव भरने में सहायता मिलती है। फिटकरी को बाँधने के लिए तथा घाव के लिए इसे बाँधने की प्रक्रिया के लिए रासायनिक कारण बताइए।
🟢 Answer
✏️ पहले समझें
🔵 फिटकरी का उपयोग घाव पर इसलिए किया जाता है क्योंकि यह संकुचन (सिकुड़न) और जमाव में सहायता करती है।
🟢 यह रक्तस्राव को कम करने में सहायक है।
🟡 फिटकरी जल के संपर्क में आयनित होकर ऐसे लवण देती है जो ऊतक (टिशू) को संकुचित करते हैं और जमने में सहायता करते हैं।
✔️ इस कारण से घाव बंद होने में सहायता मिलती है और बैक्टीरिया का प्रसार भी धीमा होता है।
💡 इसलिए फिटकरी का प्रयोग एक रासायनिक आधार पर है: यह ऊतक-संकुचनकारी (संकोचक) क्रिया करती है।
🔵 Question 15
अवक्षेपण अभिक्रिया से आप क्या समझते हैं? उदाहरण देकर समझाइए।
🟢 Answer
💡 अवक्षेपण अभिक्रिया वह अभिक्रिया है जिसमें दो विलयन आपस में क्रिया करके एक अघुलनशील ठोस बनाते हैं जिसे अवक्षेप कहते हैं।
🔵 उदाहरण
➡️ Na₂SO₄ (aq) + BaCl₂ (aq) → BaSO₄ (s)↓ + 2NaCl (aq)
🟢 यहाँ BaSO₄ अवक्षेप के रूप में नीचे बैठता है।
✔️ Final: जब किसी अभिक्रिया में अघुलनशील ठोस बनकर नीचे बैठता है, वह अवक्षेपण अभिक्रिया है।
🔵 Question 16
ऑक्सीजन के पाने या हानि के आधार पर निम्न पदों की व्याख्या कीजिए। प्रत्येक के लिए दो उदाहरण दीजिए
(a) उच्छ्वसन
(b) अपचयन
🟢 Answer
✏️ पहले आधार स्पष्ट करें
🔵 ऑक्सीकरण = ऑक्सीजन का जुड़ना या हाइड्रोजन का निकलना।
🟢 अपचयन = ऑक्सीजन का निकलना या हाइड्रोजन का जुड़ना।
(a) उच्छ्वसन (यहाँ अर्थ है ऑक्सीकरण)
💡 जब किसी पदार्थ में ऑक्सीजन जुड़ती है तो वह ऑक्सीकरण कहलाता है।
🔵 उदाहरण 1: 2Mg + O₂ → 2MgO
🔵 उदाहरण 2: C + O₂ → CO₂
✔️ दोनों में पदार्थ ने ऑक्सीजन ग्रहण की है।
(b) अपचयन
💡 जब किसी पदार्थ से ऑक्सीजन हटती है या हाइड्रोजन जुड़ती है तो यह अपचयन है।
🟢 उदाहरण 1: CuO + H₂ → Cu + H₂O
🟢 उदाहरण 2: Fe₂O₃ + 2Al → Al₂O₃ + 2Fe
✔️ दोनों में धातु के ऑक्साइड से ऑक्सीजन निकल रही है और धातु मुक्त हो रही है, यह अपचयन है।
🔵 Question 17
एक धातु ‘X’ का चमकदार तत्त्व ‘X’ का वायु की उपस्थिति में गर्म करने पर वह काला हो जाता है। इस तत्त्व ‘X’ एवं उस काले के लिए रासायनिक का नाम बताइए।
🟢 Answer
💡 दिया गया है: धातु X को वायु में गरम करने पर वह काला हो जाता है।
🔵 यह सामान्यतः तांबा (Cu) के साथ होता है।
🟢 तांबा वायु में गरम होने पर काला कॉपर ऑक्साइड (CuO) बनाता है।
➡️ 2Cu + O₂ → 2CuO
✔️ Final:
🔵 ‘X’ = तांबा (Cu)
🟢 बना काला पदार्थ = कॉपर ऑक्साइड (CuO), अर्थात तांबे का ऑक्साइड।
🔵 Question 18
लोहे की वस्तुओं को हम पर पेंट क्यों करते हैं?
🟢 Answer
🔵 लोहा वायु में आक्सीजन और आर्द्रता के संपर्क में आने पर जंग खा जाता है (Fe₂O₃·xH₂O की परत बनती है)।
🟢 पेंट एक आवरण की तरह काम करता है, जो वायु और नमी को सीधे लोहे तक पहुँचने से रोकता है।
🟡 इसलिए पेंट लोहे को जंग से बचाता है और उसकी आयु बढ़ाता है।
✔️ Final: पेंट लोहे को जंग (क्षरण) से बचाने के लिए लगाया जाता है।
🔵 Question 19
फल एवं सब्जियों को खाया जाने योग्य नाइट्रोजन से प्रभावित क्यों किया जाता है?
🟢 Answer
💡 ताज़े फल और सब्जियाँ जल्दी खराब हो सकते हैं क्योंकि वे वायु (ऑक्सीजन) में ऑक्सीकरण और अपघटन से बदलते रहते हैं।
🔵 जब उन्हें कुछ नियंत्रित वातावरण में रखा जाता है (जैसे कम ऑक्सीजन / नियंत्रित गैसें), तो उनका खराब होना धीमा होता है।
🟢 इस प्रक्रिया में वायुमंडलीय संघटन को बदला जाता है ताकि सूक्ष्मजीवी क्रिया और ऑक्सीकरण धीमा हो।
✔️ Final: नियंत्रित वातावरण (अनुकूल गैस मिश्रण) फल और सब्जियों के खराब होने की दर कम करता है, इसलिए भंडारण अवधि बढ़ती है।
🔵 Question 20
निम्नलिखित में से कौन-सा पदार्थ संक्षारण को रोकने का एक उदाहरण दीजिए।
(a) संक्षारण
(b) विकृतगुणिता
🟢 Answer
✏️ पहले स्पष्ट करें
🔵 संक्षारण (क्षरण) = धातु का धीरे-धीरे नष्ट होना, जैसे लोहे में जंग लगना।
🟢 संक्षारण को रोकने का एक तरीका है — पेंट करना, तैलीय लेप देना, जस्ता चढ़ाना (गैल्वनाइज़ करना)।
✔️ Final: लोहे की सतह पर पेंट करना संक्षारण को रोकने का उदाहरण है।
(नोट: “विकृतगुणिता” शब्द यहाँ प्रसंग में संक्षारण-रोधक के रूप में प्रयुक्त नहीं होता; मुख्य उत्तर संक्षारण-रोध के उपाय पर केंद्रित है।)
————————————————————————————————————————————————————————————————————————————
अन्य महत्वपूर्ण प्रश्न
(CBSE MODEL प्रश्न पत्र)
सिर्फ इसी पाठ से निर्मित CBSE MODEL प्रश्न पत्र
🔵 Section A (प्रश्न 1–6) – 1 अंक वाले प्रश्न (बहुविकल्पीय व बहुत लघु उत्तर)
Question 1:
निम्न में से कौन-सी अभिक्रिया उष्माक्षेपी है?
🔵 (A) 2H₂ + O₂ → 2H₂O
🟢 (B) 6CO₂ + 6H₂O → C₆H₁₂O₆ + 6O₂
🟠 (C) CaCO₃ → CaO + CO₂
🔴 (D) AgCl → Ag + Cl₂
Answer: (A) 2H₂ + O₂ → 2H₂O ✔️ (ऊष्मा निकलती है)
Question 2:
किसी रासायनिक अभिक्रिया में अभिकारकों और उत्पादों का कुल द्रव्यमान समान रहता है। यह किस नियम को दर्शाता है?
🔵 (A) ऊष्मा संरक्षण का नियम
🟢 (B) द्रव्यमान संरक्षण का नियम
🟠 (C) ऊर्जा संरक्षण का नियम
🔴 (D) संवेग संरक्षण का नियम
Answer: (B) द्रव्यमान संरक्षण का नियम ✔️
Question 3:
CuO + H₂ → Cu + H₂O अभिक्रिया में कौन ऑक्सीकरण हो रहा है?
🔵 (A) Cu
🟢 (B) CuO
🟠 (C) H₂
🔴 (D) H₂O
Answer: (C) H₂ ✔️ (क्योंकि यह H₂O में परिवर्तित होता है)
Question 4:
मैग्नीशियम जब ऑक्सीजन में जलता है तो क्या बनता है?
🔵 (A) MgO
🟢 (B) MgCO₃
🟠 (C) Mg(OH)₂
🔴 (D) MgSO₄
Answer: (A) MgO ✔️
Question 5:
नीचे दी गई अभिक्रिया का प्रकार बताइए –
Zn + CuSO₄ → ZnSO₄ + Cu
🔵 (A) संयोजन
🟢 (B) अपघटन
🟠 (C) विस्थापन
🔴 (D) द्विविस्थापन
Answer: (C) विस्थापन ✔️
Question 6:
Fe + H₂O → Fe₃O₄ + H₂ यह अभिक्रिया है –
🔵 (A) संयोजन
🟢 (B) अपघटन
🟠 (C) विस्थापन
🔴 (D) द्विविस्थापन
Answer: (C) विस्थापन ✔️
🟢 Section B (प्रश्न 7–12) – 2 अंक वाले प्रश्न
Question 7:
रासायनिक अभिक्रिया के दो लक्षण लिखिए।
Answer:
🔵 रंग परिवर्तन (जैसे नीले विलयन का हरा होना)
🟢 गैस या अवक्षेप का बनना
✔️ ये दोनों लक्षण अभिक्रिया के घटित होने का संकेत देते हैं।
Question 8:
असंतुलित समीकरण H₂ + Cl₂ → HCl को संतुलित कीजिए।
Answer:
🔵 असंतुलित समीकरण: H₂ + Cl₂ → HCl
🔵 संतुलन हेतु: 2HCl में 2 H और 2 Cl परमाणु हैं।
✔️ संतुलित समीकरण: H₂ + Cl₂ → 2HCl
Question 9:
विस्थापन अभिक्रिया का एक उदाहरण दीजिए।
Answer:
🔵 उदाहरण: Fe + CuSO₄ → FeSO₄ + Cu
🟢 यहाँ Fe ने Cu को विस्थापित किया।
✔️ यह एक विस्थापन अभिक्रिया है।
Question 10:
ऑक्सीकरण और अपचयन को परिभाषित कीजिए।
Answer:
💡 ऑक्सीकरण: जब किसी पदार्थ में ऑक्सीजन जुड़ती है या हाइड्रोजन निकलती है।
💡 अपचयन: जब ऑक्सीजन निकलती है या हाइड्रोजन जुड़ती है।
✔️ उदाहरण: CuO + H₂ → Cu + H₂O
Question 11:
रासायनिक समीकरण संतुलित करने की आवश्यकता क्यों होती है?
Answer:
🔵 द्रव्यमान संरक्षण का नियम कहता है कि अभिक्रिया के दोनों ओर परमाणुओं की संख्या समान होनी चाहिए।
✔️ अतः समीकरण संतुलन आवश्यक है।
Question 12:
किसी उष्माशोषी अभिक्रिया का एक उदाहरण लिखिए।
Answer:
🔵 प्रकाश संश्लेषण:
6CO₂ + 6H₂O + ऊष्मा → C₆H₁₂O₆ + 6O₂
✔️ इस अभिक्रिया में सूर्य की ऊर्जा अवशोषित होती है।
🟡 Section C (प्रश्न 13–22) – 3 अंक वाले प्रश्न
Question 13:
रासायनिक अभिक्रियाओं के तीन प्रकार उदाहरण सहित लिखिए।
Answer:
🔵 संयोजन: A + B → AB (CaO + H₂O → Ca(OH)₂)
🟢 अपघटन: AB → A + B (2Pb(NO₃)₂ → 2PbO + 4NO₂ + O₂)
🟡 विस्थापन: A + BC → AC + B (Zn + CuSO₄ → ZnSO₄ + Cu)
Question 14:
निम्नलिखित समीकरण को संतुलित कीजिए –
CaCO₃ → CaO + CO₂
Answer:
🔵 असंतुलित समीकरण: CaCO₃ → CaO + CO₂
✔️ दोनों ओर सभी परमाणु समान हैं।
✔️ अतः यह पहले से संतुलित है।
Question 15:
“ऑक्सीकरण और अपचयन एक साथ क्यों घटित होते हैं?”
Answer:
🔵 क्योंकि जब एक पदार्थ ऑक्सीजन ग्रहण करता है (ऑक्सीकरण), तो दूसरा ऑक्सीजन खोता है (अपचयन)।
💡 दोनों प्रक्रियाएँ परस्पर निर्भर हैं।
✔️ इसलिए हर रिडॉक्स अभिक्रिया में दोनों एक साथ होती हैं।
Question 16:
Fe + CuSO₄ → FeSO₄ + Cu अभिक्रिया में अभिकारक और उत्पाद पहचानिए।
Answer:
🔵 अभिकारक: Fe और CuSO₄
🟢 उत्पाद: FeSO₄ और Cu
✔️ यह विस्थापन अभिक्रिया का उदाहरण है।
Question 17:
किसी द्विविस्थापन अभिक्रिया का एक उदाहरण दीजिए।
Answer:
Na₂SO₄ + BaCl₂ → BaSO₄ + 2NaCl
✔️ यह द्विविस्थापन अभिक्रिया है क्योंकि आयनों का आदान-प्रदान हुआ है।
Question 18:
नीचे दी गई अभिक्रिया का प्रकार बताइए –
2Pb(NO₃)₂ → 2PbO + 4NO₂ + O₂
Answer:
💡 यह एक अपघटन अभिक्रिया है क्योंकि यौगिक टूटकर अनेक पदार्थ बने।
Question 19 (OR):
(क) एक उष्माक्षेपी अभिक्रिया का उदाहरण लिखिए।
उत्तर: CH₄ + 2O₂ → CO₂ + 2H₂O + ऊष्मा
(ख) एक उष्माशोषी अभिक्रिया का उदाहरण लिखिए।
उत्तर: 6CO₂ + 6H₂O + ऊष्मा → C₆H₁₂O₆ + 6O₂
Question 20:
रिडॉक्स अभिक्रिया क्या है? एक उदाहरण सहित समझाइए।
Answer:
💡 रिडॉक्स अभिक्रिया वह होती है जिसमें ऑक्सीकरण और अपचयन दोनों साथ होते हैं।
➡️ उदाहरण: Zn + CuO → ZnO + Cu
✔️ Zn का ऑक्सीकरण और CuO का अपचयन हुआ।
Question 21:
समीकरण संतुलन की प्रक्रिया को चरणों में लिखिए।
Answer:
✏️ चरण 1: सबसे जटिल पदार्थ से प्रारम्भ करें।
✏️ चरण 2: धातु, अधातु, फिर हाइड्रोजन, अंत में ऑक्सीजन।
✏️ चरण 3: गुणांक लगाकर परमाणुओं की संख्या बराबर करें।
✔️ उदाहरण: 3Fe + 4H₂O → Fe₃O₄ + 4H₂
Question 22:
रासायनिक अभिक्रियाओं के लक्षणों को उदाहरण सहित समझाइए।
Answer:
🔵 रंग परिवर्तन – Fe + CuSO₄ → FeSO₄ + Cu
🟢 गैस का उत्सर्जन – Zn + H₂SO₄ → ZnSO₄ + H₂
🟡 ऊष्मा परिवर्तन – CH₄ + 2O₂ → CO₂ + 2H₂O + ऊष्मा
🔴 Section D (प्रश्न 23–30) – दीर्घ उत्तर (4 अंक वाले प्रश्न)
Question 23:
रासायनिक समीकरणों के संतुलन का महत्व समझाइए।
Answer:
🔵 संतुलन से हम यह सुनिश्चित करते हैं कि द्रव्यमान संरक्षण का नियम पूरा हो रहा है।
🟢 असंतुलित समीकरण में अभिकारकों और उत्पादों के परमाणुओं की संख्या अलग होती है।
🟡 संतुलन करने से दोनों ओर परमाणुओं की संख्या समान हो जाती है।
💡 उदाहरण:
असंतुलित – H₂ + O₂ → H₂O
संतुलित – 2H₂ + O₂ → 2H₂O
✔️ अतः समीकरण संतुलन रासायनिक अभिक्रियाओं को वैज्ञानिक रूप से सही रूप में दर्शाने के लिए आवश्यक है।
Question 24:
रासायनिक अभिक्रियाओं के प्रकारों को उदाहरण सहित विस्तार से समझाइए।
Answer:
🟢 (i) संयोजन अभिक्रिया: दो या अधिक पदार्थ मिलकर एक नया पदार्थ बनाते हैं।
➡️ उदाहरण: CaO + H₂O → Ca(OH)₂
🟡 (ii) अपघटन अभिक्रिया: एक यौगिक टूटकर अनेक पदार्थ बनाता है।
➡️ उदाहरण: 2Pb(NO₃)₂ → 2PbO + 4NO₂ + O₂
🔴 (iii) विस्थापन अभिक्रिया: अधिक क्रियाशील धातु कम क्रियाशील को विस्थापित करती है।
➡️ उदाहरण: Zn + CuSO₄ → ZnSO₄ + Cu
🔵 (iv) द्विविस्थापन अभिक्रिया: दो यौगिक आयनों का आदान-प्रदान करते हैं।
➡️ उदाहरण: Na₂SO₄ + BaCl₂ → BaSO₄ + 2NaCl
✔️ इन सभी से स्पष्ट होता है कि अभिक्रियाएँ विभिन्न रूपों में घटित होती हैं।
Question 25 (OR):
(क) उष्माक्षेपी और उष्माशोषी अभिक्रियाओं में अंतर स्पष्ट कीजिए।
Answer:
🔵 उष्माक्षेपी अभिक्रिया में ऊष्मा निकलती है।
🟢 उष्माशोषी अभिक्रिया में ऊष्मा अवशोषित होती है।
💡 उदाहरण:
➡️ उष्माक्षेपी – CH₄ + 2O₂ → CO₂ + 2H₂O + ऊष्मा
➡️ उष्माशोषी – 6CO₂ + 6H₂O + ऊष्मा → C₆H₁₂O₆ + 6O₂
✔️ इसलिए इनका व्यवहार ऊष्मा के प्रवाह पर निर्भर करता है।
Question 26:
रिडॉक्स अभिक्रिया क्या होती है? उदाहरण सहित समझाइए।
Answer:
💡 जब किसी अभिक्रिया में ऑक्सीकरण और अपचयन दोनों साथ होते हैं, तो उसे रिडॉक्स अभिक्रिया कहते हैं।
🔵 ऑक्सीकरण: ऑक्सीजन का जुड़ना या हाइड्रोजन का निकलना।
🟢 अपचयन: ऑक्सीजन का निकलना या हाइड्रोजन का जुड़ना।
➡️ उदाहरण: Zn + CuO → ZnO + Cu
✔️ यहाँ Zn का ऑक्सीकरण हुआ (ZnO में बदला) और CuO का अपचयन हुआ (Cu में बदला)।
Question 27:
दैनिक जीवन में रासायनिक अभिक्रियाओं की चार घटनाएँ उदाहरण सहित बताइए।
Answer:
🔵 लोहे में जंग लगना – Fe → Fe₂O₃·xH₂O
🟢 मोमबत्ती का जलना – CH₄ + 2O₂ → CO₂ + 2H₂O
🟡 भोजन का अपघटन – जटिल कार्बोहाइड्रेट → सरल शर्करा
🔴 प्रकाश संश्लेषण – 6CO₂ + 6H₂O + ऊष्मा → C₆H₁₂O₆ + 6O₂
✔️ ये सभी हमारे पर्यावरण में घटित होने वाली प्राकृतिक रासायनिक अभिक्रियाएँ हैं।
Question 28:
किसी रासायनिक अभिक्रिया में द्रव्यमान संरक्षण का प्रमाण उदाहरण सहित प्रस्तुत कीजिए।
Answer:
💡 नियम: “किसी रासायनिक अभिक्रिया में अभिकारकों और उत्पादों का कुल द्रव्यमान समान रहता है।”
➡️ उदाहरण: BaCl₂ + Na₂SO₄ → BaSO₄ + 2NaCl
🔵 Ba, Na, S, Cl और O के परमाणुओं की संख्या दोनों ओर समान है।
✔️ अतः यह अभिक्रिया द्रव्यमान संरक्षण सिद्धांत को प्रमाणित करती है।
Question 29 (OR):
(क) उत्प्रेरक क्या होता है? एक उदाहरण दीजिए।
Answer:
💡 उत्प्रेरक वह पदार्थ है जो अभिक्रिया की गति को प्रभावित करता है पर स्वयं उपभोग नहीं होता।
➡️ उदाहरण: MnO₂, KClO₃ के अपघटन में उत्प्रेरक का कार्य करता है।
2KClO₃ → 2KCl + 3O₂ (MnO₂ की उपस्थिति में)
✔️ MnO₂ अभिक्रिया की गति बढ़ाता है पर स्वयं अपरिवर्तित रहता है।
(ख) प्रकाशीय अपघटन अभिक्रिया का उदाहरण दीजिए।
Answer:
AgCl → Ag + Cl₂ (प्रकाश के प्रभाव में)
✔️ यह प्रकाशीय अपघटन अभिक्रिया है।
Question 30:
रासायनिक समीकरणों को संतुलित करने के मुख्य चरण संक्षेप में लिखिए।
Answer:
🔵 चरण 1: सबसे जटिल यौगिक से प्रारम्भ करें।
🟢 चरण 2: पहले धातु, फिर अधातु, फिर हाइड्रोजन, अंत में ऑक्सीजन को संतुलित करें।
🟡 चरण 3: आवश्यक गुणांक जोड़कर परमाणुओं की संख्या दोनों ओर समान करें।
🔴 उदाहरण: Fe + H₂O → Fe₃O₄ + H₂
➡️ संतुलन के बाद: 3Fe + 4H₂O → Fe₃O₄ + 4H₂
✔️ अब यह समीकरण पूर्णतः संतुलित है।
—————————————————————————————————————————————————————————————————————————————-
